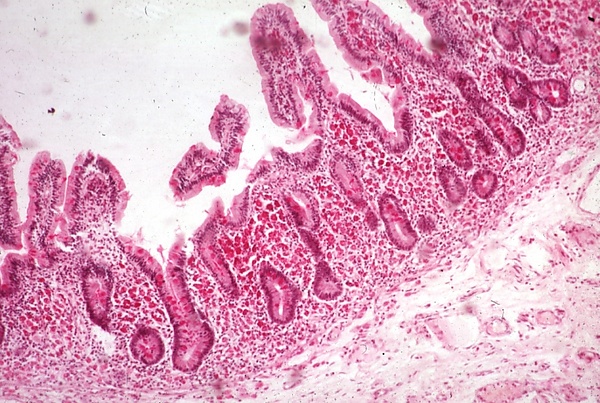
Болезнь Уиппла
Боле́знь Уи́ппла (БУ; интестина́льная липодистрофи́я, липогранулемато́з брыже́йки, хиладенэктази́я мезентериа́льная) представляет собой редкое инфекционное, системное рецидивирующее заболевание, вызываемое грамположительной бактерией Tropheryma whipplei. При этой патологии поражаются практически все органы, однако наиболее часто страдают двенадцатиперстная кишка, сердце, головной мозг и суставы. Заболевание отличается гетерогенностью клинической картины, что затрудняет его своевременную диагностику, и в отсутствие антибактериальной терапии может привести к летальному исходу[2].
Общие сведения
История
Первое описание БУ появилось в 1907 году, когда американский патолог Джордж Хойт Уиппл сообщил о результатах вскрытия пациента 36 лет, который на протяжении 5 лет жаловался на лихорадку, боли в суставах, кашель, диарею и потерю веса. При патологоанатомическом исследовании у этого пациента были обнаружены увеличенные лимфатические узлы и полисерозит. В стенке кишки и лимфатических узлах находили множественные отложения липидов и большое число макрофагов с аргирофильными палочкообразными структурами. Уиппл выдвинул два предположения о природе заболевания: инфекционная теория и нарушение метаболизма липидов, которое он счёл наиболее вероятной причиной. Он же предложил термин «интестинальная липодистрофия». В 1949 году Блэк-Шаффер в биоптатах лимфатических узлов и тонкой кишки пациентов с БУ обнаружил PAS-позитивные макрофаги, содержащие гликопротеин или мукополисахариды. В 1961 году Гардли и Хендрикс с помощью электронной микроскопии выявили палочкообразные тельца в цитоплазме макрофагов, а в 1992 году методом молекулярного секвенирования удалось идентифицировать возбудителя — бактерию Tropheryma whipplei[3].
Классификация
По клиническому течению выделяют[2]:
- классическую БУ;
- острая БУ (гастроэнтерит, пневмония, бактериемия);
- локальная БУ (энцефалит, эндокардит, артрит и другие проявления).
Этиология
Возбудителем болезни является Tropheryma whipplei — грамположительная актиномицета[4].
Патогенез
Точный патогенез БУ остаётся до конца не выясненным, однако имеющиеся данные свидетельствуют о важной роли иммунитета хозяина. Большинство людей, инфицированных Tropheryma whipplei, являются бессимптомными носителями или переносят ограниченную инфекцию с последующим формированием защитного гуморального и клеточного иммунитета. У заболевших воспалительный ответ на микроорганизм подавлен и характеризуется нарушением функции и активации макрофагов, а также ослаблением Т-клеточного ответа 1-го типа. Важную патогенетическую роль играют факторы хозяина, о чём свидетельствует двух- или трёхкратное повышение частоты встречаемости антигена HLA-B27 у поражённых лиц[5].
Попадая в тонкую кишку человека, бактерии захватываются макрофагами слизистой оболочки, которые затем мигрируют в подслизистый слой. Tropheryma whipplei способна подавлять иммунологический ответ, в результате чего макрофаги, несмотря на сохранную функцию фагоцитоза, теряют способность к лизису возбудителя. Внутри макрофагов микроорганизм размножается и вызывает снижение экспрессии CD11b — молекулы, отвечающей за созревание лизосом и внутриклеточную деградацию бактерий. При БУ возрастает экспрессия интерлейкинов IL-10 и IL-16, одновременно снижается уровень IFN-γ и IL-12, что приводит к неадекватной презентации антигена, препятствует стимуляции Т-хелперов 1-го типа и способствует размножению и системному распространению бактерии. Уровень IgG и IgM у больных низкий, что также указывает на несостоятельный гуморальный ответ[2].
Нарастающая инфильтрация поражёнными Tropheryma whipplei макрофагами приводит к сдавлению лимфатических сосудов ворсинок тонкой кишки, вызывая лимфостаз и синдром мальабсорбции. Первыми нарушению всасывания подвергаются жиры, которые постепенно накапливаются в собственной пластинке слизистой оболочки кишки — в связи с чем заболевание первоначально получило название «интестинальная липодистрофия» или «жировая липодистрофия». В дальнейшем нарушается абсорбция остальных макро- и микроэлементов. Апоптоз поражённых макрофагов сопровождается высвобождением возбудителя и его последующей диссеминацией через лимфатические и кровеносные сосуды. Tropheryma whipplei распространяется лимфогенным и гематогенным путём, в том числе через портальное кровообращение, поражая практически все органы: тонкую кишку, головной мозг, сердце, лёгкие, почки, костный мозг, кожу и суставы[2][6].
Эпидемиология
Согласно эпидемиологическим исследованиям БУ ограничены из-за небольшого числа наблюдений. Предполагаемая распространённость составляет от 0,5 до 1 случая на 1 000 000 населения. Мужчины болеют в 3-5 раз чаще женщин, а пик заболеваемости приходится на возраст 50-60 лет. БУ более распространена среди представителей европеоидной расы, однако отдельные случаи описаны у испанцев, индусов, а также у лиц негроидной и монголоидной рас. Среди заболевших преобладают жители сельской местности, чаще всего работники сельского хозяйства. Также описаны семейные случаи заболевания[3].
Диагностика
Классическое течение БУ включает раннюю, среднюю и позднюю фазы. Ранняя продромальная фаза длится менее 6 лет и характеризуется перемежающейся артралгией или серонегативным артритом, который встречается в 80 % случаев, а также лихорадкой. Промежуточная фаза продолжается от шести до восьми лет и проявляется диареей, синдромом мальабсорбции, потерей веса и болями в животе. Поздняя фаза развивается после восьми лет болезни, когда начинают преобладать неврологические симптомы. Для БУ типичен олиго- или полиартрит преимущественно крупных суставов. Половина пациентов имеют системные симптомы, включая утомляемость и ночную потливость. БУ может имитировать палиндромный ревматизм с картиной инфекционного артрита. Ревматологическими проявлениями также могут быть хронический бурсит и теносиновит, не поддающиеся терапии метотрексатом и этанерцептом. У некоторых пациентов отмечаются боли в нижней части спины за счёт спондилоартропатии, причём возможно развитие анкилозирующего спондилита и реактивного артрита[2].
Желудочно-кишечные симптомы возникают в развёрнутую стадию болезни. Пациентов беспокоит диарея, схваткообразная абдоминальная боль, прогрессирующая потеря веса вплоть до кахексии, а также анорексия и признаки синдрома мальабсорбции. Также могут наблюдаться скрытые кишечные кровотечения. Гепатобилиарные проявления отмечаются редко и включают боль в правом подреберье, увеличение печени и селезёнки, асцит и желтуху. При наличии диареи описаны случаи ошибочной диагностики воспалительных заболеваний кишечника, что приводило к резкому прогрессированию БУ на фоне иммуносупрессивной терапии с угрозой летального исхода[2].
Неврологические симптомы могут быть проявлением классической формы болезни, рецидива при ранее леченной форме или изолированной инфекции центральной нервной системы. Симптомы поражения центральной и периферической нервной системы включают глазодвигательные синдромы, мозжечковую атаксию, судорожный синдром, экстрапирамидные нарушения, гиперсомнию, психические расстройства, когнитивные нарушения вплоть до деменции, а также асептический менингит. Патогномоничными для БУ со стороны центральной нервной системы считается миоклонии — синхронные сокращения жевательных или лицевых мышц[2].
Поражения сердечно-сосудистой системы при БУ встречаются часто. У части больных выслушивается систолический шум на верхушке сердца или шум трения перикарда; также могут развиваться нарушения проводимости и застойная сердечная недостаточность. Эндокардит, вызванный Tropheryma whipplei, занимает значимое место среди эндокардитов с отрицательной гемокультурой. Данный эндокардит можно заподозрить у белых мужчин в возрасте около 50 лет с симптомами сердечной недостаточности, разрушением сердечного клапана или острым ишемическим инсультом. Наиболее часто поражается аортальный клапан, реже — митральный и трикуспидальный, что нередко требует протезирования. Также описан случай изолированного констриктивного перикардита в сочетании с многоклапанным панкардитом[2].
Кожные поражения при БУ включают гиперпигментацию, узловатую эритему, панникулит и подкожные узелки. Гиперпигментация скуловой и орбитальной областей, гиперкератоз, пурпура, глоссит, хейлит и гингивит могут возникать вторично вследствие дефицита микронутриентов. Офтальмологические проявления протекают с картиной увеита, ретинита, неврита зрительного нерва, изменениями эпителия хрусталика и двустороннего миозита глазодвигательных мышц. Поражение органов дыхания отмечается в виде кашля, одышки, выпота в плевральную полость и лёгочной гипертензии. Редко возбудитель может вызывать пневмонию, в том числе тяжёлую. Кроме того, при БУ описаны случаи спонтанного тромбоза подвздошно-бедренной вены[2].
Клинический анализ крови: характерны лейкоцитоз и тромбоцитоз, а также повышение скорости оседания эритроцитов. Возможна железодефицитная анемия[6].
Биохимический анализ крови: возможны гипопротеинемия, гипоальбуминемия и гипохолестеринемия[6].
Гистологическое исследование биоптатов поражённых тканей: характерно обнаружение в собственной пластинке слизистой оболочки биоптатов тонкой кишки, а также в образцах периферических или брыжеечных лимфатических узлов, печени, селезёнки, сердечных клапанов, ткани головного мозга, стекловидного тела и синовиальной оболочки так называемых PAS-положительных пенистых макрофагов, которые содержат лизосомальный материал разрушенных бактерий, фагоцитированных этими же клетками[2].
Полимеразная цепная реакция используется для обнаружения возбудителя в крови или в поражённых тканях[6].
При эндоскопическом исследовании верхних отделов желудочно-кишечного тракта у пациентов с БУ выявляется бледно-розовая слизистая оболочка двенадцатиперстной и тощей кишки с диффузной лимфангиэктазией. Применение эндоскопии высокого разрешения и узкоспектральных режимов позволяет определить, что ворсинки отёчны, булавовидно утолщены на концах и содержат белесоватые включения[2].
Дифференциальная диагностика
Дифференциальную диагностику БУ проводят со следующими заболеваниями[5]:
- ВИЧ;
- туберкулёз;
- воспалительное заболевание кишечника с артропатией;
- заболевания соединительной ткани;
- гипертиреоз.
Осложнения
Лечение
Схемы лечения БУ в разных странах варьируют, однако все они основаны на способности антибактериальных средств проходить через гематоэнцефалический барьер. К препаратам выбора относят антибиотики пенициллинового ряда, тетрациклины, а также комбинацию триметоприма с сульфаметоксазолом. При отсутствии ответа на антибактериальную терапию перспективно применение интерферона-гамма. Типичный подход включает индукционную терапию внутривенными антибиотиками в течение примерно двух недель, после чего переходят на поддерживающую пероральную терапию сроком до одного года. При поражении центральной нервной системы дозы препаратов удваивают или назначают более интенсивные схемы с использованием антибиотиков пенициллинового ряда в комбинации со стрептомицином. Применение глюкокортикоидов имеет вспомогательное значение. При необходимости проводится коррекция последствий синдрома мальабсорбции[3][6].
Прогноз
При своевременно начатом лечении прогноз при БУ в целом благоприятный. Однако в 8-35 % случаев возможны рецидивы заболевания, что требует динамического наблюдения за пациентами. Без назначения антибактериальной терапии болезнь может закончиться летальным исходом, который, как правило, наступает через 1-2 года от момента появления кишечных симптомов[6].
Диспансерное наблюдение
Пациенты с БУ нуждаются в диспансерном наблюдении гастроэнтеролога и инфекциониста. Объём и частота контрольных обследований определяются индивидуально[5].
Профилактика
Не разработана.
Примечания
Литература
- Мехтиев С. Н., Мехтиева О. А., Калинина Е. Ю., и др. Болезнь Уиппла: клинический случай и обзор литературы // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2023. — Т. 33, № 6. — С. 88—100. — doi:10.22416/1382-4376-2023-33-6-88-100.
- Ahmad A. I., Wikholm C., Pothoulakis I., et al. Whipple’s disease review, prevalence, mortality, and characteristics in the United States: A cross-sectional national inpatient study (англ.) // Medicine. — 2022. — 9 December (vol. 101, no. 49). — P. e32231. — doi:10.1097/MD.0000000000032231.
- Дробязгин Е. А., Попов А. Л., Аникина М. С., и др. Болезнь Уиппла: обзор литературы и клиническое наблюдение // Доказательная гастроэнтерология. — 2020. — Т. 9, № 4. — С. 74—82. — doi:10.17116/dokgastro2020904174.
- Куприянова И. Н., Стафилова М. В. Болезнь Уиппла: этиология, патогенез, клиника, диагностика и лечение // Экспериментальная и клиническая гастроэнтерология. — 2023. — № 9 (217). — С. 238—246. — doi:10.31146/1682-8658-ecg-217-9-238-246.