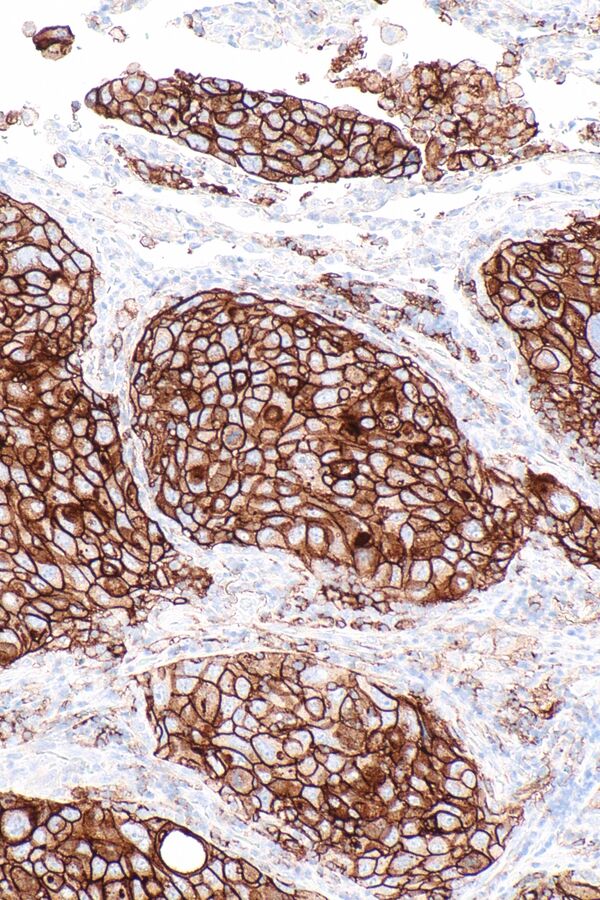
Немелкоклеточный рак лёгкого
Немелкоклеточный рак лёгкого (НМРЛ, немелкоклеточная карцинома лёгкого) — одна из часто диагностируемых злокачественных опухолей[1], характеризуется крайней агрессивностью из-за высокой митотической активности и раннего метастазирования[2], имеет самую высокую статистику смертности во всём мире[источник?].
Что важно знать
Классификация
- аденокарцинома;
- плоскоклеточный рак лёгкого;
- крупноклеточная карцинома[источник?].
- Центральный рак лёгкого — формируется из эпителия в крупных бронхах (главном, долевом, сегментарном и субсегментарном). По направлению роста выделяют: экзофитный рак, при котором опухоль растёт в просвет бронха; эндофитный рак — характеризуется ростом опухоли в толщу лёгочной паренхимы; разветвлённый рак — перибронхиальный рост.
- Периферический рак лёгкого — возникает из эпителия более мелких бронхов или локализуется в паренхиме лёгкого. Различают узловую округлую опухоль, пневмониеподобный рак и рак верхушки лёгкого.
- Атипичные формы рака — медиастинальная форма, милиарный карциноматоз[источник?].
- T — первичная опухоль
- Тх — первичная опухоль не может быть оценена или опухоль доказана наличием злокачественных клеток в мокроте или бронхиальных смывах, но не визуализируется рентгенологическими методами или при проведении бронхоскопии;
- Т0 — первичная опухоль не определяется;
- Тis — неинвазивный рак (carcinoma in situ);
- T1 — опухоль 3 см или менее в наибольшем размере, окружена лёгочной паренхимой или висцеральной плеврой, опухоль не локализуется в главном бронхе;
- T1mi — минимально инвазивная аденокарцинома;
- T1a — опухоль 1 см или менее в наибольшем размере;
- T1b — опухоль от 1 до 2 см в наибольшем измерении;
- T1c — опухоль от 2 до 3 см в наибольшем размере;
- Т2 — опухоль от 3 до 5 см; или опухоль со следующим распространением: вовлечён главный бронх, но без вовлечения карины; врастает в висцеральную плевру; связана с ателектазом или обструктивным пневмонитом, который распространяется в прикорневых отделах, включая часть или все лёгкое;
- T2a — опухоль от 3 до 4 см или размер не может быть определён;
- T2b — опухоль от 4 до 5 см;
- ТЗ — опухоль более 5 см, но не более 7 см или с инвазией в: грудную стенку; диафрагмальный нерв; париетальный перикард либо наличие другого опухолевого узла в той же доле, что и первичный узел;
- Т4 — опухоль более 7 см или любого размера с инвазией в диафрагму, средостение, сердце, крупные сосуды, трахею, возвратный нерв, пищевод, тела позвонков, висцеральный перикард, отдельный опухолевый узел в другой ипсилатеральной доле, нежели первичная опухоль.
- N — регионарные лимфатические узлы
- Nх — недостаточно данных для оценки состояния регионарных лимфатических узлов;
- N0 — нет метастазов в регионарных лимфатических узлах;
- N1 — метастазы в ипсилатеральных перибронхиальных и/или ипсилатеральных корневых лимфатических узлах, или метастазы во внутрилегочных лимфатических узлах, включая прямое поражение лимфатических узлов;
- N1a — поражены лимфатические узлы одного коллектора N1;
- N1b — поражены лимфатические узлы нескольких коллекторов N1;
- N2 — метастазы в ипсилатеральных медиастинальных и/или субкаринальных лимфатических узлах;
- N2a — поражены лимфатические узлы у одного коллектора N2 без вовлечения лимфатических узлов коллектора N1;
- N2a2 — поражены лимфатические узлы одного коллектора N2 с вовлечением лимфатических узлов коллектора N1;
- N2b — множественное вовлечение лимфатических узлов коллектора N2;
- N3 — в виде остеоартропатии.
- М — отдалённые метастазы
- Мх — недостаточно данных для определения отдалённых метастазов;
- М0 — нет признаков отдалённых метастазов;
- M1 — есть отдалённые метастазы;
- М1а — опухолевые узлы в контралатеральном лёгком, опухолевое узелковое поражение плевры, метастатический плевральный или перикардиальный выпот;
- М1b — одиночный отдалённый опухолевый узел;
- M1c — множественные внелёгочные метастазы в одном или нескольких органах[3][4].
Этиология
Курение табака является основной причиной появления болезни, но в 10-25 % случаев она возникает у никогда не куривших людей[5].
Другие факторы риска:
- наличие хронической обструктивной болезни лёгких в анамнезе;
- профессии, связанные с контактом с углём, алюминием, асбестом, радоном и другими веществами;
- наследственный анамнез;
- раннее проведённая лучевая терапия других опухолей внутригрудной локализации[источник?].
Патогенез
Значимую роль в патогенезе немелкоклеточного рака лёгкого играют эпигенетические механизмы: метилирование ДНК, реорганизация хроматина и регуляция экспрессии генов с помощью микроРНК. Экспрессия генов меняется среди подтипов НМРЛ и в зависимости от факторов окружающей среды, особенно от воздействия сигаретного дыма. Активация арил-углеводородного рецептора (AhR) одним из компонентов табачного дыма — бензо(а)пиреном — является одним из звеньев канцерогенеза лёгкого, но изменения экспрессии AhR-зависимых генов-мишеней и микроРНК, остаются недостаточно изученными. Существуют различные механизмы нарушения экспрессии генов-супрессоров и онкогенов, что также играет важную роль в развитии подтипов рака. Наибольший интерес представляют гены TP53, KRAS, PTEN[источник?].
Для аденокарциномы лёгкого характерны драйверные мутации в гене EGFR, прежде всего Del19 и L858R, которые усиливают онкогенную функцию рецептора, что сопровождается усилением пролиферации клеток опухоли. Однако встречаются и более редкие молекулярные перестройки: транслокация ALK (частота 4-6 %), ROS1 (1-2 %), мутация в гене BRAF (около 1 %). При плоскоклеточном раке таких мутаций в настоящее время не обнаружено[источник?].
По выраженностью и распространённостью признаков ороговения подразделяется на высокодифференцированный (ороговевающий) и низкодифференцированный (неороговевающий) тип. Плоскоклеточный ороговевающий рак отличается множеством изолированных клеток опухоли. Форма клеток — от округлой до полигональной. Форма ядра также разнообразна (округлая, овальная, треугольная, палочковидная). Характерна гиперхромность, крупноглыбчатая структура хроматина. Ядрышки редки. Размеры клеток — от мелких до гигантских. Митозы происходят редко. Плоскоклеточный неороговевающий рак имеет признаки плоскоклеточной дифференцировки в клетках опухоли. Ороговение присутствует лишь в единичных изолированных клетках. Их форма разнообразна, они крупного размера. Ядра большие, полиморфные, гиперхромные, расположены по центру, имеют неровный контур. Часто присутствуют одно или несколько крупных ядрышек. Встречаются митозы. Цитоплазма чаще плотная, светло-голубая. Наиболее редкий вариант плоскоклеточного рака представлен единичными полигональными крупными клетками с немногочисленными клеточными мостиками. В таком случае цитоплазмы немного, и она в виде узкого ободка. Ядра крупные, расположены центрально[3].
Представлен большими полиморфными недифференцированными клетками. Ядра крупные, полиморфные, гиперхромные, с неровными контурами, неравномерной структурой хроматина, с множественными ядрышками. Высокое ядерноцитоплазматическое соотношение. Выраженный опухолевый диатез. Цитоплазма обильная, светлого цвета[3].
Эпителиальная опухоль с признаками железистой дифференцировки клеток и формированием ацинарных, папиллярных, бронхиолоальвеолярных или солидных клеточных структур. Характерно слизеобразование. Ядра в клетках эксцентрично расположены, структура хроматина и число ядрышек разнообразны, также возможна многоядерность. Цитоплазма гомогенная, пенистая или мелковакуолизированная. В некоторых случах может быть базофильная. Слизь в цитоплазме может накапливаться в большом количестве, смещая ядро и растягивая цитоплазму, формируя перстневидную форму клеток. При ацинарной аденокарциноме в большом количестве присутствуют ацинусоподобные структуры, при папиллярной — папиллоподобные, при муцинозной аденокарциноме в препарате присутствует большое количество слизи, при перстневидноклеточной опухоли в препарате обнаруживается большое количество перстневидных клеток[3].
Эпидемиология
НМРЛ является одной из лидирующих онкологий с низкой 5-летней выживаемостью. В 2018 г. от него умерло более 1,7 млн человек (18,4 % от общего числа смертей от рака во всем мире) в связи с тем, что у более половины случаев диагноз выявляется на поздней стадии[6].
Немелкоклеточная карцинома лёгких встречается примерно в 85 % случаев онкологических заболеваний лёгких, среди которых преобладают аденокарциномы (30-45 %) и плоскоклеточные опухоли (25-40 %). При исследовании пациентов с диагностированным НМРЛ в возрасте от 20 до 46 лет, был сделан вывод, что преимущественно пациентами являются женщины, с гистологическим типом аденокарциномы, некурящие, которые в большинстве случаев имеют местно-распространённую или метастатическую форму заболевания[источник?].
Диагностика
У пациентов наблюдаются следующие симптомы:
- Слабость;
- Утомляемость;
- Кашель (с нарастанием обтурации бронха может сопровождаться выделением мокроты слизистого или слизисто-гнойного характера);
- Одышка;
- Боль в груди (может быть обусловлена локализацией новообразования в плащевой зоне лёгкого, а также наличием плеврального выпота или ателектаза лёгкого с признаками обтурационного пневмонита);
- Кровохарканье (может проявляться в виде прожилок алой крови в мокроте или в виде диффузно окрашенной мокроты);
- Снижение аппетита;
- Синдром верхней полой вены (характерно для медиастинального рака);
- Синдром Панкоста: боль в участке плечевого сустава и плеча, атрофия мышц предплечья (характерно для периферического рака верхушки лёгкого);
- Повышение температуры тела;
- Признаки обтурационной пневмонии (характерно для центрального рака лёгких)[3].
Также возможно бессимптомное течение или проявление паранеопластических синдромов (синдромы гиперпродукции адренокортикотропного, антидиуретического, паратиреоидного гормонов, эстрогенов, серотонина) в виде остеоартропатии, синдрома Кушинга, мигрирующего тромбофлебита, нейропатии и миопатии[3].
- Клинический анализ крови;
- биохимический анализ крови;
- общий анализ мочи;
- молекулярно-генетическое исследование и изучение биомаркеров в опухоли: определение активирующих мутаций EGFR (18-21 экзон), транслокации ALK, транслокации ROS1, мутации BRAF V600E, экспрессия PD-L1. По необходимости: транслокации гена RET, мутации пропуска 14 экзона гена c-MET, мутации гена KRAS, мутации 20 экзона гена HER2, определение последовательности вставок (инсерций) в 20 экзоне гена EGFR, транслокации генов семейства NTRK;
- коагулологические исследования;
- гистологическое исследование биоптата с определением морфологического типа НМРЛ[7];
- Рентгенография и компьютерная томография органов грудной клетки, также в отдельных случаях возможно ПЭТ-КТ;
- При планировании хирургического этапа лечения проводится оценка функции лёгких: форсированная жизненная ёмкость лёгких; объём форсированного выдоха за 1 секунду; по возможности — диффузионный тест;
- Фибробронхоскопия[источник?].
Для уточнения распространённости заболевания или при подозрении на метастазирование:
- Ультразвуковое исследование или КТ органов брюшной полости с внутривенным контрастированием;
- Ультразвуковое исследование шейно-надключичных зон;
- Остеосцинтиграфия;
- МРТ или КТ головного мозга с контрастным усилением[источник?].
Дифференциальная диагностика
- Турбекулёз;
- Другие нозологические варианты карциномы лёгких[3].
Осложнения
- Метастазирование в головной мозг[источник?].
Лечение
Один из основных методов лечения — хирургический. Объём проведения операции определяется распространённостью опухолевого процесса, гистологической формой опухоли и функциональным состоянием пациента. Пациенты с 0-IIIА стадиями считаются операбельными, с IIIB (T3N2) — потенциально операбельными. При этом радикальное вмешательство удаётся выполнить только у 10-20 % пациентов. Стандартный объём операции включает в себя анатомическую резекцию лёгкого (лобэктомия, билобэктомия) с ипсилатеральной медиастинальной лимфодиссекцией. Однако у 30-55 % диагностируется рецидив заболевания в виде отдалённых метастазов, преимущественно в первые два года после радикального вмешательства, поэтому необходим системный подход к лечению[источник?].
Комплексный подход к каждому пациенту обеспечивает выбор оптимальной и реализуемой стратегии, учитывая современные возможности лечения, в том числе использование комбинированных методов. Консервативная терапия включает применение химиотерапии, лучевой терапии, иммуноонкологических препаратов, в частности ингибиторов контрольных точек иммунного ответа (в рамках паллиативного лечения диссеминированных форм и консолидирующего лечения больных с нерезектабельным НМРЛ), таргетной терапии (у больных с наличием драйверных мутаций в генах EGFR, ALK, ROS1, BRAF). В некоторых случаях показано проведение адьювантной химиотерапии, что позволяет увеличить 5-летнюю выживаемость на 5,4 %. Для уменьшения объёма опухоли и повышения резектабельности при поздних стадиях проводится неоадъювантная химиотерапия[источник?].
Лечение пациентов с IV стадией расценивается как паллиативное. Оно направлено на увеличение продолжительности жизни и улучшение её качества за счёт раннего начала поддерживающей и симптоматической терапии[источник?].
Прогноз
Общая 5-летняя выживаемость с НМРЛ составляет 18 %, так как обычно на момент диагностирования у пациентов уже имеются метастазы. При прогнозировании учитывается морфология первичной опухоли, которая признаётся в качестве надёжного предиктора биологического поведения новообразования при раке лёгких. Также неблагоприятным прогностическим фактором является распространение опухолевых клеток по лимфатическим сосудам[8].
Диспансерное наблюдение
Задача наблюдения заключается в своевременном выявлении прогрессирования болезни для скорейшего начала химиотерапии либо оперативного вмешательства с удалением операбельных метастазов и рецидивирующих новообразований[источник?].
Рекомендуемая частота осмотров онколога для пациентов, находящихся в удовлетворительном состоянии после радикальной терапии следующая: первые три года обследования проводятся каждые 3 месяца, в четвёртый и пятый годы — каждые 6 месяцев. Для контроля используются физикальный осмотр, УЗИ и рентгенография органов грудной клетки либо компьютерная томография. Магнитно-резонансная томография головного мозга и остеосцинтиграфия выполняются ежегодно. После 5 лет с момента операции пациенты обследуются один раз в год[источник?].
Профилактика
- Отказ от активного и пассивного курения. Существует прямо пропорциональная зависимость между выкуриваемых за день количеством сигарет и риском возникновения рака лёгких;
- Своевременное лечение заболеваний лёгких;
- Использование современных средств защиты лицам, контактирующим с асбестом, хромом, никелем, кадмием, мышьяком, дизельным топливом[источник?].