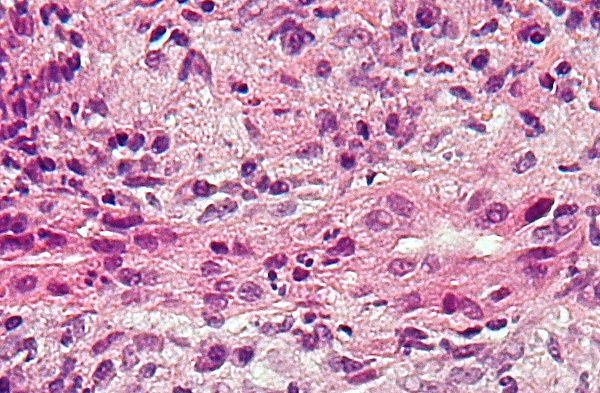
Первичный билиарный холангит
Перви́чный билиа́рный холанги́т (ПБХ) — это хроническое медленно прогрессирующее холестатическое заболевание печени неизвестной этиологии, при котором первоначально поражаются внутридольковые и септальные жёлчные протоки, а в завершающей стадии развиваются цирроз печени и печёночная недостаточность[2].
Что важно знать
История
Первое описание заболевания относится к 1851 году, когда Аддисон и Гулл описали клиническую картину прогрессирующей желтухи в отсутствие механической обструкции крупных жёлчных протоков. Термин «первичный билиарный цирроз» был предложен в 1949—1950 годах двумя исследовательскими группами . Однако, на Международной согласительной конференции 1965 года E. Rubin и соавт. рекомендовали использовать название «негнойный деструктивный хронический холангит», которое некоторые учёные считают более точным. Однако в 2014 и 2015 годах Европейская ассоциация исследования печени (EASL) и Американская ассоциация исследования печени (AASLD) одобрили изменение названия с «первичного билиарного цирроза» на «первичный билиарный холангит»[3][4][5][6][7].
Эпидемиология
Частота ПБХ варьируется в зависимости от стран и континентов, составляя от 40 до 400 случаев на 1 миллион населения. Заболевание чаще встречается в развитых странах Европы и Северной Америки, особенно в северных регионах Европы, где его частота достигает 1 случая на 700 человек (около 2,7-3,2 случаев на 100 тысяч населения ежегодно). ПБХ составляет около 2 % в структуре летальности. Среди заболевших доминируют женщины в возрасте от 40 до 60 лет, соотношение мужчин и женщин — 1:9 (90 % пациентов — женщины). Преобладание женщин связывают с моносомией по X-хромосоме в Т- и В-лимфоцитах периферической крови. В 84 % случаев ПБХ сопутствуют внепечёночные аутоиммунные заболевания, такие как синдром Шёгрена, системная красная волчанка, системная склеродермия, ревматоидный артрит, тиреоидит Хашимото, язвенный колит и другие[2][4][8][9].
Этиология и патогенез
Этиология ПБХ остаётся неясной. Среди возможных причин рассматривались различные бактерии, такие как Escherichia coli, Salmonella minnesota, Chlamydia pneumoniae, Staphylococcus aureus, Mycobacterium tuberculosis и другие. Было отмечено, что ПБХ часто сопровождается инфекциями мочевыводящих путей, основным возбудителем которых являются R-формы Escherichia coli. Поначалу предполагали возможную связь заболевания с инфекцией Helicobacter pylori, но выяснилось, что её частота при ПБХ не отличается от таковой у здоровых людей. Доказать участие бактериальной инфекции в этиологии ПБХ не удалось, так как в ткани печени не удалось обнаружить генетический материал каких-либо бактерий[2][10][11][12].
В патогенезе ПБХ участвуют аутоиммунные механизмы, внутрипечёночный холестаз, генетические и экологические факторы. Рассматривалась также гипотеза об этиологической роли эндогенных ретровирусов, а также цитомегаловируса и вируса Эпштейна-Барр, однако она не подтвердилась методами доказательной медицины[13][14].
Генетическая предрасположенность к первичному ПБХ выражена относительно слабо. Исследования на монозиготных близнецах, происходивших из семей с больными ПБХ, показали, что заболевание не проявляется с полной пенетрантностью. Среди 8 монозиготных близнецов с наследственным риском развития ПБХ, болезнь была диагностирована у 5 из них. Среди 1118 ближайших родственников больных (первой степени родства), ПБХ был выявлен лишь у 8 человек. В целом, частота «семейных накоплений» составляет 4—6 %[2][15][16].
У 95 % пациентов с ПБХ в крови обнаруживаются аутоантитела к аутоантигенам внутренней мембраны митохондрий холангиоцитов (АМА), что служит основным индикатором аутоиммунных механизмов, участвующих в развитии заболевания, и является высокоспецифическим маркером ПБХ. В 1982 году с помощью молекулярного клонирования был выявлен кетоацидодегидрогеназный мукопротеиновый комплекс OADC, который является основным аутоантигеном ПБХ, ассоциированным с АМА. Показано, что аутоантитела против компонентов OADC представляют собой АМА-М2-аутоантитела, характерные для данного заболевания. Ключевыми аутоантигенами OADC являются Е2-субъединицы пируватдегидрогеназного комплекса (PDC-Е2), дегидрогеназа кетокислот с разветвлённой цепью (ВСО-PDC-Е2) и оксоглутаровая дегидрогеназа (OGDC-Е2). У пациентов с ПБХ в сыворотке крови обычно выявляют аутоантитела, реагирующие с PDC-Е2 .Основная мишень иммунного ответа — эпителий жёлчных протоков. АМА связываются с апикальной мембраной холангиоцитов, активируя Т-лимфоциты и усиливая воспалительный процесс. Т-лимфоциты Th1 стимулируют провоспалительные цитокины, такие как интерлейкин-2 и интерферон-γ, вызывая апоптоз эпителия жёлчных протоков. Поскольку митохондрии — источник свободных радикалов в организме, их роль также важна в развитии заболевания[2][9][10][17][18][19][20].
Роль факторов внешней среды в развитии первичного ПБХ недостаточно изучена. Однако установлена связь заболевания с интенсивным курением: чем продолжительнее и интенсивнее курение (до 100 сигарет в день), тем выше риск развития болезни, что измеряется показателем «пачко/лет». Среди больных ПБХ 76 % являются многолетними курильщиками (в контрольной группе — 56 %; p < 0,05). У курильщиков наблюдается более быстрое прогрессирование фиброза печени, активизация воспалительного процесса и повышение уровня провоспалительных цитокинов (ИФНγ, ИЛ-2). У пациентов с ПБХ часто наблюдается дефицит эстрогенов, что может объяснять значительное преобладание женщин среди больных. В патогенезе ПБХ также важную роль играют ксенобиотики (вещества, чуждые организму человека, такие как фармакопрепараты, пестициды и органические соединения), которые метаболизируются в печени. Эти вещества оказывают токсическое воздействие на печень, усиливая процессы апоптоза и вызывая некроз гепатоцитов и холангиоцитов, что способствует образованию аутоантигенов. Некоторые исследователи отмечают возможную патогенетическую роль инфекций мочевыводящих путей, которые встречаются у 35 % пациентов с ПБХ и чаще всего вызваны R-формой Escherichia coli[2][15][21].
Клиническая картина
Для ПБХ характерно длительное латентное течение. Даже через 10 лет после начала заболевания скрытое течение сохраняется у 15 % больных. Люди с первичным ПБХ часто испытывают усталость (80 %), что является неспецифическим симптомом, но может быть изнуряющим и значительно снижать качество жизни. Его патогенез до сих пор не выяснен, и это затрудняет как исследование его специфичности, так и лечение. Следует оперативно выявлять и лечить сопутствующие заболевания, которые могут способствовать или ухудшать усталость, такие как депрессия, гипотиреоз, анемия, ожирение или побочные эффекты медикаментов. Также часто встречаются сухость кожи и сухость глаз. Зуд наблюдается у 20-70 % больных и может развиться на любом этапе заболевания. Часто описывается зуд в области стоп и ладоней, однако, пациенты могут испытывать зуд на коже головы, лице, спине или других участках. Обычно зуд имеет умеренную или слабую интенсивность, может проявляться как покалывание или жжение, и может возникать даже при нормальных показателях функции печени. Он не связан с прогрессией заболевания печени и может уменьшаться или исчезать по мере его развития. Влияние на качество жизни и ночной сон также связано с усталостью. Зуд может быть крайне редким, не поддающимся лечению и требующим трансплантации печени. Обычно зуд бывает прерывистым, усиливается ночью и проходит летом. У людей с более тяжёлыми формами ПБХ может развиться желтуха (пожелтение глаз и кожи). ПБХ также снижает плотность костей, что повышает риск переломов. Может наблюдаться ксантелазма (кожные поражения вокруг глаз) или другие ксантомы в результате повышенного уровня холестерина. Тяжесть проявление клинических симптомов может варьироваться в зависимости от печёночной недостаточности, возникающей на фоне основного заболевания[22][23].
Осложнения
ПБХ может прогрессировать с исходов в цирроз печени, что, в свою очередь, может привести к ряду симптомов или осложнений, включая:
- асцит — задержка жидкости в животе;
- увеличение селезёнки (спленомегалия);
- варикозное расширение вен пищевода;
- печёночная энцефалопатия;
- развитие холангиокарциномы;
- холелитиаз.
Кроме того, у людей с ПБХ иногда могут наблюдаться признаки сопутствующего экстрагепатального аутоиммунного заболевания, такого как заболевания щитовидной железы, ревматоидный артрит или синдром Шёгрена (в до 80 % случаев)[23][24].
Диагностика
Большинство пациентов с ПБХ диагностируются на бессимптомной стадии, когда они были направлены к гепатологу из-за аномальных результатов анализов на функцию печени (чаще всего повышение гамма-глютамилтранферазы или щелочной фосфатазы) при проведении ежегодных скрининговых анализов. Другие распространённые случаи включают скрининг пациентов с аутоиммунными заболеваниями, не связанными с печенью, такими как ревматоидный артрит, исследование повышенного уровня холестерина, оценку зуда или неразрешённый холестаз после родов. Диагностика ПБХ обычно не вызывает затруднений. Основой для окончательного диагноза являются следующие факторы:
- Аномалии в анализах на печёночные ферменты обычно присутствуют, и повышенные уровни гамма-глутамилтрансферазы и щелочной фосфатазы могут быть обнаружены на ранних стадиях заболевания. Повышение билирубина наблюдается на более поздних стадиях.
- Аутоантитела против митохондрий (АМА) являются характерным серологическим маркером для ПБХ, обнаруживаемым у 90-95 % пациентов и только у 1 % контрольной группы. Пациенты с ПБХ имеют АМА против комплекса пируватдегидрогеназы (PDC-E2), ферментного комплекса, который находится в митохондриях. У тех, кто является АМА-отрицательным, но имеет заболевания, схожие с ПБХ, могут быть обнаружены АМА при использовании более чувствительных методов диагностики.
- Могут присутствовать другие аутоантитела:
- измерения антиядерных антител не являются диагностическим значимыми для ПБХ, так как они не являются специфичными, но могут иметь значение для прогноза;
- анти-гликопротеин-210 антитела, а в меньшей степени анти-p62 антитела, коррелируют с прогрессированием заболевания до терминальной стадии печёночной недостаточности. Анти-gp210 антитела обнаруживаются у 47 % пациентов с ПБХ;
- анти-центромерные антитела часто коррелируют с развитием портальной гипертензии;
- анти-np62 и анти-sp100 антитела также ассоциируются с ПБХ.
- Для исключения блокировки жёлчных протоков обычно выполняется ультразвуковое исследование, магнитно-резонансная холангиопанкреатография или компьютерная томография. Это необходимо, если требуется исключить заболевания, вызывающие вторичный билиарный цирроз, такие как заболевания жёлчных протоков или жёлчные камни. Также может быть полезна биопсия печени, и если остаются сомнения, как в некоторых случаях, может быть выполнена эндоскопическая ретроградная холангиопанкреатография — эндоскопическое исследование жёлчного протока.
- С учётом высокой специфичности серологических маркеров биопсия печени не является необходимой для диагностики ПБХ, однако она все ещё требуется, если ПБХ-специфические антитела отсутствуют или подозревается сопутствующий аутоиммунный гепатит или неалкогольный стеатогепатит. Биопсия печени может быть полезна для стадирования заболевания, оценки фиброза и дуктопении (дефицита жёлчных протоков). Также она может быть уместна при наличии других экстрагепатальных сопутствующих заболеваний[23][25][26][27].
Для морфологического исследования печени при ПБХ необходимо получить 5—9 биоптатов в связи с мозаичностью её поражения при этом заболевании. На основании результатов морфологического исследования биоптатов различают 4 стадии гистологических изменений в печени:
- I стадия — хронического негнойного деструктивного холангита;
- II стадия пролиферация холангиол; перидуктулярный фиброз;
- III стадия: фиброз стромы печени и наличие воспалительных инфильтратов;
- IV стадия: признаки монолобулярного цирроза печени; синдром исчезновения жёлчных протоков малого и среднего калибра[28][29].
Лечение
Поскольку этиология ПБХ не установлена, специфического этиотропного лечения не существует. В разное время для лечения больных ПБХ использовались препараты из различных фармакологических групп, в первую очередь с иммуносупрессивным действием. К ним относятся глюкокортикостероиды (ГКС) — такие как преднизолон, метипред, будесонид, а также нестероидные иммуносупрессоры, такие как азатиоприн, метотрексат, циклоспорин А и другие. Также изучались препараты, оказывающие антифибротическое действие (например, Д-пеницилламин), а также средства с антимитотическим и противовоспалительным эффектом, такие как колхицин. Однако эффект этих препаратов оказался ограниченным (например, ГКС, азатиоприн, метотрексат, циклоспорин А) или полностью отсутствовал (Д-пеницилламин, колхицин, хлорамбуцил). Кроме того, для части этих препаратов был отмечен высокий риск развития серьёзных побочных эффектов (метотрексат, циклоспорин А, Д-пеницилламин, колхицин). В настоящее время единственным фармакологическим средством, способным обеспечить достижение отчётливого лечебного эффекта, являются — урсодезоксихолевая кислота (УДХК)[2][15][19].
В основном терапия направлена на уменьшение проявления клинических симптомов заболевания. У людей с ПБХ может быть нарушена липидозависимая абсорбция жирорастворимых витаминов (A, D, E, K). Рекомендуется соответствующая добавка витаминов, когда уровень билирубина повышен. Пациенты с ПБХ имеют повышенный риск развития остеопороза по сравнению с общей популяцией и другими пациентами с заболеваниями печени. Скрининг и лечение этого осложнения являются важной частью лечения ПБХ. Как и при всех заболеваниях печени, потребление алкоголя следует ограничить или полностью исключить. У пациентов с прогрессирующим заболеванием печени единственным методом лечения, который может привести к излечению, является трансплантация печени. Результаты лечения благоприятные, при этом пятилетняя выживаемость пациентов после трансплантации печени лучше, чем при большинстве других показаний для пересадки[30][31]
Прогноз
Введение УДХК значительно изменило течение заболевания. Множество клинических испытаний и наблюдательных исследований показали его эффективность на биохимию печени, гистологическое прогрессирование и выживаемость без трансплантации печени. Среди пациентов, получающих лечение УДХК, степень улучшения биохимических показателей печени, то есть ответ на УДХК, помогает определить прогноз на длительный срок. В отсутствие цирроза пациенты, у которых уровень печёночных ферментов снижается до нормальных значений на фоне лечения УДХК, имеют отличный прогноз выживаемости, который может быть сопоставим с общим населением. Однако выживаемость значительно снижается у тех, у кого биохимические показатели печени остаются аномальными при лечении.
Два наиболее важных параметра для оценки ответа на лечение УДХК— это щелочная фосфатаза и общий билирубин. Были разработаны качественные и количественные определения ответа на УДХК, основанные на изменениях уровня билирубина, трансаминаз после 6-24 месяцев лечения УДХК в дозе 13-15 мг/кг/день. Пациентов на момент диагностики можно стратифицировать по риску ответа на УДХК. Это важно для выявления пациентов, которые могут быть кандидатами для вторичной терапии до того, как будет выявлено неэффективное действие УДХК, что может повлиять на течение заболевания.
Гепатоцеллюлярная карцинома встречается редко при ПБХ. Недавние крупномасштабные когортные исследования показали, что отсутствие ответа на УДХК после 12 месяцев терапии и мужской пол связаны с повышенным риском развития ГЦК в дальнейшем у пациентов с ПБХ. После трансплантации печени рецидив заболевания может составлять до 18 % через 5 лет и до 30 % через 10 лет. В настоящее время нет консенсуса по поводу факторов риска рецидива заболевания[31][32][33].
Примечания
Литература
- Энциклопедический словарь медицинских терминов. В 3-х томах / Главный редактор Б. В. Петровский. — Москва: Советская энциклопедия, 1982. — Т. 1. — 1424 с. — 100 000 экз. Архивная копия от 29 августа 2009 на Wayback Machine
- Малая медицинская энциклопедия. — под ред. В. И. Покровского. — М.: Советская энциклопедия, 1991. — Т. 1. — 577 с. — ISBN 5-85270-040-1. Архивная копия от 6 декабря 2009 на Wayback Machine.
- Заболевания печени и жёлчных путей — Ш. Шерлок, Дж. Дули; ред.: З. Г. Апросина, Н. А. Мухин. — М. : ГЭОТАР-Медицина, 1999. — 860 с. : ил.. — ISBN 5-88816-013-X
- Внутренние болезни. Система органов пищеварения: учеб. пособие / Г. Е. Ройтберг, А. В. Струтынский. — 5-е изд., перераб. и доп. — М. : МЕДпресс-информ, 2018. — 576 с. : ил. ISBN 978-5-00030-523-2
- Майер К.-П. Гепатит и последствия гепатита: Пер. с нем. М.; 1999: 273—93.