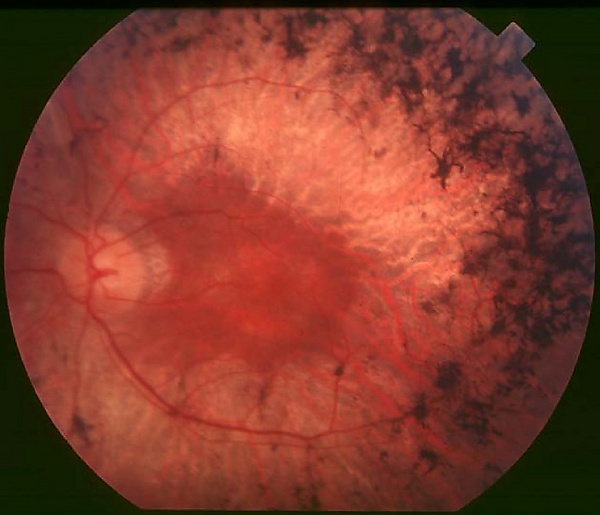
Пигментный ретинит
Пигме́нтный ретини́т (ПР, пигме́нтная абиотрофи́я сетча́тки; англ. retinitis pigmentosa[1]) — прогрессирующая наследственная дегенерация сетчатки, характеризующаяся гибелью фоторецепторов и отложением пигмента в сетчатке[2]. Болезнь проявляется низким зрением по ночам, медленной адаптацией к темноте, ограничением периферического зрения. В зависимости от типа мутации острота зрения сохраняется на уровне 0,7 или падает ниже 0,1. Для лечения применяют витамин А, лютеин, воретиген непарвовец-рзил, ретинальные имплантаты. Рекомендовано ношение солнцезащитных очков[3].
Общие сведения
История
В 1991 году компания «Second Sight» начала разработку ретинального имплантата[4], первая версия которого (Argus I) была выпущена в 2002 году и протестирована на шести пациентах[5]. В 2006 году создан Argus II, который был одобрен FDA[6], а в 2017 имплантирован российскому пациенту[7]. Позднее производство было прекращено, а компания сосредоточилась на разработке нового имплантата — Orion, электроды которого помещают в зрительную кору головного мозга[3].
В 2006 году исследователи из Великобритании пересаживали стволовые клетки мышам с продвинутой стадией ПР и программировали развитие фоторецепторов. Эти фоторецепторы развились и приобрели необходимые нервные связи в сетчатке[8].
В 2008 году учёные Биологического научного института Осаки выявили белок пикачурин, который, по их мнению, мог помочь в разработке лекарства[9][10].
В 2010 году в исследовании на мышах получены обнадёживающие результаты генной терапии ПР[11]. В этом же году японская компания R-Tech Ueno завершила вторую фазу клинических исследований офтальмологического раствора UF-021 для лечения ПР.
В 2012 году учёные из Медицинского центра Колумбийского университета показали на животной модели, что генная терапия и терапия индуцированных плюрипотентных стволовых клеток могут быть перспективными вариантами лечения[12].
В 2012 году учёные из Института глаза Баском Палмер показали на животной модели, что введение в глазное яблоко мезэнцефалических астроцитов нейротрофического фактора защищают фоторецепторы[13].
В 2014 году учёные из Университета Аликанте показали, что каннабиноиды могут замедлить потерю зрения в случаях ПР[14].
Исследователи из Университета Беркли, Калифорния, смогли восстановить зрение слепым мышам, эксплуатируя «photoswitch», который активизирует ганглиозные клетки сетчатки в образце с повреждёнными палочками и колбочками[15].
В 2017 году FDA одобрила имплантацию бионического глаза Argus II.
В 2020 году в обзоре научной литературы, посвящённом различным методам электростимуляции в офтальмологии, сделан предварительный вывод о «возможной эффективности» (рекомендация уровня B) транскорнеальной электростимуляции при пигментном ретините[16].
- Деррик Морган, ямайский ска, рокстеди и регги — музыкант.
- Нил Fachie, британский паралимпийский велосипедист[17].
- Линди Хоу, австралийский тандем-велосипедист и пловец[18].
- Джон Уэллнер, американский актёр[19].
- Стив Уинн, американский бизнес-магнат и разработчик казино в Лас-Вегасе[20].
- Рэйчел Leahcar, австралийская певица.
- Вилли Браун, бывший мэр Сан-Франциско.
- Стив Лонеган, мэр Боготы, Нью-Джерси, Республиканский кандидат в Сенат США.
- Аманда Своффорд, американская модель[21].
- Ричард Бернштейн, судья Верховного суда, Мичиган.
- Ян Трехерн, британский фотограф.
- Мэтью Бентон, суперзвезда кабаре и владелец / управляющий директор / художественный руководитель танцоров Мэтью Бентон.
- Молли Бёрк, мотивационный спикер, блогер.
Классификация
По связи с другими заболеваниями выделяют:
- несиндромальный ПР — развивается изолированно;
- синдромальный ПР — сочетается с нейросенсорными расстройствами или аномалиями развития:
- синдромом Ушера,
- синдром Барде — Бидля,
- синдром Кернса — Сейра,
- болезнь Рефсума,
- абеталипопротеинемия[22];
- вторичный ПР — сочетается с системными заболеваниями[23].
| OMIM | Ген | Тип |
|---|---|---|
| 180100 | RP1 | Пигментный ретинит-1 |
| 312600 | RP2 | Пигментный ретинит-2 |
| 300029 | RPGR | Пигментный ретинит-3 |
| 608133 | PRPH2 | Пигментный ретинит-7 |
| 180104 | RP9 | Пигментный ретинит-9 |
| 180105 | IMPDH1 | Пигментный ретинит-10 |
| 600138 | PRPF31 | Пигментный ретинит-11 |
| 600105 | CRB1 | Пигментный ретинит-12, аутосомно-рецессивный |
| 600059 | PRPF8 | Пигментный ретинит-13 |
| 600132 | TULP1 | Пигментный ретинит-14 |
| 600852 | CA4 | Пигментный ретинит-17 |
| 601414 | HPRPF3 | Пигментный ретинит-18 |
| 601718 | ABCA4 | Пигментный ретинит-19 |
| 602772 | EYS | Пигментный ретинит-25 |
| 608380 | CERKL | Пигментный ретинит-26 |
| 607921 | FSCN2 | Пигментный ретинит-30 |
| 609923 | TOPORS | Пигментный ретинит-31 |
| 610359 | SNRNP200 | Пигментный ретинит 33 |
| 610282 | SEMA4A | Пигментный ретинит-35 |
| 610599 | PRCD | Пигментный ретинит-36 |
| 611131 | NR2E3 | Пигментный ретинит-37 |
| 268000 | MERTK | Пигментный ретинит-38 |
| 268000 | USH2A | Пигментный ретинит-39 |
| 612095 | PROM1 | Пигментный ретинит-41 |
| 612943 | KLHL7 | Пигментный ретинит-42 |
| 268000 | CNGB1 | Пигментный ретинит-45 |
| 613194 | BEST1 | Пигментный ретинит-50 |
| 613464 | TTC8 | Пигментный ретинит-51 |
| 613428 | C2orf71 | Пигментный ретинит-54 |
| 613575 | ARL6 | Пигментный ретинит-55 |
| 613617 | ZNF513 | Пигментный ретинит-58 |
| 613861 | DHDDS | Пигментный ретинит-59 |
| 613194 | BEST1 | Пигментный ретинит, концентрический |
| 608133 | PRPH2 | Пигментный ретинит, дигенический |
| 613341 | LRAT | Пигментный ретинит, ювенильный |
| 268000 | SPATA7 | Пигментный ретинит, ювенильный, аутосомно-рецессивный |
| 268000 | CRX | Пигментный ретинит, запоздалый доминирующий |
| 300455 | RPGR | Пигментный ретинит, X-хромосомный, с синореспираторной инфекцией, с глухотой или без неё |
Этиология
Обнаружено более 100 мутаций, ответственных за развитие ПР. Большинство из них — миссенс-мутации с аутосомно-доминантным типом наследования[24].
Ген родопсина кодирует главный белок наружных сегментов фоторецепторов. Исследования показывают, что мутации в этом гене ответственны примерно за 25 % аутосомно-доминантных форм ПР[25][26].
Мутации в пре-мРНК факторах сплайсинга (PRPF3, PRPF4, PRPF31, PRPF8 и SNRNP200) провоцируют сплайсосомопатии, ведущие к ПР. Такие мутации вызывают нарушения в работе U4/U6-комплекса сплайсосом либо U5-комплекса (PRPF8).
Более 150 мутаций Pro23His встречаются по всему домену гена опсина и распределяются по трём областям белка (внутридисковому, трансмембранному и цитоплазматическому доменам). Одной из основных биохимических причин ПР в случае мутаций белка родопсина являются фолдинг белка и молекулярные шапероны[27]. На мутацию кодона 23 в гене родопсина приходится наибольшая доля мутаций в Соединённых Штатах. Ряд исследований сообщили о других мутациях, коррелирующих с ПР: Thr58Arg, Pro347Leu, Pro347Ser и удаление Ile-255[26][28][29][30][31]. В 2000 году сообщалось о редкой мутации в кодоне 23, вызывающей аутосомно-доминантный ПР, в которой пролин изменялся на аланин[32].
Патогенез
Патогенез у человека не изучен. Опыты на животных показывают, что у крыс пигментный эпителий фагоцитирует отслоившиеся диски внешних сегментов погибших палочек, а обломки внешних сегментов накапливаются. У мышей с гомозиготной рецессивной мутацией палочки прекращают развитие и подвергаются дегенерации до завершения созревания клеток. У мышей и собак обнаружен дефект цГМФ-фосфодиэстеразы, который способствует повышению концентрации цГМФ до токсической[3].
Эпидемиология
На РП приходится около 50 % случаев наследственных болезней сетчатки. Распространённость несиндромного РП в мире около 1 случая на 5000 человек: в Дании — 1:3026, Бирмингеме 1:4869, в Индии — 1:372. Мужчины болеют немного чаще, чем женщины, поскольку Х-сцепленная форма чаще проявляется у мужчин. Распространённость синдромного РП от 4 до 17 случаев на 100 000 человек. Аутосомно-рецессивные формы проявляются в раннем подростковом возрасте, аутосомно-доминантные после 20 лет. Более 75 % больных обращаются за медицинской помощью после 30 лет[33].
Диагностика
Больные жалуются на низкое зрение по ночам, медленную адаптацию к темноте, ограничение периферического зрения, вспышки, головные боли. Острота зрения обоих глаз постепенно снижается до 0,1 или хуже у 25 % больных. Однако больше половины больных сохраняют остроту зрения 0,5 или лучше хотя бы на одном глазу. Только 0,5 % пациентов слепнут на оба глаза[3]. ПР может сочетаться с катарактой, глаукомой, миопией, кератоконусом, болезнью Коатса, друзами диска зрительного нерва[22].
Молекулярно-генетическое тестирование[33].
- Визометрия. Острота зрения снижена.
- Офтальмоскопия. На глазном дне видны отложения пигмента в виде костных телец с депигментацией или атрофией пигментного эпителия вокруг отложений, диск зрительного нерва бледный, артерии сужены.
- Периметрия. Определяется концентрическое сужение поля зрения.
- Электроретинография. На ранних стадиях снижается амплитуд a- и b-волн.
- Темновая адаптометрия. Исследование полезно для выявления ранних стадий — абсолютный порог палочек повышен, а темновая адаптация замедлена.
- Исследование цветовосприятия. Восприятие цвета нарушено.
- Оптическая когерентная томография. Метод используют для диагностики осложнений ПР[34].
Дифференциальная диагностика
Болезни, от которых необходимо дифференцировать ПР:
- болезнь Беста;
- центральная серозная хориоретинопатия;
- хлорохиновая ретинопатия;
- хроническая прогрессирующая наружная офтальмоплегия;
- ювенильный ретиношизис;
- возрастная макулярная дегенерация[35];
- атрофия гирате;
- амавроз Лебера;
- хороидеремия;
- односторонний подострый нейроретинит;
- сифилитический ретинит;
- краснушная ретинопатия[3].
Осложнения
Могут развиваться:
- кистозный макулярный отёк;
- эпиретинальная мембрана;
- витреомакулярный тракционный синдром[3];
- слепота;
- катаракта;
- хориоидальная неоваскуляризация;
- пролиферативная витреоретинопатия[33].
Лечение
Ношение солнцезащитных очков помогает замедлить прогрессирование ПР[3].
Назначают пероральный приём лютеина и высоких доз витамина A, однако их эффективность остаётся спорной[33].
Для лечения больных с мутацией гена RPE65 одобрена витрэктомия с инъекцией генетического препарата воретиген непарвовец-рзил в субретинальное пространство[36].
Исследуется лечение с помощью ретинальных имплантатов Orion[3].
Прогноз
Лучший прогноз у больных аутосомно-доминантным РП — у большинства пациентов до 30 лет острота зрения сохраняется на уровне 0,7 или выше. Худший прогноз у больных Х-сцепленным ПР — к 50 годам острота зрения снижается до 0,1 и ниже[3].
Диспансерное наблюдение
Больных наблюдает офтальмолог 1 раз в год[35].
Профилактика
Генетическое консультирование при планировании беременности[33].
Примечания
Литература
- Ryan’s Retina / Schachat A. P. — 7th edition. — China: Elsevier, 2018. — ISBN 978-0-323-40197-5.
- Kanski’s Synopsis of Clinical Ophthalmology / Salmon J. F. — 4th edition. — Elsevier, 2023. — ISBN 978-0-7020-8374-7.