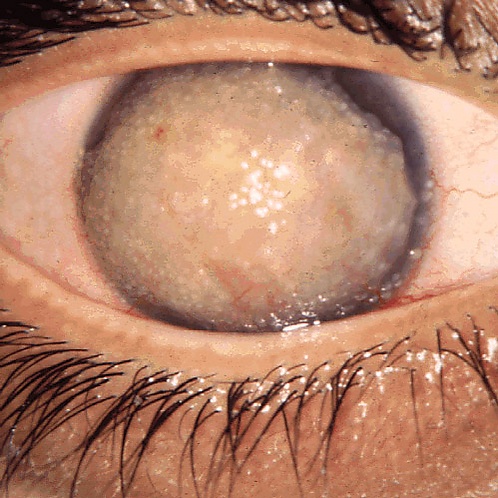
Дистрофии роговицы
Дистрофи́и рогови́цы — группа наследственных, обычно двусторонних и медленно прогрессирующих заболеваний роговицы, которые традиционно рассматриваются как состояния, не связанные с факторами окружающей среды или системными болезнями. Международный комитет по классификации дистрофий роговицы традиционно относит к этой группе дистрофию базальной мембраны эпителия и центральную облаковидную дистрофию Франсуа, признавая, что патогенетически это дегенеративные процессы[1]. Болезни обусловлены мутациями в генах, кодирующих синтез белков-переносчиков, ферментов или структурных белков, участвующих в метаболизме роговицы[2][3]. Могут протекать бессимптомно. Симптомные случаи проявляются болью в глазах, светобоязнью, ощущением инородного тела в глазу, ухудшением зрения[4]. Медикаментозное лечение симптоматическое — направлено на купирование боли и дискомфорта. При выраженных помутнениях и болях выполняют фототерапевтическую кератэктомию или кератопластику. Прогноз зависит от типа дистрофии[5].
Общие сведения
История
В 1889 году О. Хааб и Ф. Диммер впервые описали болезнь, сегодня известную как решётчатая дистрофия роговицы 1 типа[6]. В 1890 году термин «дистрофия роговицы» впервые употребил немецкий офтальмолог Артур Греноу для описания гранулярной дистрофии, позже швейцарский офтальмолог Хьюго Бибер описал решётчатую дистрофию. В 1910 году австрийский офтальмолог Эрнст Фукс опубликовал описание 13 случаев помутнения центральной части роговицы с образованием булл и назвал это состояние «эпителиальной дистрофией»[2]. В 1917 году A. Греноу указал на наследственный характер болезней. В 1938 году М. Баклерс опубликовал первую генетическую классификацию. О картировании первого гена, отвечающего за развитие зернистой дистрофии роговицы 1 типа, сообщили Х. Эйберг и соавт. в 1993 году[6]. В 2005 году был создан Международный комитет по классификации дистрофии роговицы (англ. International Committee for Classification of Corneal Dystrophies), сформировавший новую классификацию на основании данных генетики и гистопатологии. Классификация обновлялась в 2015 и 2024 годах[1].
Классификация
- Эпителиальные и субэпителиальные дистрофии:
- дистрофия базальной мембраны эпителия (категория [К] 3);
- рецидивирующие эрозионные дистрофии эпителия:
- рецидивирующая эрозионная дистрофия эпителия (К1);
- дистрофия роговицы Франческетти (К4);
- дистрофия Смоландиенсис (К4);
- дистрофия Хельсингландика (К4);
- субэпителиальная муцинозная дистрофия роговицы (К4);
- дистрофия роговицы Меесманна (К1);
- эпителиальная дистрофия роговицы Лиша (К1);
- желатинозная каплевидная дистрофия роговицы (К1).
- Эпителиально-стромальные дистрофии TGFBI:
- дистрофия роговицы Рейса — Бюклерса (К1);
- дистрофия роговицы Тиля — Бенке (К1);
- решётчатые дистрофии роговицы:
- классическая решётчатая дистрофия роговицы (К1);
- варианты классической решётчатой дистрофии роговицы (К1);
- гранулярная дистрофия роговицы, тип 1 (К1);
- гранулярная дистрофия роговицы, тип 2 (К1).
- Стромальные дистрофии:
- пятнистая дистрофия роговицы (К1);
- дистрофия роговицы Шнайдера (К1);
- врождённая стромальная дистрофия роговицы (К1);
- задняя аморфная дистрофия роговицы (К1);
- центральная облаковидная дистрофия Франсуа (К4)
- предесцеметовые дистрофии роговицы:
- предесцеметовая дистрофия роговицы (К4);
- точечная и полихроматическая предесцеметовая дистрофия роговицы (К1).
- Эндотелиальные дистрофии:
- эндотелиальная дистрофия роговицы Фукса (К1, К2 или К3);
- задняя полиморфная дистрофия роговицы [тип 1, тип 2, тип 3] (К1);
- врождённая наследственная эндотелиальная дистрофия (К1 или К3);
- Х-сцепленная эндотелиальная дистрофия роговицы (К2);
- Удалённые дистрофии:
- дистрофия роговицы Грейсона — Вильбрандта (К4)[1].
- Чётко определённая дистрофия, ген картирован и идентифицирован, специфические мутации известны.
- Чётко определённая дистрофия, картированная на один или несколько специфических хромосомных локусов, но ген(ы) не идентифицированы.
- Чётко определённая дистрофия, не картированная на хромосомном локусе.
- Предполагаемая, новая или ранее задокументированная дистрофия; нозологическая самостоятельность не доказана[1].
Этиология
Патогенез
Общий механизм связан с нарушением метаболизма роговицы из-за нарушения синтеза белков-переносчиков, ферментов или структурных белков. Мутации в гене TGFBI нарушают образование фибриллярных белков и их взаимодействие с коллагеном, ламинином и фибронектином, поддержание гомеостаза внеклеточного матрикса. В результате мутации в генах KRT3 и KRT12 (дистрофия Месманна) нарушается синтез кератина 3 и кератина 12. Мутация UBIAD1 (дистрофия Шнайдера) приводит к нарушению метаболизма витамина К и кофермента Q[2].
Эпидемиология
Большинство дистрофий роговицы наследуются по аутосомно-доминантному типу, некоторые — по аутосомно-рецессивному[3]. Наследование эпителиальной дистрофии Лиша и Х-сцепленной эндотелиальной дистрофии сцеплено с Х-хромосомой[2]. Истинная распространённость неизвестна из-за бессимптомного течения многих случаев[3]. В Соединённых Штатах Америки распространённость всех дистрофий роговицы оценивают менее чем в 0,01 %; эндотелиальных дистрофий — в 530 случаев на 1 млн человек; гранулярной, макулярной или решётчатой дистрофий — в 5—10 случаев на 1 млн человек. Самая распространённая — эндотелиальная дистрофия Фукса — в 2012 году 39 % трансплантаций роговицы в мире проведены больным этой дистрофией. Дистрофия Фукса чаще встречается у людей европеоидной расы[4] и в 4 раза чаще у женщин, чем у мужчин[3], хотя в среднем мужчины и женщины болеют дистрофиями роговицы одинаково часто. Гранулярная дистрофия роговицы 2 типа шире распространена в Европе, желатинозная каплевидная дистрофия — в Японии, дистрофия Месманна — в Германии и Дании, а решётчатая дистрофия 2 типа — в Финляндии[4].
Диагностика
Дистрофии роговицы долго протекают бессимптомно и медленно прогрессируют. Симптомы появляются вместе с видимыми изменениями роговицы, которые обычно двусторонние, симметричные и медленно прогрессируют. Некоторые дистрофии при рождении (например, пятнистая, врождённая стромальная и врождённая наследственная эндотелиальная дистрофии), другие в 10—30 лет (например, дистрофия Фукса и решётчатая дистрофия 2 типа)[4]. Больные начинают жаловаться на боль в глазах, светобоязнь, ощущение инородного тела в глазу, ухудшение зрения[4].
- Молекулярно-генетическое исследование позволяет точно определить вид дистрофии.
- Гистологическое исследование и электронную микроскопию роговицы используют в клинических исследованиях для диагностики удалённых в ходе кератопластики роговиц[2][4].
Выполняют:
- визометрию — при некоторых дистрофиях острота зрения снижается на поздних стадиях;
- офтальмотонометрию — внутриглазное давление оценивают, чтобы исключить глаукому;
- биомикроскопию за щелевой лампой с окрашиванием роговицы — выявляют изменения, характерные для той или иной дистрофии (помутнения поверхностных или глубоких слоёв, буллы, потерю эпителия или эндотелия);
- офтальмоскопию — необходима для исключения болезней хрусталика и сетчатки;
- оптическая когерентная томография роговицы — помогает оценить локализацию дистрофии[2][4].
Дифференциальная диагностика
Состояния, от которых необходимо дифференцировать:
- кератоконус;
- буллёзная кератопатия[3];
- дегенерации роговицы[1].
Лечение
Некоторые дистрофии не требуют лечения (например, предесцеметовые, гранулярная 2 типа, задняя полиморфная)[5]. Больным с дискомфортом в глазах назначают увлажняющие капли или гели, при болях на фоне повреждения эпителия — бандажные контактные линзы[4].
Эффективного медикаментозного лечения нет. Больным с эпителиальными дистрофиями при отёке роговицы и буллах назначают глазные капли гипертонических растворов натрия хлорида или декстрозы, нестероидные противовоспалительные препараты[4].
При сильных болях и помутнении роговицы выполняют фототерапевтическую кератэктомию или кератопластику[5].
Учёные разрабатывают методы генной терапии на основе кластерных регулярно расположенных коротких палиндромных повторов[7].
Прогноз
Прогноз различный: одни дистрофии не влияют на зрение (например, дистрофии Меесманна, гранулярная дистрофия 2 типа), другие успешно лечатся хирургически (например, пятнистая дистрофия и дистрофия Шнайдера), третьи быстро рецидивируют после кератопластики (например, желатинозная дистрофия и дистрофия Рейса — Бюклерса)[5].
Диспансерное наблюдение
Больных наблюдают офтальмологи. Длительность и частоту наблюдения подбирают индивидуально[6].
Профилактика
Не разработана.
Примечания
Литература
- Constantin C. Corneal dystrophies: pathophysiological, genetic, clinical, and therapeutic considerations // romanian journal of ophthalmology. — 2021-06-12. — Т. 65, № 2. — С. 104–108. — ISSN 2501-2533 2457-4325, 2501-2533. — doi:10.22336/rjo.2021.22.
- Titoyan K. H., Kchikmatullin R. I., Usubov E. L., Valishin I. D. Corneal dystrophy: literature review, own clinical observations // Point of view. East – west. — 2023-12-28. — № 4. — С. 39–48. — ISSN 2410-1257. — doi:10.25276/2410-1257-2023-4-39-48.
- Weiss J. S., Rapuano C. J., Seitz B., et al. IC3D Classification of Corneal Dystrophies—Edition 3 (англ.) // Cornea. — 2024-02-12. — Т. 43, № 4. — С. 466–527. — ISSN 0277-3740. — doi:10.1097/ico.0000000000003420.
Ссылки
- Moshirfar M., Bennett P. Corneal Dystrophy. StatPearls. StatPearls (8 июля 2023). Дата обращения: 24 марта 2026.
- National Organization for Rare Disorders. Corneal Dystrophies. National Organization for Rare Disorders. National Organization for Rare Disorders (30 июня 2010). Дата обращения: 24 марта 2026.