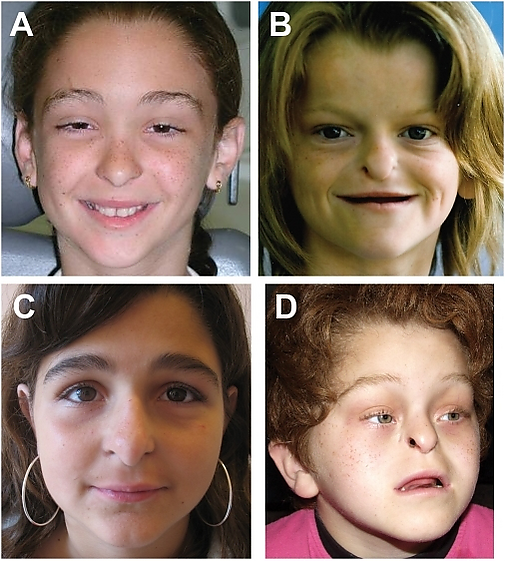
Синдром Йохансона – Близзарда
Синдром Йохансона — Близзарда — это редкое аутосомно-рецессивное заболевание, которое проявляется врождённой недостаточностью экзокринной функции поджелудочной железы и гипоплазией или аплазией крыльев носа. На сегодняшний день в мире зарегистрировано около 100 случаев этого синдрома, а в русскоязычных источниках встречаются лишь единичные описания. Заболевание развивается из-за мутации в гене UBR1, расположенном на длинном плече 15-й хромосомы[1].
Общие сведения
История
Этот синдром относится к редким заболеваниям и впервые был описан Йохансоном и Близзардом в 1971 г. В 2005 году была выявлена мутация в гене UBR1, ответственная за развитие данного синдрома[2].
Этиология
Ген UBR1, расположенный на 15 хромосоме, в настоящее время является единственным известным геном, ассоциированным с синдромом Йохансона — Близзарда. Он кодирует убиквитинлигазу убиквитин-зависимого протеолитического пути. UBR1 играет ключевую роль в развитии и поддержании функции ацинарных клеток поджелудочной железы. Ранее сообщалось, что при данном синдроме происходит внутриутробное разрушение ацинарной ткани с последующим её замещением жировой, а также постепенное развитие эндокринной недостаточности, приводящей к диабету[3].
Патогенез
Белок убиквитин — это универсальный, повсеместно экспрессирующийся белок, характерный для эукариотических организмов. Убиквитин участвует в регуляции других белков, помечая их для последующей деградации протеасомами. Этот процесс начинается, когда убиквитинлигаза ковалентно присоединяет молекулу убиквитина к боковой цепи лизина в целевом белке-субстрате (повреждённом, неправильно свёрнутом или ненужном белке, который требуется разрушить). Эта реакция повторяется несколько раз, формируя цепочку молекул убиквитина — процесс, известный как полиубиквитинирование. Полиубиквитинирование белка служит сигналом для протеасомы разрушить его посредством протеолиза[4][5].
Убиквитин-протеасомная система играет ключевую роль в нелизосомной деградации внутриклеточных белков, а убиквитин также может участвовать в модификации белков для выполнения определённых функций. Как деградация, так и модификация белков являются частью общей регуляторной системы, необходимой для таких клеточных процессов, как деление клеток, передача сигналов, функционирование клеточных рецепторов, апоптоз, поддержание целостности ДНК, воспалительный ответ и контроль его развития, связанный с клеточным циклом и гомеостазом в целом[6][7].
При синдроме Йохансона — Близзарда мутации в гене UBR1 изменяют, нарушают или полностью блокируют синтез убиквитинлигазы. В ацинарных клетках поджелудочной железы UBR1 экспрессируется наиболее интенсивно по сравнению с другими тканями организма. Нарушение работы убиквитин-протеасомной системы, вызванное недостаточной активностью убиквитинлигазы, является причиной как врождённого, так и прогрессирующего воспалительного повреждения, замещения жировой тканью, разрастания соединительной ткани и ошибок в иннервации ацинусов и островков поджелудочной железы. Это связано с нарушением нормального апоптоза повреждённых клеток и аномальным накоплением белков. Аналогичные процессы наблюдаются и в других тканях, зависящих от нормальной экспрессии UBR1, включая черепно-лицевую область, опорно-двигательную и нервную системы, зубы и внутренние органы[8][9].
Эпидемиология
Распространенность ориентировочно составляет 1 на 250 000 новорождённых детей. В настоящее время в мире описано около 100 случаев данного синдрома, в русскоязычной литературе имеются единичные упоминания[2].
Клинические проявления
Клинические проявления и физические признаки синдрома Йохансона — Близзарда могут значительно варьировать у разных пациентов. Важно отметить, что у поражённых лиц могут полностью отсутствовать симптомы. Однако недостаточность поджелудочной железы, аномалии зубов и характерная форма носа встречаются почти у всех поражённых лиц. Тяжесть синдрома также может варьировать, и у некоторых младенцев могут развиться угрожающие жизни осложнения в младенческом возрасте[10].
Младенцы с синдромом Йохансона — Близзарда обычно имеют характерные краниофациальные аномалии при рождении. Наиболее яркой и постоянной чертой является необычно маленький нос «клювовидной» формы из-за отсутствия (аплазии) или недоразвития (гипоплазии) крыльев носа. Кроме того, у некоторых поражённых младенцев может наблюдаться маленькая недоразвитая верхняя челюсть, маленький заострённый подбородок, длинная узкая верхняя губа и микроцефалия. У некоторых младенцев могут отсутствовать слёзные точки или иметься аномальный слёзный проток. В некоторых случаях наблюдались более тяжёлые повреждения лицевого черепа включая расщелину губы или нёба.
Младенцы с синдромом Йохансона — Близзарда могут иметь низкий вес при рождении и общую мышечную гипотонию. Без лечения у младенцев обычно наблюдается задержка роста. В конечном итоге у поражённых лиц может развиться низкорослость. У поражённых младенцев и детей также могут отмечаться задержки развития, хотя в некоторых случаях интеллект остаётся нормальным. Может присутствовать тугоухость или глухота.
Дефицит роста при синдроме может быть связан с мальабсорбцией и экзокринной недостаточностью поджелудочной железы. Панкреатическая недостаточность является распространённым и выраженным признаком данной патологии. В результате возникает дефицит пищеварительных ферментов, что препятствует нормальному всасыванию жиров и других питательных веществ. У лиц с синдромом Йохансона — Близзарда кишечная мальабсорбция приводит к обильному зловонному стулу с избытком жира. Кроме задержки роста, панкреатическая недостаточность может вызывать дефицит витаминов, хроническую анемию, гипокальциемию и другие нарушения питания. Например, у поражённых младенцев наблюдается потеря белка, приводящая к отёкам.
У ряда пациентов может развиться эндокринная недостаточность поджелудочной железы. Недостаточная выработка инсулина приводит к диабету. У многих младенцев с данным синдромом также имеются характерные аномалии волос и кожи головы. Волосы часто бывают редкими, сухими и светлыми. Может наблюдаться отсутствие кожи на родничках. В дальнейшем могут развиться участки облысения.
У большинства поражённых младенцев и детей также имеются характерные аномалии зубов. Молочные зубы могут быть аномально маленькими, конусовидными и редкими, с короткими деформированными корнями. Большинство постоянных зубов отсутствуют. Появившиеся зубы также могут быть аномально маленькими с деформированными корнями.
Примерно у 40 % поражённых лиц наблюдается гипотиреоз. Симптомы гипотиреоза обычно проявляются в детском возрасте и могут способствовать задержке роста и психомоторного развития. У некоторых младенцев и детей с синдромом Йохансона — Близзарда могут быть дополнительные аномалии, включая атрезию ануса или анальный стеноз. Могут наблюдаться аномалии мочеполовой системы. У мужчин это может включать гипоспадию и микропенис. У женщин могут быть удвоение влагалища, клиторомегалия и другие аномалии. Также может наблюдаться гидронефроз.
У младенцев и детей с синдромом Йохансона — Близзарда могут развиться дополнительные признаки, включая недоразвитие сосков, обратное расположение органов, врождённые пороки сердца, гипопитуитаризм и повышенную восприимчивость к инфекциям. Также сообщалось о дефиците гормона роста и ювенильном диабете у данных пациентов[10].
Диагностика
Специфических инструментальных и лабораторных методов диагностики нет. Диагноз может быть предположен на основании характерных симптомов, тщательного клинического обследования и детального изучения анамнеза пациента. Окончательный диагноз подтверждается молекулярно-генетическим тестированием, которое выявляет характерные мутации гена UBR1, вызывающие это заболевание.
Для оценки тяжести состояния каждого пациента могут проводиться дополнительные исследования. Они включают аудиометрические тесты для определения степени потери слуха и компьютерную томографию для оценки масштабов жировой инфильтрации поджелудочной железы. Важно, чтобы все больные дети проходили скрининг на возможные серьёзные осложнения, включая врождённые пороки сердца, гипопитуитаризм, гипотиреоз и развитие ювенильного диабета[10].
Дифференциальная диагностика
Дифференциальная диагностика синдрома проводится со следующими состояниями[11]:
- Муковисцидоз (кистозный фиброз)
- Синдром Швахмана — Даймонда;
- Синдром Пирсона
Лечение
Хотя заболевание не имеет радикального лечения, терапия, направленная на коррекцию отдельных симптомов, часто оказывается успешной. Эффективность и объём лечения определяются индивидуальной тяжестью проявлений у каждого конкретного пациента.
Терапия носит преимущественно симптоматический и поддерживающий характер. Пациенты нуждаются в пожизненной заместительной терапии панкреатическими ферментами для обеспечения нормального всасывания жиров и других питательных веществ. Во многих случаях дополнительно назначают витаминные добавки (жирорастворимые витамины A, D, E, K) для профилактики или коррекции авитаминозов, вызванных мальабсорбцией. Рекомендуется специальная диета с лёгкими для усвоения высокобелковыми добавками (гидролизованные белки) для обеспечения полноценного питания. Хотя такая терапия улучшает усвоение нутриентов и способствует набору веса, большинство пациентов остаются ниже сверстников[10].
При гипотиреозе требуется незамедлительная заместительная терапия тироксином. Особенно критично раннее выявление и лечение гипотиреоза у младенцев. Дозировка гормона требует тщательного контроля и коррекции с учётом возможной мальабсорбции[10].
Некоторые аномалии, ассоциированные с синдромом, поддаются хирургической коррекции. Могут быть выполнены:
- реконструкция недоразвитых или отсутствующих крыльев носа;
- Пластика ануса или наложение колостомы при атрезии или стенозе ануса;
- коррекция урогенитальных аномалий;
- устранение пороков сердца[10].
Стоматологические аномалии корректируются с помощью:
- композитных реставраций;
- зубных протезов;
- других ортопедических методик[10].
При тугоухости показано слухопротезирование[10].
Краниофациальные аномалии и деформации скелета могут корректироваться хирургически с использованием костных трансплантатов и остеотомии[12].
Для пациентов с интеллектуальными нарушениями эффективны программы специального образования, методы психологической коррекции и occupational-терапия, адаптированные как для самого пациента, так и для членов его семьи[13].
Прогноз
Экзокринная недостаточность поджелудочной железы и осложнения тяжёлой белково-энергетической недостаточности (такие как выраженная гипопротеинемия, дефицит витаминов, иммунодефицитные состояния) могут приводить к летальному исходу в младенческом или раннем детском возрасте. Однако при правильном лечении и ведении пациенты, как правило, доживают до взрослого возраста[14].
Примечания
Литература
- Легошина И. Н., Плужник В. И., Запорожченко О. В., Хлюнева Н. М. Синдром Йохансона - Близзарда у новорождённого ребёнка. // Российский педиатрический журнал. — 2022. — № 4.
- Ипатова М. Г., Шумилов П. В., Щиголева Н. Е., Мухина Ю. Г. Редкие наследственные заболевания поджелудочной железы у детей: синдром Швахмана — Даймонда, синдром Йохансона — Близзарда. Разбор клинических случаев // Доктор.Ру. — 2017. — № 12 (141).