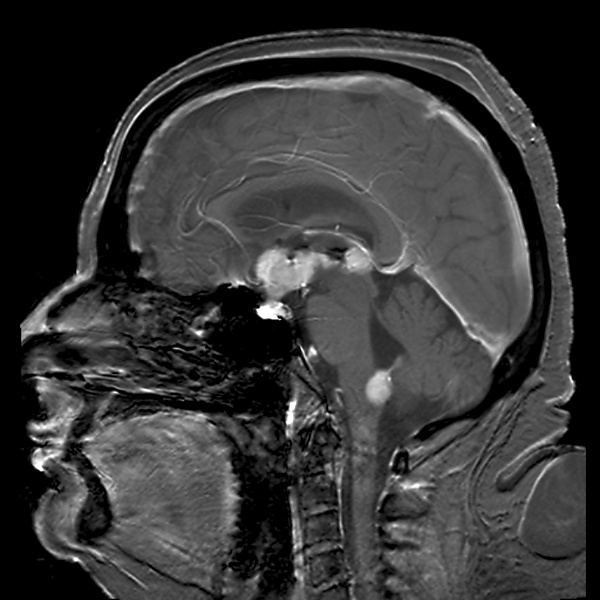
Первичная лимфома центральной нервной системы
Перви́чная лимфо́ма центра́льной не́рвной систе́мы (ПЛЦНС) — редкая агрессивная экстранодальная опухоль, характеризующуюся высокой степенью злокачественности. Заболевание возникает преимущественно у пациентов с иммунодефицитами различного генеза и занимает второе место по частоте встречаемости среди всех экстранодальных лимфом у взрослых. Клиническая картина отличается неспецифичностью и проявляется прогредиентным нарастанием очаговой неврологической симптоматики, когнитивными и поведенческими нарушениями, а также признаками внутричерепной гипертензии, включая головную боль и тошноту. Течение заболевания характеризуется неблагоприятным прогнозом[1][2].
Общие сведения
| Первичная лимфома центральной нервной системы | |
|---|---|
| МКБ-11 | 2A8Z |
| МКБ-10 | C83.3, C85.7 |
| МКБ-10-КМ | C83.3, C83.7, C83.8, C83.9, C85.2, C85.7, C91.8 |
| МКБ-9 | 200.5 |
| DiseasesDB | 29451 |
| MeSH | D008222 |
История
Впервые морфологическое описание ПЛЦНС было выполнено в 1929 году. Позднее, в 1938 году, было представлено более подробное описание опухоли, которую из-за внешнего сходства с новообразованиями лимфатических узлов классифицировали как ретикулярно-клеточную саркому. Вплоть до 1970-х годов в научной литературе эта патология фигурировала под разными названиями, такими как «периваскулярная саркома», «ретикулосаркома» и «микроглиома». Однако понимание уникальной природы заболевания сформировалось лишь в 1974 году после специального доклада, посвящённого данной проблеме. Объектом пристального изучения ПЛЦНС стали с конца 1980-х годов, когда исследователи отметили резкое увеличение числа выявляемых случаев этой патологии[1][3].
Классификация
Выделяют 5 клинических форм ПЛЦНС[1]:
- краниальная форма: характеризуется наличием в головном мозге одного или нескольких объёмных опухолевых образований;
- спинальная форма: встречается крайне редко, подразумевает поражение спинного мозга;
- интраокулярная форма: обусловлена поражением структур глаза, включая сетчатку, стекловидное тело и зрительные нервы;
- первичная дуральная лимфома: опухоль, локализующаяся в твёрдой мозговой оболочке;
- центральный лимфоматоз: форма заболевания с диффузным распространением опухолевых клеток без образования солитарных узлов;
- нейролимфоматоз: характеризуется инфильтрацией периферических и/или черепных нервов злокачественными В-лимфоцитами.
Этиология
Этиология ПЛЦНС до конца не установлена. К числу важнейших факторов риска развития заболевания относится иммунодефицит — как врождённый, так и приобретённый. Помимо иммунодефицитных состояний к предрасполагающим факторам также относятся различные аутоиммунные заболевания (миастения, ревматоидный артрит, системная красная волчанка и саркоидоз), системные васкулиты, например, тромбоцитопеническая пурпура, демиелинизирующие заболевания (прогрессирующая мультифокальная лейкоэнцефалопатия и рассеянный склероз), наличие мультиформной глиобластомы, системные онкологические заболевания, а также инфицирование вирусом гепатита С, вирусами герпеса и состояние после трансплантации органов. Вирус Эпштейна — Барр тесно связан с развитием ПЛЦНС в условиях Т-клеточного иммунодефицита, например у пациентов, получающих иммуносупрессивную терапию после трансплантации органов[1][4].
ПЛЦНС характеризуется соматическими мутациями в гене иммуноглобулинов IGHV4-34. Кроме того, выявляются аберрантные гипермутации в генах, регулирующих клеточный цикл, транскрипцию и апоптоз: BTG2, H1-4, KLHL14, MYD88, CD79B, MYC, PAX5, PIM1, RHOH и SUSD2[5].
Патогенез
В основе развития заболевания лежит сложное сочетание генетических нарушений и изменений в микроокружении опухоли. Ключевую роль играет конститутивная активация сигнальных путей В-клеточного рецептора и ядерного фактора каппа-би, что обеспечивает выживание и пролиферацию злокачественных В-клеток. Наиболее характерными генетическими событиями являются мутации в генах MYD88 (чаще всего L265P) и CD79B, которые часто встречаются одновременно. Важную роль в патогенезе играет микроокружение опухоли, в частности макрофаги и микроглия. Среди них выделяют субпопуляции с противоопухолевой активностью (М1-подобные) и субпопуляции, способствующие росту опухоли (М2-подобные), причём преобладание последних ассоциировано с неблагоприятным прогнозом. М2-подобные макрофаги экспрессируют молекулы иммунных контрольных точек, такие как лиганд запрограммированной клеточной гибели 1. Эндотелиальные клетки и астроциты также вносят вклад в патогенез: эндотелий продуцирует интерлейкин-4 и галектин-3, которые поддерживают выживаемость опухолевых клеток, а астроциты экспрессируют рецептор фактора активации В-клеток, взаимодействуя с опухолевыми клетками. Важной особенностью патогенеза ПЛЦНС является способность опухолевых клеток уклоняться от иммунного надзора, что достигается за счёт потери экспрессии главного комплекса гистосовместимости первого класса вследствие мутаций в генах HLA или в генах B2M[4][5].
Гистологически для опухоли характерен ангиоцентрический рост — скопление крупных атипичных В-клеток вокруг сосудов. В периваскулярном пространстве также обнаруживаются реактивные Т-клетки, формирующие характерный периваскулярный инфильтрат. Формированию такого рисунка способствуют хемокины: эндотелиальные клетки сосудов продуцируют факторы CXCL12 и CXCL9, которые привлекают опухолевые В-клетки (экспрессирующие рецептор CXCR4) и цитотоксические Т-клетки (экспрессирующие CXCR3) соответственно[5].
Эпидемиология
ПЛЦНС составляет около 4 % от всех первичных опухолей центральной нервной системы и от 4 до 6 % всех экстранодальных лимфом. Согласно данным популяционных исследований, распространённость варьирует от 0,3 до 0,6 случая на 100 000 населения. Показатели распространённости существенно различаются в зависимости от возраста: за последние сорок лет наибольший рост заболеваемости отмечен среди пациентов старше 60 лет. В возрастной группе от 70 до 79 лет распространённость достигает 4,32 случая на 100 000 человек. Распространённость заболевания среди ВИЧ-инфицированных в среднем составляет 6,1 %, однако этот показатель значительно варьирует в зависимости от географического региона[5][6].
Диагностика
Клиническая картина ПЛЦНС отличается большим разнообразием и напрямую зависит от локализации и распространённости патологического процесса. Характерные для системных лимфом общие симптомы, такие как лихорадка неясного генеза, ночная потливость и потеря веса, при данной патологии встречаются крайне редко. В зависимости от локализации опухоли к возможным проявлениям ПЛЦНС относятся[5][7]:
- поражение паренхимы головного мозга: заболевание манифестирует с очагового неврологического дефицита: слабость в конечностях, чувствительные нарушения, атаксия, поражение черепных нервов. Наблюдаются нейропсихические и поведенческие изменения: депрессия, апатия, замедление мышления, импульсивное поведение, психотические расстройства. Характерны симптомы внутричерепной гипертензии, включая головную боль, а также судорожный синдром. Локализация опухоли определяет специфику симптомов: изменения личности и двигательные нарушения связаны с поражением лобной доли, афазия — с височной или теменной долей, зрительные расстройства — с затылочной долей, нарушения координации — с мозжечком;
- лимфома мозговых оболочек: характеризуется полинейропатией черепных нервов, корешковыми спинальными симптомами, головной болью, атаксией, энцефалопатией и нарушением функции тазовых органов;
- поражение глаза: проявляется затуманиванием зрения, снижением его остроты и появлением помутнения зрения. Поражение, как правило, двустороннее. Офтальмологическая симптоматика может предшествовать неврологическим проявлениям, возникать одновременно с ними или служить признаком рецидива заболевания;
- спинальная лимфома: клиническая картина представлена подостро развивающейся миелопатией с болями в спине.
При гистологическом исследовании биоптата опухоли выявляются крупные лимфоидные клетки, формирующие солидные поля с характерным периваскулярным ангиоцентрическим рисунком по периферии очага. Опухолевые клетки представлены крупными лимфоцитами с центробластоподобной или иммунобластоподобной морфологией. В ткани опухоли также присутствует небольшое количество реактивных Т-лимфоцитов, макрофагов, активированной микроглии, реактивных астроцитов и неопластических В-клеток[5][7].
Иммуногистохимическое исследование биоптата опухоли: опухолевые клетки экспрессируют В-клеточные маркеры: CD20, CD79a и PAX5. В большинстве случаев определяется иммунофенотип поздних герминальных центров с экспрессией BCL6 и MUM1. Пролиферативная активность опухоли, как правило, очень высокая. Экспрессия CD10 встречается редко. Характерной особенностью является почти исключительная экспрессия иммуноглобулинов M и D, что свидетельствует об отсутствии переключения классов иммуноглобулинов[5].
Клинический анализ ликвора: характерен плеоцитоз, нормальная концентрация глюкозы и повышенная концентрация белка[5].
Позитронно-эмиссионная томография позволяет дифференцировать ПЛЦНС от глиом и инфекционных поражений. ПЛЦНС характеризуются более высоким уровнем метаболической активности по сравнению с глиомами, причём зона патологического накопления радиофармпрепарата на позитронно-эмиссионной томографии часто превышает размеры очага на магнитно-резонансной томографии, что отражает инфильтративный рост опухоли за пределы видимых изменений[4].
Магнитно-резонансная томография головного мозга: на Т2-взвешенных изображениях опухоль выглядит как относительно гипоинтенсивное образование на фоне гиперинтенсивного вазогенного отёка. После введения контрастного вещества на Т1-взвешенных изображениях наблюдается гомогенное диффузное накопление контраста. Характерным признаком является ограничение диффузии, что обусловлено высокой клеточностью опухоли и малым количеством внеклеточной жидкости. На картах измеряемого коэффициента диффузии это проявляется гипоинтенсивностью опухолевой ткани, тогда как зона вазогенного отёка остаётся гиперинтенсивной. При перфузионных исследованиях отмечается умеренное повышение относительного объёма церебральной крови[5].
Дифференциальная диагностика
Дифференциальная диагностика ПЛЦНС проводится со следующими заболеваниями[4]:
- другие первичные или вторичные новообразования центральной нервной системы, такие как глиомы высокой степени злокачественности и метастатические поражения;
- острое нарушение мозгового кровообращения;
- демиелинизирующие заболевания и другие воспалительные поражения;
- токсоплазмоз;
- грибковые абсцессы;
- синдром Толосы — Ханта.
Лечение
Основными направлениями лечения ПЛЦНС у взрослых являются химиотерапия с включением высоких доз антиметаболитов в комбинации с моноклональными антителами к CD20, алкилирующими агентами, ингибиторами ангиогенеза и ингибиторами тирозинкиназ с обязательным интратекальным введением цитостатиков, с последующей консолидацией ремиссии у молодых пациентов высокодозной химиотерапией и аутологичной трансплантацией гемопоэтических стволовых клеток, либо, при невозможности трансплантации, химиотерапией высокими дозами или лучевой терапией на весь головной мозг. В поддерживающей терапии применяются ингибиторы контрольных точек, а для профилактики нейротоксичности при лучевой терапии — нейропротекторы[7].
В ряде случаев — при больших размерах новообразования и развитии угрожающего жизни дислокационного синдрома — может быть оправдана резекция опухоли[1].
Прогноз
Обобщённый прогноз при ПЛЦНС остаётся неблагоприятным, несмотря на чувствительность опухоли к химиолучевой терапии. Применение современных схем лечения позволяет значительно улучшить результаты по сравнению с лучевой терапией в монорежиме. К неблагоприятным факторам прогноза относятся возраст старше 60 лет, низкий функциональный статус пациента (индекс Карновского менее 70 %), наличие множественных внутричерепных очагов, вовлечение в процесс мозговых оболочек, наличие интраокулярной лимфомы, а также повышение концентрации белка в цереброспинальной жидкости[1][4].
ПЛЦНС характеризуется высокой частотой рецидивов, особенно в первые 2 года после завершения лечения. У пожилых и ослабленных пациентов рецидивы нередко возникают раньше, что может быть связано с менее интенсивной терапией на первом этапе. Хотя большинство рецидивов происходит в течение первых 2 лет, описаны случаи поздних рецидивов спустя более 10 лет после постановки диагноза[2].
Диспансерное наблюдение
Пациенты с ПЛЦНС нуждаются в диспансерном наблюдении онколога и невролога. Наблюдение за пациентами включает регулярную магнитно-резонансную томографию головного мозга: каждые 3 месяца в течение первых 2 лет, затем каждые 6 месяцев до 5 лет, а после 5 лет — ежегодно пожизненно в связи с риском отдалённых рецидивов. Повторные исследования цереброспинальной жидкости и магнитно-резонансная томография позвоночника проводятся только у пациентов, у которых исходно было поражение мозговых оболочек или спинного мозга. Пациенты с внутриглазной формой заболевания нуждаются в регулярном офтальмологическом наблюдении[2].
Профилактика
Не разработана.
Примечания
Литература
- Zhang L., Zhang Q. A systematic review of primary central nervous system lymphoma (англ.) // Holistic Integrative Oncology. — 2024. — 11 May (vol. 3). — P. 19. — doi:10.1007/s44178-024-00086-9.
- Ferreri A. J. M., Calimeri T., Cwynarski K., et al. Primary central nervous system lymphoma (англ.) // Nature Reviews Disease Primers. — 2023. — 15 June (vol. 9). — P. 29. — doi:10.1038/s41572-023-00439-0.
- Бублиевский Д., Евзиков Г. Первичная лимфома центральной нервной системы: клиника, диагностика, современные подходы к лечению // Нейрохирургия. — 2012. — Т. 12, № 1. — С. 74—81. — doi:10.17650/1683-3295-2012-12-1-74-81.
- Воинов Н. Е., Улитин А. Ю., Читанава Т. В., и др. Первичные лимфомы центральной нервной системы. Вопросы эпидемиологии и лечения. Клинический пример междисциплинарного подхода в терапии // Трансляционная медицина. — 2022. — Т. 9, № 1. — С. 49—59. — doi:10.18705/2311-4495-2022-9-1-49-59.