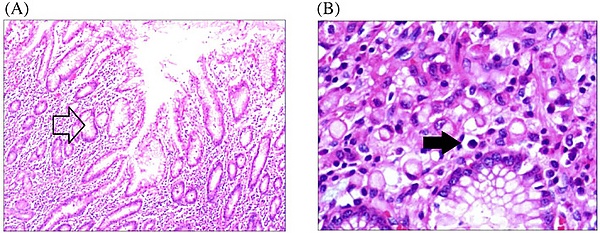
Перстневидноклеточный рак желудка
Перстневиднокле́точный ра́к желу́дка (ПКРЖ) — агрессивный гистологический подтип диффузного типа аденокарциномы желудка, при котором более 50 % клеток, имеющих специфическую «перстневидную» морфологию. При этом типе рака желудка клетки выделяют большое количество слизи, которая накапливается в цитоплазме, оттесняя ядро к периферии, что придаёт клетке сходство с перстнем. Для ПКРЖ типичны низкая дифференцировка, высокая степень злокачественности, выраженная инвазивность, повышенный риск метастазирования и слабый ответ на стандартные методы радио- и химиотерапии[1].
Общие сведения
История
ПКРЖ изначально был относён к «неклассифицированному» типу рака желудка. В 1990 году Всемирная организация здравоохранения в своей классификации выделила аденокарциному из перстневидных клеток в отдельный специфический тип рака желудка. Согласно этой классификации, ПКРЖ был описан как карцинома со слабой когезией, состоящая преимущественно из опухолевых клеток с преобладанием цитоплазматического муцина и причудливо расположенным серповидным ядром[2].
Классификация
ПКРЖ является гистологическим подтипом рака желудка[3].
| Классификация TNM[4] | |
| Т — характеристика первичной опухоли, то есть максимальная глубина инвазии опухоли в стенку желудка | |
| Тх | Первичная опухоль не может быть оценена |
| Т0 | Данных о наличии первичной опухоли не выявлено |
| Tis | Карцинома in situ (опухоль в пределах слизистой оболочки без инвазии собственной пластинки) / тяжёлая дисплазия |
| T1 | Опухоль захватывает собственную пластинку или мышечную пластинку слизистой оболочки, подслизистый слой |
| Т1а | Опухоль захватывает собственную пластинку или мышечную пластинку слизистой оболочки |
| Т1b | Опухоль захватывает подслизистый слой |
| T2 | Опухоль захватывает мышечный слой |
| T3 | Опухоль захватывает субсерозную оболочку без инвазии в висцеральную брюшину или прилежащие структуры; к опухолям этой группы относятся также опухоли с инвазией желудочно-ободочной и желудочно-печёночной связки, большого и малого сальников без поражения висцеральной брюшины, покрывающей эти структуры; при наличии опухолевой перфорации брюшины, покрывающей связки желудка или сальник, опухоль классифицируется как T4 |
| T4 | Опухоль распространяется на серозную оболочку (висцеральная брюшина) или соседние структуры (интрамуральное распространение опухоли на 12-перстную кишку или пищевод не считается распространением на соседние структуры, но используются для характеристики «T» в случае максимальной глубины инвазии в любой из этих областей) |
| Т4а | Опухоль распространяется на серозную оболочку (висцеральная брюшина) |
| Т4b | Опухоль распространяется на соседние структуры, такие как селезёнка, поперечная ободочная кишка, печень, диафрагма, поджелудочная железа, передняя брюшная стенка, надпочечник, почка, тонкая кишка, забрюшинное пространство |
| N — характеристика состояния регионарных лимфатических узлов (для точной оценки pN необходимо иссечение и исследование не менее 16 лимфоузлов) | |
| Nx | Регионарные лимфатические узлы не могут быть оценены |
| N0 | Нет метастазов в регионарных лимфатических узлах |
| N1 | Поражение 1—2 регионарных лимфатических узлов |
| N2 | Поражение 3—6 регионарных лимфатических узлов |
| N3 | Поражение 7 и более регионарных лимфатических узлов:
|
| M — характеристика отдалённых метастазов | |
| Mx | Наличие отдалённых метастазов установить невозможно |
| M0 | Отдалённые метастазы отсутствуют |
| M1 | Наличие отдалённых метастазов или наличие опухолевых клеток в смывах/биоптатах с брюшины |
Этиология
Развитие ПКРЖ является полиэтиологичным процессом, в котором участвует совокупность наследственных, инфекционных, диетических факторов и фоновых патологий желудка. Наследственная предрасположенность играет существенную роль и реализуется через ряд синдромов. Наиболее значим наследственный диффузный рак желудка, который представляет собой аутосомно-доминантное заболевание, обусловленное мутациями в гене CDH1. Этот ген кодирует белок Е-кадгерин, критически важный для клеточной адгезии. Данный синдром приводит к развитию перстневидно-клеточного рака в 30—50 % случаев, характеризуется высоким кумулятивным пожизненным риском (до 83 %) и ранним средним возрастом манифестации (около 37 лет). Другие наследственные синдромы, ассоциированные с повышенным риском ПКРЖ, включают синдром Линча, синдром ювенильного полипоза, синдром Пейтца — Егерса и семейный аденоматозный полипоз, при которых риск колеблется от 1 до 29 %[2][4].
Ключевым внешним фактором является хроническая инфекция, вызванная бактерией Helicobacter pylori, которая инициирует каскад изменений слизистой оболочки. Вредные привычки, в первую очередь курение, также вносят значительный вклад в канцерогенез. Алиментарные факторы риска включают злоупотребление алкоголем, а также частое потребление солёной, жареной, консервированной, маринованной и острой пищи. Опасность представляют и продукты, загрязнённые микотоксинами, наряду с диетой, бедной микроэлементами и витаминами[4].
Развитию ПКРЖ часто предшествуют фоновые заболевания желудка. К ним относятся хронический атрофический и гиперпластический гастрит, аденоматозные полипы, пернициозная анемия, состояние после резекции желудка, а также болезнь Менетрие. Эти состояния создают среду, способствующую дисплазии и злокачественной трансформации эпителиальных клеток[4].
Патогенез
Патогенез ПКРЖ формируется на основе уникального и характерного набора молекулярно-генетических нарушений. Эти нарушения конвергируют на ключевых клеточных процессах, в первую очередь на механизмах межклеточного взаимодействия и контроле роста, что в итоге определяет его агрессивный фенотип с ранней инвазией и метастазированием[2].
Центральным драйвером заболевания является инактивация гена CDH1, расположенного на хромосоме 16q22.1. Этот ген кодирует трансмембранный гликопротеин Е-кадгерин — основной белок адгезивных контактов, обеспечивающий физическое сцепление эпителиальных клеток и поддержание полярности ткани. Потеря его функции вследствие мутаций (включая точковые мутации, делеции и нарушения в сайтах сплайсинга) приводит к критическому нарушению межклеточной адгезии. Это событие является фундаментальным для формирования определяющего гистологического признака ПКРЖ — фенотипа слабой когезии, когда опухолевые клетки теряют связь друг с другом и приобретают способность к диффузной инфильтрации стенки желудка[2].
Прогрессирование опухолевого процесса поддерживается комплексом дополнительных генетических изменений. Частыми событиями выступают инактивирующие мутации в гене-супрессоре опухолей TP53, ведущие к неконтролируемому клеточному делению и геномной нестабильности, а также активирующие мутации в гене PIK3CA, что гиперстимулирует пролиферативный PI3K/AKT/mTOR сигнальный путь. Важную роль играют амплификации онкогенов, таких как CCNE1 (циклин E1) и MYC, которые дополнительно ускоряют клеточный цикл и рост опухоли[2].
Отличительной геномной чертой ПКРЖ является специфическая хромосомная перестройка — химерная транслокация CLDN18-ARHGAP26/6. Образующийся в результате химерный белок объединяет внеклеточный домен белка плотных контактов клаудина-18 с внутриклеточной ГТФазоактивирующей частью белка ARHGAP. Эта аномалия напрямую нарушает Rho-опосредованную регуляцию актинового цитоскелета и окончательно дестабилизирует клеточную адгезию и морфологию, усиливая инвазивный потенциал[2].
Гистологически ПКРЖ характеризуется уникальными морфологическими признаками, которые позволяют отличить его от других типов аденокарцином. Основной диагностический критерий — наличие характерных перстневидных клеток, составляющих более 50 % опухолевой массы. Эти клетки имеют округлую или овальную форму и увеличенный размер, их диаметр может в 1—2 раза превышать диаметр окружающих нормальных столбчатых эпителиоцитов. Патогномоничный признак — массивное накопление внутриклеточного муцина в цитоплазме, которое смещает ядро к периферии, придавая ему форму полумесяца или перстня. Цитоплазма при окраске гематоксилином и эозином часто выглядит светлой, вакуолизированной, с розоватым оттенком муцина. Помимо типичных зрелых форм, в опухоли наблюдаются различные цитологические варианты перстневидных клеток. К ним относятся незрелые клетки с сильно эозинофильной цитоплазмой и ядром, занимающим значительную часть клетки; высокопролиферативные клетки с крупными ядрами и выраженными ядрышками; клетки с оптически пустыми вакуолями и дегенеративные формы с очень большим размером, капсулой и пикнотичными или отсутствующими ядрами[5].
Опухоль обычно развивается из слизистых желёз в верхней части шейки желудочных ямок, где отмечается увеличение муцинпродуцирующих клеток. В процессе трансформации одиночные или множественные перстневидные клетки, происходящие из столбчатого эпителия, первоначально появляются среди клеток слизистой шейки, а затем мигрируют за пределы желёз в строму, где начинают независимую моноклональную пролиферацию[5].
Рост опухоли часто носит инфильтративный характер, с поперечным распространением в пределах слизистой оболочки. Макроскопически это может проявляться в виде эрозий, небольших язв или локальных вдавлений слизистой оболочки из-за её истончения. В строме обычно присутствует воспалительный инфильтрат, состоящий из лимфоцитов, плазматических клеток и нейтрофилов, могут формироваться лимфоидные фолликулы. Пролиферация фиброзной соединительной ткани, а также явления кишечной метаплазии для данного типа рака желудка не характерны[5].
Эпидемиология
В структуре заболеваемости в Российской Федерации рак желудка занимает 5-е место, а в структуре смертности от злокачественных опухолей — 3-е место. ПКРЖ — это второй по частоте встречаемости гистологический тип аденокарциномы желудка, на который приходится от 20 до 54 % всех случаев. Общая расчётная годовая заболеваемость составляет приблизительно 6,22 случая на 100 000 населения. ПКРЖ чаще встречается у женщин и у более молодых пациентов в возрастной группе от 55 до 61 лет[4][6].
Диагностика
Клинические проявления ПКРЖ подразделяются на общие и местные, связанные с локализацией и характером роста опухоли. К общим симптомам относятся немотивированная слабость, прогрессирующая потеря веса, снижение аппетита, тошнота, картина анемии и боли в животе. Локальные проявления определяются анатомическим расположением новообразования: при поражении кардиоэзофагеального перехода развивается дисфагия; опухоль антрального отдела с формированием пилоростеноза приводит к тошноте и рвоте съеденной пищей. Изъязвлённые формы часто осложняются кровотечением и перфорацией, а диффузно-инфильтративный рост, вызывающий уменьшение объёма желудка, сопровождается чувством быстрого насыщения после приёма даже небольшого количества еды[4].
Клинический анализ крови, коагулограмма, биохимический анализ крови и клинический анализ мочи выполняются с целью оценки общего состояния и выявления сопутствующей патологии перед планируемым лечением[4].
Гистологическое исследование биоптата опухоли: для подтверждения диагноза ПКРЖ необходимо выявление более 50 % перстневидных клеток в биоптате[4].
Молекулярно-генетический анализ методом секвенирования: возможно выявление мутации в гене CDH1[2].
Эндоскопическое исследование: позволяет непосредственно визуализировать опухолевый очаг, точно определить его размеры, локализацию и макроскопический тип роста (экзофитный, язвенно-инфильтративный или диффузный), а также оценить угрозу потенциальных осложнений, таких как кровотечение или перфорация. При ПКРЖ эндоскопическая картина может иметь свои особенности: нередко выявляется диффузная инфильтрация стенки желудка без чётко очерченного экзофитного компонента, что приводит к ригидности стенок и сужению просвета (симптом «кожаного мешка»). Слизистая оболочка при этом часто выглядит бледной, сглаженной, с эрозиями или без выраженных язвенных дефектов[4].
Рентгенологическое исследование верхних отделов желудочно-кишечного тракта с двойным контрастированием (пассаж бария) может быть использовано для определения протяжённости поражения в случаях, когда присутствуют обструктивные симптомы, или когда объёмная проксимальная опухоль препятствует прохождению эндоскопа для осмотра отделов желудка ниже препятствия (чаще при опухолях гастроэзофагеального перехода)[7].
На компьютерных томограммах ПКРЖ может иметь различный вид: полиповидное образование с изъязвлением или без него, очаговое утолщение стенки с неровностью слизистой или изъязвлением, диффузное утолщение стенки с отсутствием нормальных складок слизистой оболочки (инфильтративные поражения), очаговая инфильтрация стенки желудка, а также неравномерное утолщение стенки и выраженное контрастное усиление, что типично для скиррозных (фиброзных) форм рака. Из-за высокого содержания муцина клетки ПКРЖ имеют пониженную плотность (низкое затухание) на снимках, а также могут содержать участки кальцификации[7].
Для комплексной оценки локального процесса и поиска отдалённых очагов (увеличенные лимфатические узлы, возможные метастазы) проводится компьютерная или магнитно-резонансная томография грудной клетки, брюшной полости и малого таза и ультразвуковое исследование органов брюшной полости[4][7].
Эндоскопическое ультразвуковое исследование (эндосонография) позволяет определить глубину инвазии опухоли и наличие патологически изменённых или увеличенных вовлечённых лимфоузлов, а также прорастание опухоли в соседние структуры[4].
Дифференциальная диагностика
Дифференциальная диагностика ПКРЖ проводится со следующими заболеваниями[4][8]:
- Другие гистологические типы рака желудка:
- тубулярная аденокарцинома;
- слизистая (муцинозная) аденокарцинома;
- папиллярная аденокарцинома;
- аденокарцинома смешанного строения;
- медуллярный рак с лимфоидной стромой;
- микропапиллярный рак;
- плоскоклеточный рак;
- железисто-плоскоклеточный рак;
- мукоэпидермоидный рак;
- панетоклеточный рак;
- париетальноклеточный рак;
- гепатоидная аденокарцинома;
- рак с остеокластоподобными гигантскими клетками;
- крупноклеточный рак с рабдоидным фенотипом;
- плеоморфный рак;
- саркоматоидный (веретеноклеточный) рак;
- недифференцированный (анапластический) рак;
- гастробластома.
- Острый гастрит.
- Атрофический гастрит.
- Бактериальный гастроэнтерит.
- Хронический гастрит.
- Рак пищевода.
- Стриктура пищевода.
- Эзофагит.
- Неходжкинская лимфома.
- Язвенная болезнь.
- Вирусный гастроэнтерит.
Осложнения
Осложнения, связанные непосредственно с первичной опухолью при ПКРЖ, включают кровотечение, обструкцию просвета органа, перфорацию стенки желудка и образование свищей в соседние органы. Осложнения, возникающие вследствие хирургического лечения, включают интра- и послеоперационное кровотечение, инфекционные осложнения (инфекции области хирургического вмешательства и внутрибрюшинные), несостоятельность анастомозов, интраоперационное повреждение окружающих структур (таких как селезёнка и двенадцатиперстная кишка), а также отдалённые осложнения, например, развитие послеоперационных грыж[8].
Лечение
Стандартные методы лечения применяются в соответствии с общими принципами терапии рака желудка, однако особых, более эффективных протоколов для данного гистологического подтипа не разработано. Лечение ПКРЖ основывается на стадии заболевания. При раннем раке, ограниченном слизистой оболочкой, методом выбора является эндоскопическая подслизистая резекция. Во всех остальных случаях основой радикального лечения служит обширное хирургическое вмешательство. Объём операции определяется локализацией и типом опухоли. Для ПКРЖ, особенно при диффузно-инфильтративном росте или наследственном синдроме, стандартом является гастрэктомия с расширенной лимфодиссекцией (D2). Резекция желудка для этого подтипа обычно не применяется. Системная терапия используется для повышения эффективности лечения. При местно-распространённых, но операбельных опухолях стандартом стала периоперационная химиотерапия, которая проводится до и после операции. Если лечение начато с хирургии, то после неё может назначаться адъювантная химиотерапия, особенно пациентам с факторами высокого риска рецидива (поражение лимфоузлов, низкая дифференцировка опухоли)[4].
Прогноз
ПКРЖ характеризуется крайне неблагоприятным прогнозом по сравнению с другими гистологическими типами аденокарциномы желудка. Данная опухоль ассоциирована с более агрессивным течением заболевания, что выражается в больших размерах первичного узла на момент диагностики, более глубокой инвазии в стенку желудка и обширном метастатическом поражении регионарных лимфатических узлов. Совокупность этих биологических особенностей напрямую обусловливает значительно худшие показатели выживаемости пациентов с ПКРЖ[2][4].
Диспансерное наблюдение
После завершения радикального лечения пациентам с ПКРЖ рекомендовано регулярное диспансерное наблюдение. Его целью является раннее выявление местного рецидива, отдалённых метастазов или метахронных опухолей для своевременного начала терапии. График наблюдения зависит от вида проведённого лечения. После хирургической операции в первые 1—2 года осмотр проводят каждые три — шесть месяцев. На третий — пятый год после операции — один раз в шесть — двенадцать месяцев. Через пять лет после лечения визиты назначаются ежегодно или при появлении жалоб. Для пациентов с высоким риском рецидива интервалы между осмотрами могут быть сокращены. После эндоскопической подслизистой резекции контрольную эзофагогастродуоденоскопию выполняют каждые три месяца в первый год, каждые шесть месяцев на второй и третий годы, а затем — ежегодно[4].
Объём обследования при каждом плановом визите включает: сбор жалоб, анамнеза и физикальный осмотр, лабораторные исследования (клинический и биохимический анализ крови), эзофагогастродуоденоскопию согласно установленному графику, инструментальные исследования по клиническим показаниям (ультразвуковое исследование или компьютерная томография органов брюшной полости, рентгенография органов грудной клетки), а также обязательную оценку нутритивного статуса пациента и коррекцию нутритивной недостаточности при её выявлении[4].
Профилактика
Общие меры профилактики ПКРЖ включают соблюдение диеты, исключающей термическое и механическое повреждение слизистой оболочки, отказ от курения и употребления алкоголя, а также своевременное лечение фоновых и предопухолевых заболеваний желудка. Для пациентов с наследственной предрасположенностью, а именно с подтверждённой мутацией в гене CDH1, которая лежит в основе наследственного диффузного рака желудка, рекомендован особый режим: тактика включает динамическое наблюдение с проведением эндоскопического обследования каждые 6—12 месяцев. Согласно позиции ряда экспертов, для носителей данной мутации, особенно в возрасте от 18 до 40 лет, может быть рассмотрено выполнение профилактической гастрэктомии без проведения расширенной лимфодиссекции[4].
Примечания
Литература
- Волченко Н. Н., Баранова И. Б., Борисова О. В. Перстневидноклеточный рак желудка. Возможности цитологической диагностики. Клинический случай // Новости клинической цитологии России. — 2021. — № 1. — doi:10.24412/1562-4943-2021-1-0002.
- Fung B. M., Patel M., Patel N. et al. Signet Ring Cell Gastric Carcinoma: Clinical Epidemiology and Outcomes in a Predominantly Latino County Hospital Population (англ.) // Digestive Diseases and Sciences. — 2021. — Vol. 66. — P. 1240—1248. — doi:10.1007/s10620-020-06341-z.
- Zhang Z. S., Deng W. Y., Huang S. L. et al. Clinicopathological characteristics of signet-ring cell carcinoma derived from gastric fovelar epithelium (англ.) // Journal of Digestive Diseases. — 2022. — July (vol. 23, no. 7). — P. 396—403. — doi:10.1111/1751-2980.13120.