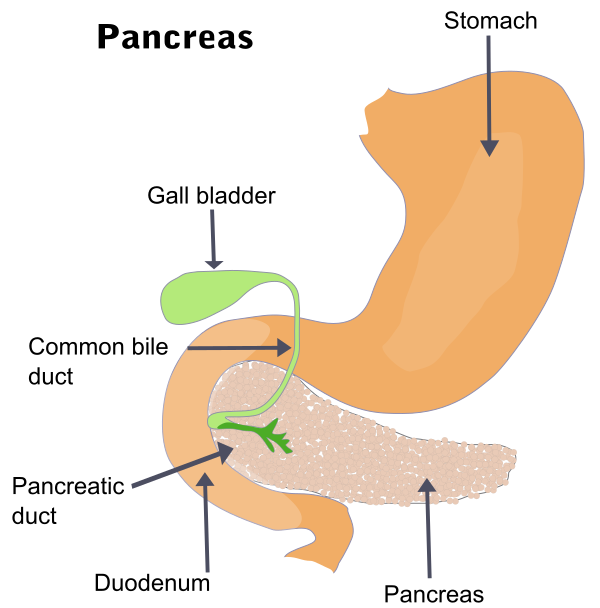
Рак поджелудочной железы
Рак поджелу́дочной железы́ — злокачественное новообразование, исходящее из эпителия железистой ткани или протоков поджелудочной железы.
Общие сведения
Этиология
Заболеваемость раком поджелудочной железы ежегодно увеличивается. Эта болезнь занимает шестое место по распространённости среди онкологических заболеваний среди взрослого населения. Поражает преимущественно людей пожилого возраста, одинаково часто мужчин и женщин[2]. В США в данное время рак поджелудочной железы находится на четвертом месте среди причин смерти от рака. Согласно предварительной оценке Американского онкологического общества, в 2015 году эта опухоль будет выявлена у 48 960 человек, и 40 560 пациентов погибнут. Риск возникновения рака у каждого жителя США в течение жизни составляет 1,5 %[3].
Факторами риска рака поджелудочной железы являются:
- употребление спиртных напитков
- курение
- обилие жирной и острой пищи
- сахарный диабет
- цирроз печени
К предраковым заболеваниям относятся:
- Аденома поджелудочной железы
- Хронический панкреатит
- Киста поджелудочной железы
Обычно опухоль поражает головку железы (50-60 % случаев), тело (10 %), хвост (5-8 % случаев). Также наблюдается полное поражение поджелудочной железы — 20-35 % случаев. Опухоль представляет собой плотный бугристый узел без чётких границ, на разрезе — белый или светло-жёлтый.
Недавно обнаружен ген, влияющий на форму нормальных клеток поджелудочной железы, который может принимать участие в развитии рака. По результатам исследования, опубликованного в журнале Nature Communications, целевой ген — это ген протеинкиназы P1 (PKD1). Воздействуя на него, можно будет затормозить рост опухоли. PKD1 контролирует как рост, так и метастазирование опухоли. На данный момент исследователи заняты созданием ингибитора PKD1, для того, чтобы можно было провести его дальнейшие испытания[4]
В ходе исследования, проведенного в медицинском центре Лангон при Университете Нью-Йорка, было выявлено, что вероятность развития рака поджелудочной железы на 59 % выше у тех пациентов, у которых в ротовой полости присутствует микроорганизм Porphyromonas gingivalis. Также риск заболевания в два раза выше, если у пациента будет обнаружен Aggregatibacter actinomycetemcomitans. На данный момент разрабатывается скрининговый тест, который позволит определять вероятность развития рака поджелудочной железы[5].
Гистологические формы
Всего насчитывают 5 гистологических форм рака поджелудочной железы:
- Аденокарцинома
- Плоскоклеточный рак
- Цистаденокарцинома
- Ацинарно-клеточный рак
- Недифференцированный рак
Наиболее распространена аденокарцинома, наблюдающаяся в 80 % случаев рака поджелудочной железы[2].
Метастазирование
Лимфогенное метастазирование рака поджелудочной железы имеет 4 стадии. На первой стадии поражаются панкреатодуоденальные лимфатические узлы (около головки поджелудочной железы), на второй — ретропилорические и гепатодуоденальные, затем на третьей — чревные и верхнебрыжеечные лимфатические узлы и на четвёртой стадии — забрюшинные (парааортальные) лимфатические узлы.
Гематогенное метастазирование приводит к развитию отдалённых метастазов в печени, лёгких, почках, костях.
Кроме того, наблюдается имплантационный перенос опухолевых клеток по брюшине.
Клиническая классификация
Клиническая TNM-классификация применяется только к карциномам экзокринной части поджелудочной железы и нейроэндокринным опухолям поджелудочной железы, включая карциноиды.
T — первичная опухоль
- Tx — первичная опухоль не может быть оценена
- T0 — отсутствие данных о первичной опухоли
- Tis — карцинома in situ
- T1 — опухоль не более 2 см в наибольшем измерении в пределах поджелудочной железы
- T2 — опухоль более 2 см в наибольшем измерении в пределах поджелудочной железы
- T3 — опухоль распространяется за пределы поджелудочной железы, но не поражает чревный ствол или верхнюю брыжеечную артерию
- T4 — опухоль прорастает в чревный ствол или верхнюю брыжеечную артерию
Примечания:
Tis также включает панкреатическую интраэпителиальную неоплазию III.
N — регионарные лимфатические узлы
- Nx — регионарные лимфатические узлы не могут быть оценены
- N0 — нет метастазов в регионарных лимфатических узлах
- N1 — есть метастазы в регионарных лимфатических узлах
Примечания: Регионарными лимфатическими узлами являются околопанкреатические узлы, которые можно подразделить следующим образом:
| группа узлов | локализация |
|---|---|
| Верхние | сверху над головкой и телом |
| Нижние | снизу под головкой и телом |
| Передние | передние поджелудочно-двенадцатиперстные, пилорические (только для опухолей головки) и проксимальные брыжеечные |
| Задние | задние поджелудочно-двенадцатиперстные, лимфатические узлы общего жёлчного протока и проксимальные брыжеечные |
| Селезёночные | узлы ворот селезёнки и хвоста поджелудочной железы (только для опухолей тела и хвоста) |
| Чревные | только для опухолей головки |
M — отдалённые метастазы
- M0 — нет отдалённых метастазов;
- M1 — есть отдалённые метастазы.
Стадии
| стадия | критерий T | критерий N | критерий M |
|---|---|---|---|
| Стадия 0 | Tis | N0 | М0 |
| Стадия IA | T1 | N0 | М0 |
| Стадия IB | T2 | N0 | М0 |
| Стадия IIA | T3 | N0 | М0 |
| Стадия IIB | T1, T2, T3 | N1 | М0 |
| Стадия III | T4 | Любая N | М0 |
| Стадия IV | Любая T | Любая N | М1 |
Симптомы
Симптомы рака поджелудочной железы часто не специфичны и не выражены, в связи с чем опухоль во многих случаях обнаруживается на поздних стадиях процесса. Среди симптомов наиболее часто присутствует механическая желтуха при прорастании или компрессии желчных протоков.
Если опухоль поражает головку железы, то она проявляется синдромом Курвуазье: при пальпации правого верхнего квадранта живота обнаруживается желчный пузырь, увеличенный вследствие давления желчи. Рак тела и хвоста поджелудочной железы сопровождается ноющей болью в эпигастрии, которая иррадиирует в поясницу и зависит от положения тела. Прорастание опухолью желудка и поперечно-ободочной кишки вызывает нарушения их проходимости. В дальнейшем нарушается функция железы и других органов пищеварительного тракта. Возможны кровотечения из поражённых органов.
Рак поджелудочной железы также сопровождается общими симптомами, характерными для злокачественных опухолей: раковая интоксикация, снижение аппетита и массы тела, общая слабость, повышение температуры организма и др.
Диагностика
Традиционными диагностическими методами исследования являются ультразвуковое исследование и компьютерная томография с болюсным контрастным усилением. Эти методы позволяют визуализировать не только распространённость первичной опухолевой массы, но и оценить наличие метастазов, сопутствующей патологии. Помимо этого, по показаниям применяются такие рентгенологические методы, как исследование желудка и двенадцатиперстной кишки с сульфатом бария (для оценки наличия дефектов наполнения из-за сдавления опухолью), эндоскопическая ретроградная холангиопанкреатография (для оценки распространённости поражения жёлчных и панкреатических протоков, морфологической верификации). С диагностической целью может применяться диагностическая лапароскопия, лапаротомия с биопсией или тонкоигольная биопсия под контролем УЗИ.
Кроме методов, позволяющих определить анатомические особенности образования поджелудочной железы, существуют методы, позволяющие индивидуально определить прогноз течения заболевания. Одним из таких методов является определение в крови матриксных металлопротеиназ[6][7][8][9].
Значительным прогрессом в диагностике рака поджелудочной железы на ранней стадии является эндосонография (эндоскопический ультразвук)[10]. В отличие от обычного УЗИ, для эндосонографии используется гибкий эндоскоп с видеокамерой и ультразвуковым датчиком, который можно ввести в кишку непосредственно к исследуемому образованию. Эндосонография решает проблему четкости изображения, которая возникает при исследовании глубоких органов чрескожным методом. При раке поджелудочной железы эндоскопический ультразвук позволяет установить диагноз в 95—98 % случаев на самой ранней стадии.
В начале 2012 года 15-летний первокурсник Джек Андрака (англ. Jack Andraka) из North County High School, расположенной в пригороде Балтимора городе Glen Burnie, штат Мэриленд, США, изобрёл тестер рака[11], который позволяет диагностировать рак поджелудочной железы, лёгких и яичек на ранних стадиях путём анализа крови или мочи. Указанный тестер создан на основе бумаги для проведения диабетических тестов.
По заявлению автора, основанному на некорректных оценках[12], метод более чем в сто раз быстрее, в десятки—тысячи раз дешевле (бумажный тестер при массовом изготовлении стоит не дороже 3-х центов) и в сотни раз более чувствителен, чем существовавшие до этого методы тестирования. Точность результатов по предварительным заявлениям может составлять 90 % или более. На разработку и исследования юного изобретателя подвигла смерть от рака поджелудочной железы близкого друга семьи мальчика.
За свою инновационную разработку Джек Андрака в мае 2012 года получил грант в сумме $75 000 на Всемирном конкурсе научных и инженерных достижений школьников, который ежегодно проходит в США (Intel ISEF 2012). Грант профинансирован компанией Intel. В январе 2014 года в журнале Forbes была опубликована статья, в которой способ тестирования Джека Андрака ставится под сомнение[12].
Лечение
- Хирургическое вмешательство (по показаниям, при отсутствии метастазов — в 10—15 % случаев)
- Радиотерапия (в комплексе с хирургическим вмешательством)
- Химиотерапия
- Гормональная терапия
- Симптоматическая терапия (обезболивание и др.)
- Виротерапия
- Необратимая электропорация (нанонож)
Из хирургических методов наиболее распространена при раке поджелудочной железы панкреатодуоденальная резекция (операция Уиппла), которая включает удаление головки поджелудочной железы с опухолью, участка двенадцатиперстной кишки, части желудка и жёлчного пузыря с регионарными лимфоузлами. Противопоказанием к операции считается распространение опухоли на крупные рядом лежащие сосуды и наличие отдаленных метастазов.
Послеоперационное лечение, называемое адъювантной терапией, проводится пациентам, у которых нет выявленных признаков остаточной болезни, но есть вероятность того, что в организме остались микроскопические опухолевые частицы, способные в отсутствие лечения привести к рецидиву опухоли и смерти[13]. Клинические рекомендации Ассоциации онкологов России 2018 года содержат 3 основных режима: GEMCAP, гемцитабин, фторпиримидины[14].
Другие препараты: олапариб.
Прогноз
Условно неблагоприятный. Современные хирургические методики позволяют снизить периоперационную смертность до 5 %. Однако медиана выживаемости после операции составляет 15-19 месяцев, а пятилетняя выживаемость — менее 20 %[15]. Если полное удаление опухоли невозможно, практически всегда следует рецидив; у оперированных больных с рецидивом продолжительность жизни в 3—4 раза больше, чем у неоперированных.[16] Современное состояние медицины не позволяет эффективно излечивать рак поджелудочной железы и в основном концентрируется на симптоматической терапии. В некоторых случаях положительный эффект даёт терапия интерфероном. Средняя 5-летняя выживаемость после радикального хирургического лечения составляет 8-45 %, что делает его одним из самых опасных заболеваний. В 2020 году во всем мире летальность от рака поджелудочной железы составила — 93,99 % (на 495 773 случаев 466 003 смертей)[17].
Другие опухоли поджелудочной железы
- Карциноидные опухоли
- Нейроэндокринные опухоли и опухоли из островковых клеток — инсулома
Примечания
Литература
- Ганцев Ш. Х. Онкология: Учебник для студентов медицинских вузов. — М.: ООО «Медицинское информационное агентство», 2006. — 488 с. — 5000 экз. — ISBN 5-89481-418-9.
- TNM: Классификация злокачественных опухолей. / Под ред. Л. Х. Собинина и др.; пер. с англ. и науч. ред. А. И. Щёголева, Е. А. Дубовой, К. А. Павлова. — М.: Логосфера, 2011. — 276 с. — Перевод изд. TNM Classification of Malignant Tumours, 7th ed. — ISBN 978-5-98657-025-9.
- Кубышкин В. А. Рак поджелудочной железы. // Consilium medicum. Том 5, № 8 (2003).
- Местно-распространенный рак. Пер. с англ. Н. Д. Фирсова (2017).