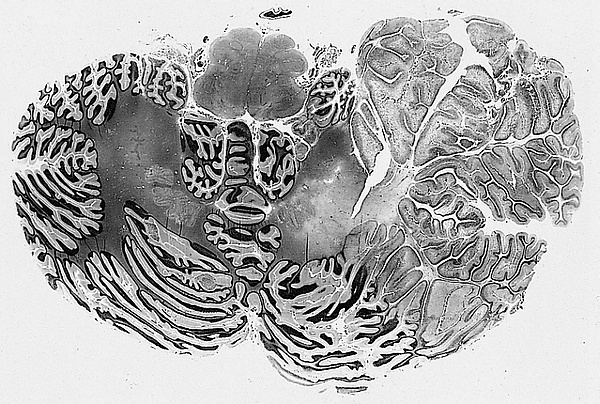
Болезнь Лермитта — Дюкло
Болезнь Лермитта — Дюкло (БЛД; диспластическая ганглиоцито́ма мозжечка́) — крайне редкое наследственное заболевание, характеризующееся образованием медленно растущей доброкачественной гамартомы в мозжечке. Основные клинические проявления включают головную боль, тошноту, рвоту, папиллоэдему, мозжечковую атаксию, хромоту и различные нервно-психологические нарушения. Заболевание связано с мутациями в гене PTEN, который выполняет функцию супрессора опухолевого роста. Единственным эффективным методом лечения остаётся хирургическое вмешательство[1].
Что важно знать
История
Впервые это заболевание описали в 1920 году французский невропатолог Жан-Жак Лермитт и его коллега Пьер Дюкло. Они представили клинический случай 36-летнего мужчины, у которого первые симптомы проявились ещё в 10-месячном возрасте в виде снижения слуха с левой стороны и болей в затылочной области. Позднее другие зарубежные исследователи также описывали клинические проявления этой патологии. В медицинской литературе болезнь упоминалась под разными названиями: диффузная ганглиоцитома мозжечка, пуркинома, гамартома, диспластическая ганглиоцитома, диффузная ганглионеврома, а также гипертрофия зернистого слоя мозжечка. В 1937 году хирург Кристенсен сообщил о первом успешном оперативном вмешательстве при диспластической ганглиоцитоме правого полушария мозжечка. Позднее, в 1969 году, Амбер впервые зафиксировал семейный случай этого заболевания. Важным этапом в изучении патологии стало открытие в 1997 году гена PTEN, мутации в котором связаны с развитием БЛД[1].
Этиология
БЛД передаётся по аутосомно-доминантному типу наследования и развивается из-за мутации гена PTEN (phosphate and tensin homolog), расположенного в локусе 10q23.31. Примерно у 90 % пациентов с БЛД выявляются мутации либо в самом этом гене, либо в его промоторных регионах. Он кодирует липидную фосфатазу, которая действует на фосфатидилинозитол-3-киназу (PI3K). Подавляя активность серин/треонинкиназы, PTEN регулирует сигнальный путь PI3K, что в итоге способствует усилению апоптоза и предотвращает неконтролируемое клеточное деление[2].
Патогенез
Белок PTEN выполняет две важные функции: во-первых, он подавляет образование серин/треонинкиназы, способствующей опухолевому росту, а во-вторых, предотвращает чрезмерную активацию фосфоинозитид-3-киназного сигнального пути, который часто бывает задействован в онкогенезе. В нормальных условиях PTEN поддерживает баланс между пролиферацией и запрограммированной гибелью клеток, сдерживая их неконтролируемое размножение. Однако при возникновении мутаций в гене PTEN нарушается функционирование кодируемого им белка. Это приводит к сбоям в регуляции клеточного цикла, в результате чего клетки начинают бесконтрольно делиться и разрастаться[1].
Гистологически при БЛД выявляются следующие патологические изменения: отсутствие слоя клеток Пуркинье, выраженное утолщение молекулярного слоя с признаками избыточной миелинизации аксонов, гипертрофия зернистого слоя мозжечка. Характерной особенностью является замещение нормального зернистого слоя диспластическими кортикальными нейронами, а также прогрессирующая атрофия белого вещества мозжечка. Эти структурные изменения формируют уникальную гистологическую картину заболевания[3].
Эпидемиология
Эпидемиология БЛД остаётся недостаточно изученной — в мире описано 300 случаев заболевания. Наиболее часто болезнь проявляет себя в возрасте от 20 до 40 лет, при этом гендерных различий в распространённости не наблюдается[3].
Диагностика
БЛД может проявляться уже в детском возрасте, когда возникают первые симптомы прогрессирующего поражения задней черепной ямки. Длительность развития клинических проявлений варьирует от нескольких месяцев до десятилетий. Наиболее выраженное скопление патологических клеток при БЛД обычно формируется к 30—40 годам, что определяет характерную динамику симптоматики. Типичными проявлениями являются поражение черепных нервов, мозжечковая атаксия и признаки внутричерепной гипертензии, которые часто развиваются вследствие острой или хронической гидроцефалии, хотя в некоторых случаях заболевание может протекать бессимптомно[2].
Для данной патологии характерна ассоциация с различными пороками развития, например, макроцефалия, гидроцефалия, сирингомиелия и скелетные аномалии (полидактилия, синдактилия, асимметрию лицевого скелета). Реже наблюдаются липомы, нейрофибромы, гемангиомы и папулёзные высыпания на языке. В ряде случаев заболевание сочетается с поражениями щитовидной и молочной желёз, патологией мочеполовой системы и желудочно-кишечными нарушениями[2].
При магнитно-резонансной томографии головного мозга выявляются характерные изменения в виде слоистого рисунка: на T1-взвешенных изображениях определяется гипоинтенсивный сигнал, в то время как T2-взвешенные изображения демонстрируют чередование участков высокой и низкой интенсивности, что создаёт патогномоничный «тигровый» рисунок[3].
При компьютерной томографии головного мозга выявляется неспецифическое гиподенсное образование в мозжечке, в ряде случаев с участками кальцификации. Патологический процесс преимущественно затрагивает кору одного полушария мозжечка, иногда распространяясь на червь, и лишь в редких случаях переходит на противоположное полушарие[4].
По данным позитронно-эмиссионной томографии и однофотонной эмиссионной компьютерной томографии: выявляется повышенное накопление радиофармпрепарата (фтордезоксиглюкозы при позитронно-эмиссионной томографии, таллия-201 при однофотонной эмиссионной компьютерной томографии), что отражает усиленный метаболизм в области поражения[4].
По данным магнитно-резонансной спектроскопии выявляются характерные метаболические изменения: повышение концентрации лактата, умеренное снижение N-ацетиласпартата (примерно на 10 %), значительное уменьшение концентрации мио-инозитола (на 30—80 %) и холина (на 20—50 %), а также снижение соотношения холин/креатин[4].
Молекулярно-генетический анализ: характерно выявление мутации в гене PTEN методом секвенирования[1].
Осложнения
Наиболее частым осложнением после лечения являются стойкие мозжечковые нарушения, за которыми следуют судорожные приступы, а также редкие случаи мозжечкового мутизма в сочетании с дыхательными расстройствами. У небольшого числа пациентов развивались гидроцефалия, инфекции шунтирующих систем и вентрикулиты. В единичных случаях отмечались такие тяжёлые последствия, как энцефаломаляция, несахарный диабет, ухудшение зрения и выраженная гипотензия[3].
Дифференциальная диагностика
Дифференциальная диагностика БЛД проводится со следующими заболеваниями[3]:
- церебеллит;
- подострый инфаркт мозжечка;
- медуллобластома с обширной нодулярностью;
- синдром Коудена.
Лечение
Хирургическое удаление опухоли остаётся наиболее эффективным методом лечения БЛД. Оперативное вмешательство часто сопряжено с техническими трудностями из-за диффузного характера поражения и отсутствия чётких границ патологического очага в глубинных структурах мозжечка[1][3].
В отдельных случаях описано применение лучевой терапии и химиотерапии[3].
Прогноз
Благодаря доброкачественному характеру и медленному росту опухоли при БЛД прогноз в большинстве случаев благоприятный. У пациентов без клинических симптомов хирургическое вмешательство может не требоваться. В медицинской литературе не зафиксировано ни одного случая злокачественного перерождения данного новообразования[5].
Примечания
Литература
- Бимурзин А. А., Калиновский А. В. Хирургическое лечение болезни Лермитта–Дюкло (диспластической ганглиоцитомы мозжечка) (рус.) // Нейрохирургия : журнал. — 2020. — Т. 22, № 1. — С. 77—82. — doi:10.17650/1683-3295-2020-22-1-77-82.