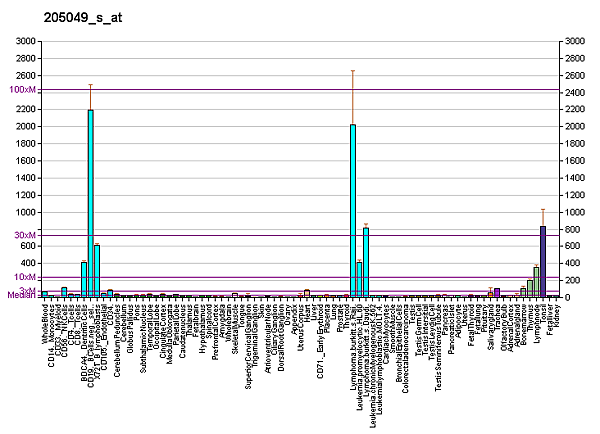
CD79A
CD79A (англ. B-cell antigen receptor complex-associated protein alpha chain) — мембранный белок, продукт гена человека CD79A[5]. Вместе с родственным белком CD79B образует гетеродимер, ассоциированный с мембрано-связанным иммуноглобулином на поверхности B-лимфоцита, что формирует B-клеточный рецептор. Аналогичным образом CD79A ассоциирует с CD3 в Т-клеточном рецепторе и позволяет клетке отвечать на присутствие антигена на клеточной поверхности[6]. Ген связан с развитием агаммаглобулинемии 3-го типа[7].
Что важно знать
| CD79A | |||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | CD79A, IGA, MB-1, CD79a molecule, MB1, IGAlpha | ||||||||||||||||||||||||||||||||||||||||||||||
| Внешние ID | OMIM: 112205 MGI: 101774 HomoloGene: 31053 GeneCards: CD79A | ||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
Ген
Ген CD79A мыши был клонирован в 1980-х годах[8], ген CD79A человека был открыт в начале 1990-х годов[9][10]. Короткий ген длиной 4.3 kb содержит 5 экзонов.
Ген CD79A характеризуется консервативной последовательностью в ходе эволюции, начиная с лучепёрых рыб, но отсутствует у хрящевых рыб, таких как акулы[11]. Таким образом, появление CD79A совпадает с эволюцией B-клеточного рецептора с более широким разнообразием в результате рекомбинации множественных элементов V, D и J у костистых рыб по сравнению с единственными элементами V, D и J у акул[12].
Структура белка
CD79A состоит из 226 аминокислот, молекулярная масса 30,0 кДа. В результате альтернативного сплайсинга образуется 2 изофомы[5]. Это мембранный белок с внеклеточным иммуноглобулиновым доменом, одним трансмембранным участком и коротким цитоплазматическим доменом[5]. Цитоплазматический участок содержит множественные участки фосфорилирования, включая консервативный мотив связывания с двойным фосфотирозином ITAM[13][14]. Более крупная изоформа у человека содержит участок 88-127, образуя полный иммуноглобулиновый домен, тогда как короткая изоформа имеет укороченный иммуноглобулиновый домен[5] CD79a has several cysteine residues, one of which forms covalent bonds with CD79b.[15].
Функции
CD79a имеет несколько функций в развитии и функционировании B-клеток. Гетеродимер CD79a/b нековалентно ассоциирован с тяжёлой цепью иммуноглобулина через свой трансмембранный домен и образует либо B-клеточный рецептор вместе с лёгкой цепью иммуноглобулина, либо пре-B-клеточный рецептор вместе с суррогатной лёгкой цепью в развивающихся B-клетках. Ассоциация гетеродимера CD79a/b с тяжёлой цепью иммуноглобулина необходима для поверхностной экспрессии B-клеточного рецептора и индуцируемого рецептором входа кальция и фосфорилирования тирозина[16]. Генетическая делеция трансмембранного экзона в гене CD79A приводит к потере белка и полной блокировки развития B-клеток на этапе перехода про-B- в пре-B-клетку[17]. Аналогично, у больных с гомозиготным вариантом сплайсинга развивается потеря трансмембранного участка и укороченный белок или его отсутствие приводит к агаммаглобулинемии и дефицита периферических B-клеток[7][18][19].
Остатки тирозина в ITAM-мотиве CD79a (Tyr188 и Tyr199 у человека; Tyr182 и Tyr193 у мыши), которые фосфорилируются в ответ на перешивку B-клеточного рецептора, играют критическую роль в связывании Syk-киназ и переносе сигнала[20][21]. Кроме этого, тирозины ITAM-мотивов CD79a и CD79b синергически опосредуют переход про-B- в пре-B-клетки[22][23]. Потеря одного из двух ITAM-мотивов CD79a/b приводит к нарушению развития B-клеток, однако независимый от T-клеток ответ типа II и опосредуемый B-клеточным рецептором вход кальция остаётся нормальным. Однако наличие обоих функциональных ITAM-мотивов CD79a/b необходимо для нормального T-лимфоцит-зависимого ответа[22][24]. Цитоплазматический домен CD79a содержит дистальный от ITAM-мотива тирозин (Tyr210 у человека, Tyr204 у мыши), который после фосфорилирования может связываться с BLNK и Nck[25][26][27] и критически важен для рецептор-опосредованной пролиферации B-клеток и развития В1-клеток[28]. Фосфорилирование тирозинов ITAM-мотива и перенос сигнала отрицательно регилируется остатками серина и треонина, расположенных вблизи мотива (Ser197, Ser203, Thr209 у человека; Ser191, Ser197, Thr203 у мыши)[29][30] и играет роль в ограничении образования плазматических клеток костного мозга, секретирующих IgG2a и IgG2b[23].
В диагностике
Белок CD79a присутствует на поверхности только B-клеток, что делает его надёжным маркёром B-лимфоцитов в иммуногистохимических исследованиях. Белок также остаётся на B-клетках после их трансформации в плазматические клетки, а также на практически всех B-клеточных неоплазмах, включая B-клеточные лимфомы, плазмацитомы и миеломы. CD79a экспрессирован на аномальных лимфоцитах в некоторых случаях болезни Ходжкина. Поскольку CD79a находится на предшественниках B-клеток, этот белок может использоваться для окрашивания более широкого спектра клеток, чем стандартный B-клеточный маркёр CD20, экспрессируемый главным образом на зрелых B-клеточных лимфомах, и, таким образом, часто оба маркёра применяются в иммуногистохимических панелях одновременно[6].
См. также
Примечания
Литература
- Herren B, Burrows PD (2003). “B cell-restricted human mb-1 gene: expression, function, and lineage infidelity”. Immunologic Research. 26 (1—3): 35—43. DOI:10.1385/IR:26:1-3:035. PMID 12403343. S2CID 38456117.
- Leduc I, Preud'homme JL, Cogné M (Oct 1992). “Structure and expression of the mb-1 transcript in human lymphoid cells”. Clinical and Experimental Immunology. 90 (1): 141—6. DOI:10.1111/j.1365-2249.1992.tb05846.x. PMC 1554548. PMID 1395095.
- Müller B, Cooper L, Terhorst C (Jun 1992). “Cloning and sequencing of the cDNA encoding the human homologue of the murine immunoglobulin-associated protein B29”. European Journal of Immunology. 22 (6): 1621—5. DOI:10.1002/eji.1830220641. PMID 1534761. S2CID 23910309.
- Hutchcroft JE, Harrison ML, Geahlen RL (Apr 1992). “Association of the 72-kDa protein-tyrosine kinase PTK72 with the B cell antigen receptor”. The Journal of Biological Chemistry. 267 (12): 8613—9. PMID 1569106.
- Yu LM, Chang TW (Jan 1992). “Human mb-1 gene: complete cDNA sequence and its expression in B cells bearing membrane Ig of various isotypes”. Journal of Immunology. 148 (2): 633—7. PMID 1729378.
- Venkitaraman AR, Williams GT, Dariavach P, Neuberger MS (Aug 1991). “The B-cell antigen receptor of the five immunoglobulin classes”. Nature. 352 (6338): 777—81. Bibcode:1991Natur.352..777V. DOI:10.1038/352777a0. PMID 1881434. S2CID 4246284.
- Kurosaki T, Johnson SA, Pao L, Sada K, Yamamura H, Cambier JC (Dec 1995). “Role of the Syk autophosphorylation site and SH2 domains in B cell antigen receptor signaling”. The Journal of Experimental Medicine. 182 (6): 1815—23. DOI:10.1084/jem.182.6.1815. PMC 2192262. PMID 7500027.
- Lankester AC, van Schijndel GM, Cordell JL, van Noesel CJ, van Lier RA (Apr 1994). “CD5 is associated with the human B cell antigen receptor complex”. European Journal of Immunology. 24 (4): 812—6. DOI:10.1002/eji.1830240406. PMID 7512031. S2CID 25093082.
- Vasile S, Coligan JE, Yoshida M, Seon BK (Apr 1994). “Isolation and chemical characterization of the human B29 and mb-1 proteins of the B cell antigen receptor complex”. Molecular Immunology. 31 (6): 419—27. DOI:10.1016/0161-5890(94)90061-2. PMID 7514267.
- Brown VK, Ogle EW, Burkhardt AL, Rowley RB, Bolen JB, Justement LB (Jun 1994). “Multiple components of the B cell antigen receptor complex associate with the protein tyrosine phosphatase, CD45”. The Journal of Biological Chemistry. 269 (25): 17238—44. PMID 7516335.
- Pani G, Kozlowski M, Cambier JC, Mills GB, Siminovitch KA (Jun 1995). “Identification of the tyrosine phosphatase PTP1C as a B cell antigen receptor-associated protein involved in the regulation of B cell signaling”. The Journal of Experimental Medicine. 181 (6): 2077—84. DOI:10.1084/jem.181.6.2077. PMC 2192043. PMID 7539038.