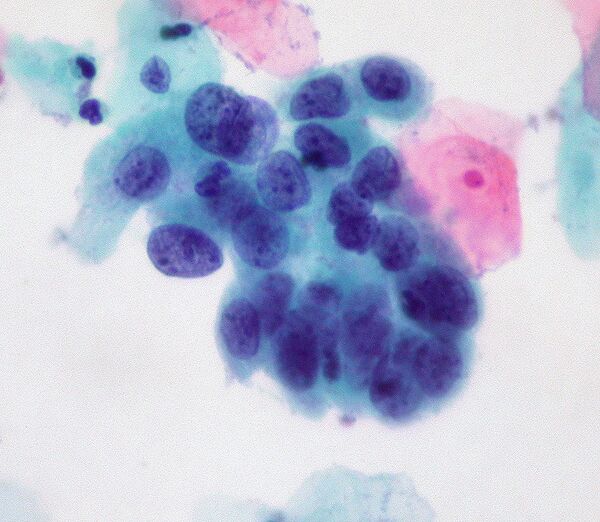
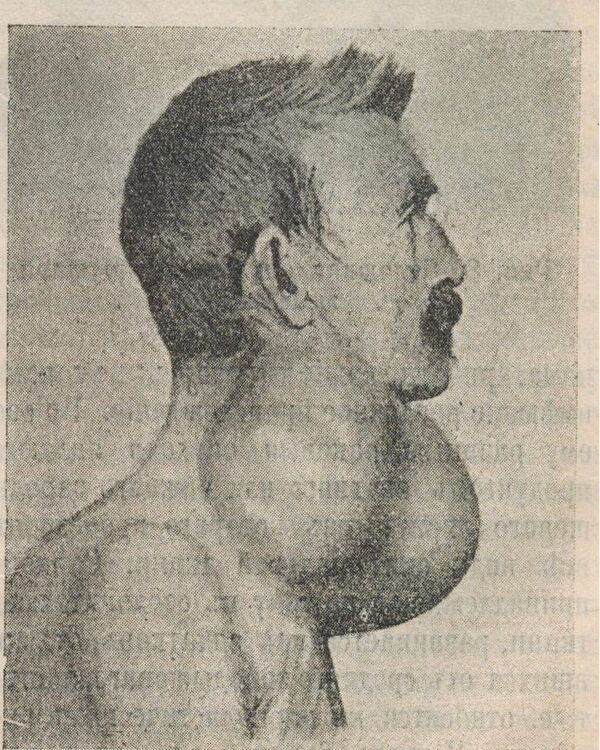
Карцинома
Карцинома (др.-греч. καρκίνος — «рак», -ωμα от ὄγκωμα — «опухоль») — вид злокачественной опухоли (рак)[1], развивающейся из клеток эпителиальной ткани различных органов (кожи, слизистых оболочек и многих внутренних органов)[2]. По данным Всемирной организации здравоохранения, в 2018 году от этого заболевания умерли 9 600 000 человек[3].
Общие сведения
Общей характеристикой злокачественных опухолей является их выраженный клеточный атипизм (утрата клетками способности к дифференцировке с нарушением структуры ткани, из которой происходит опухоль), агрессивный рост с поражением как самого органа, так и других близлежащих органов, склонность к метастазированию, то есть к распространению клеток опухоли с током лимфы или крови по всему организму с образованием новых очагов опухолевого роста во многих органах, удалённых от первичного очага. По темпам роста большинство злокачественных опухолей превосходят доброкачественные и, как правило, могут достигать значительных размеров в короткие сроки. Различают также вид злокачественных местнодеструктирующих опухолей, которые растут с образованием инфильтрата в толще ткани, приводя к её разрушению, но, как правило, не метастазируют (базалиома кожи).
Карцинома в различных органах
- Рак верхушки лёгкого с синдромом Панкоста
- Рак влагалища
- Рак гортани
- Рак губы
- Рак желудка
- Рак лёгкого
- Рак молочной железы
- Рак мочевого пузыря
- Рак печени (гепатоцеллюлярный рак (карцинома))
- Рак поджелудочной железы
- Рак почки
- Рак простаты
- Колоноректальный рак
- Рак шейки матки
- Рак щитовидной железы
- Рак яичника
- Рак мочеточника
- Рак пищевода
- Рак прямой кишки
- Рак ободочной кишки
- Рак кожи (базалиома, плоскоклеточная карцинома)
- Рак матки (также называемый как рак тела матки)
- Рак ротоглотки
- Рак носоглотки
- Рак слизистой оболочки полости рта
- Рак желчевыводящих путей (холангиоцеллюлярный рак (карцинома))
- Рак языка
- Рак гипофиза
- Герминогенный, эмбриональный рак яичка
История
Некоторые археологические исследования свидетельствуют о том, что от различных видов рака страдали ещё неандертальцы[4].
Впервые заболевание было описано в древнеегипетском папирусе Эдвина Смита (ок. 1600 г. до н. э.)[5]. В папирусе описываются восемь случаев опухолей или язв молочной железы, которые были удалены при помощи прижигания раковой ткани, а также сообщается, что от этой болезни нет лечения.
Название «карцином» произошло от введённого Гиппократом (460—370 гг. до н. э.) термина «карцинома», обозначавшего злокачественную опухоль с перифокальным воспалением. Гиппократ назвал опухоль карциномой, потому что она внешне напоминает краба[6]. Он описал несколько видов рака, а также предложил термин ὄγκος[7].
Римский врач Авл Корнелий Цельс (Aulus Cornelius Celsius) в I в. до н. э. предложил на ранней стадии лечить рак удалением опухоли, а на поздних — не лечить вообще. Он перевёл греческое слово καρκίνος на латинское слово cancer, слово рак. Гален использовал слово ὄγκος для описания всех опухолей, что и дало современный корень слову онкология[8].
Заболеваемость
Заболеваемость злокачественными опухолями непрерывно растёт. Ежегодно в мире регистрируется порядка 6 миллионов новых случаев заболевания злокачественными опухолями. Наиболее высокая заболеваемость среди мужчин отмечена во Франции (361 на 100000 населения), среди женщин в Бразилии (283,4 на 100000). Отчасти это объясняется старением населения. Следует отметить, что большинство опухолей развивается у лиц старше 50 лет, а каждый второй онкологический больной старше 60 лет. Наиболее часто поражаются предстательная железа и лёгкие у мужчин и молочная железа у женщин. Смертность от онкологических заболеваний занимает третье место в мире, вслед за заболеваниями сердечно-сосудистой системы и заболеваниями дыхательной системы (в том числе ХОБЛ)[9].
Этиология и патогенез
На данный момент известно большое количество факторов, способных запустить механизмы онкогенеза (вещества или факторы окружающей среды, обладающие таким свойством, называют онкогенами).
- Химические онкогены — к ним относят различные группы полициклических и гетероциклических ароматических углеводородов, ароматические амины, нитрозосоединения, афлатоксины, прочие (винилхлорид, металлы, пластмассы, асбест, многостенные углеродные нанотрубки и др.). Их общей характеристикой является способность реагировать с ДНК клеток, тем самым вызывая их злокачественное перерождение.
- Онкогены физической природы: различные виды ионизирующего излучения (α-, β-, γ-излучение, рентгеновское излучение, нейтронное излучение, протонное излучение, мюонное излучение, кластерная радиоактивность, потоки ионов, осколки деления, нейтрино высоких энергий), ультрафиолетовое излучение.
- Биологические факторы онкогенеза: различные типы вирусов (герпесоподобный вирус Эпштейна — Барр (лимфома Беркитта), вирус папилломы человека (рак шейки матки), вирусы гепатитов B и C (рак печени), несущих в своей структуре специфические онкогены, способствующие модификации генетического материала клетки с её последующей малигнизацией.
- Гормональные факторы — некоторые типы гормонов человека (половые гормоны) могут вызвать злокачественное перерождение тканей, чувствительных к действию этих гормонов (рак молочной железы, рак яичка, рак предстательной железы).
- Генетические факторы. Одним из состояний, которые могут спровоцировать развитие заболевания, является пищевод Баррета.
В целом воздействуя на клетку, канцерогены вызывают определённые нарушения её структуры и функции (в особенности ДНК), что называется инициацией. Повреждённая клетка таким образом приобретает выраженный потенциал к малигнизации. Повторное воздействие канцерогена (того же, что вызвал инициацию, или любого другого) приводит к необратимым нарушениям механизмов, контролирующих деление, рост и дифференцировку клеток, в результате которых клетка приобретает ряд способностей, не свойственных нормальным клеткам организма — промоция. В частности, опухолевые клетки приобретают способность к бесконтрольному делению, теряют тканеспецифическую структуру и функциональную активность, изменяют свой антигенный состав и пр.
Рост опухоли (опухолевая прогрессия) характеризуется постепенным снижением дифференцировки и увеличением способности к бесконтрольному делению, а также изменением взаимосвязи опухолевой клетки с организмом, что приводит к образованию метастазов. Метастазирование происходит преимущественно лимфогенным путём (то есть с током лимфы) в регионарные лимфоузлы, или же гематогенным путём (с током крови) с образованием метастазов в различных органах (лёгкие, печень, кости и т. д.).
Структура
Строение карциномы в значительной степени зависит от структурно-функциональных особенностей клеток органов, из которых она развилась. Так, из клеток, контактирующих с внешней средой (эпителий кожи, слизистой оболочки рта, пищевода, гортани, прямой кишки), развивается опухоль, состоящая из многослойного плоского эпителия (ороговевающего и неороговевающего), которая носит название плоскоклеточной карциномы (плоскоклеточный рак).
Из эпителия железистых тканей (железы бронхов, молочная железа, простата) развивается опухоль железистой структуры (железистый рак) — аденокарцинома.
По степени дифференцировки выделяют:
- Высокодифференцированные опухоли
- Среднедифференцированные опухоли
- Малодифференцированные опухоли
- Недифференцированные опухоли
Для высокодифференцированных опухолей характерно строение, близкое строению ткани, из которой образовалась данная опухоль. В случае средне- и малодифференцированных опухолей сходство структуры опухоли и исходной ткани снижается, становится стёртым. Иногда клеточный и тканевой атипизм новообразования могут быть настолько выраженными, что определить тканевую принадлежность опухоли практически невозможно (недифференцированные опухоли). Как правило, они характеризуются высокой степенью злокачественности (то есть способностью образовывать метастазы).
В зависимости от преобладания в структуре опухоли стромы (соединительной ткани) или паренхимы (раковых клеток), различают простой рак, в котором строма и паренхима развиты в одинаковой степени, медуллярный рак, в структуре которого преобладает паренхима, и фиброзный рак (скирр), в котором преобладает строма.
Многие раковые клетки (особенно с высоким уровнем дифференцировки) сохраняют за собой функцию исходной ткани. Так, клетки аденокарциномы (рак из железистой ткани) могут продуцировать слизь.
Данная классификация использует числовое обозначение различных категорий для обозначения распространения опухоли, а также наличия или отсутствия локальных и отдалённых метастазов.
От лат. tumor — опухоль. Описывает и классифицирует основной очаг опухоли.
- T0 — опухоль клинически не определяется.
- Tis — так называемая «carcinoma in situ» («рак на месте») — то есть не прорастающая базального слоя эпителия.
- T1—4 — различная степень развития очага. Для каждого из органов существует отдельная расшифровка каждого из индексов.
- Tx — практически не используется. Выставляется только на время, когда обнаружены метастазы, но не выявлен основной очаг.
От лат. nodulus — узелок. Описывает и характеризует наличие регионарных метастазов, то есть в регионарные лимфатические узлы.
- Nx — выявление регионарных метастазов не проводилось, их наличие не известно.
- N0 — регионарных метастазов не обнаружено при проведении исследования с целью обнаружения метастазов.
- N1—3 — выявлены регионарные метастазы.
Характеристика наличия отдалённых метастазов, то есть — в отдалённые лимфоузлы, другие органы, ткани (исключая прорастание опухоли).
- Mx — выявление отдалённых метастазов не проводилось, их наличие не известно.
- M0 — отдалённых метастазов не обнаружено при проведении исследования с целью обнаружения метастазов.
- M1 — выявлены отдалённые метастазы.
Для некоторых органов или систем применяются дополнительные параметры (P или G, в зависимости от системы органов), характеризующие степень дифференцировки и морфологическую близость биоптата к здоровым тканям организма. Клиническая значимость данного критерия определяется тем, что опухоли с высокой степенью дифференцировки лучше поддаются лечению.
- Grade 1 (G1) — высокая степень дифференцировки опухоли (менее агрессивная опухоль с лучшим прогнозом).
- Grade 2 (G2) — умеренная степень дифференцировки опухоли.
- Grade 3 (G3) — низкая степень дифференцировки опухоли.
- Grade 4 (G4) — анапластическая, недифференцированная опухоль. Наихудший прогноз.
Клинические проявления
Симптоматика рака зависит главным образом от месторасположения опухоли, от темпов её роста, наличия метастазов.
Наиболее частыми признаками являются:
- Изменение кожных покровов на ограниченном участке в виде растущей припухлости, окружённой каймой гиперемии. Припухлости могут изъязвляться, обнажая глубокие язвы, нечувствительные к лечению.
- Изменение тембра голоса, затруднение глотания или прохождения пищи через пищевод, упорный кашель, боль в области грудной клетки или живота.
- Потеря массы, снижение аппетита, немотивированная слабость, стойкое повышение температуры тела, анемия, уплотнение молочной железы и кровянистые выделения из соска, кровянистые выделения из мочевого пузыря, затруднение мочеиспускания и т. д.
Диагностика
Своевременное обращение к врачу, тщательный сбор анамнеза, проведение внимательного осмотра пациента часто способствуют выявлению рака на ранних стадиях, поддающихся лечению. Особое внимание следует уделять выявлению предопухолевых заболеваний (пигментная ксеродермия, эритроплазия Кейра, меланоз Дюбрея, врождённый множественный полипоз толстой кишки), наличие которых предполагает как лечение, так и постоянный контроль за состоянием здоровья больного[10].
Для выявления опухоли применяются все доступные диагностические методы, например:
- Физикальное обследование пациента
- Рентгенография, компьютерная томография, МРТ
- Общий анализ крови, биохимический анализ крови, выявление опухолевых маркёров в крови
- Пункция, биопсия с морфологическим исследованием
- Эндоскопия (ЭГДС, цистоскопия, бронхоскопия и т. д.)
Дифференциальная диагностика
Лечение
Лечение рака зависит от типа опухоли, её локализации, строения, стадии заболевания в соответствии с классификацией TNM.
Различают следующие типы лечения:
- Хирургическое удаление опухоли с прилежащими тканями. Эффективно для лечения опухолей небольших размеров, доступных для хирургического вмешательства, и при отсутствии метастазов. Нередко после хирургического лечения могут возникать рецидивы опухоли.
- Лучевая терапия применяется для лечения малодифференцированных опухолей, чувствительных к радиации. Также применяются для локального разрушения метастазов.
- Химиотерапия используется для лечения различных, зачастую, поздних стадий рака с использованием цитотоксических средств, гормональных/антигормональных средств, иммунных препаратов, ферментных препаратов, противоопухолевых антибиотиков[11] и других лекарственных препаратов, которые разрушают или замедляют рост раковых клеток.
- Генная терапия наиболее современный метод лечения, суть которого заключается в воздействии на систему STAT (signal transduction and activator of transcription) и другие системы, тем самым регулируя процесс деления клеток.
- Нейтрон-захватная терапия — метод лечения опухоли, похожий на лучевую терапию, но отличающийся от неё тем, что используются нейтроны вместо обычного облучения. Нейтроны проникают глубоко в ткани опухоли, поглотившие, например, бор, и уничтожают их, не повреждая при этом здоровые ткани в отличие от радиотерапии. Данная терапия показала очень высокий процент полного выздоровления в лечении опухолей, составляющий 73,3 % даже на запущенной стадии. Учёным новосибирского Института ядерной физики имени Г. И. Будкера СО РАН удалось уничтожить 99 % опухолевых клеток в ходе эксперимента по лечению рака с помощью ускорителя для бор-нейтронозахватной терапии[12].
- Иммунотерапия. Иммунная система стремится уничтожить опухоль. Однако она в силу ряда причин часто не в состоянии это сделать. Иммунотерапия помогает иммунной системе бороться с опухолью, заставляя её атаковать опухоль эффективнее или делая опухоль более чувствительной. Противораковая вакцина Вильяма Коли, а также вариант данной вакцины — пицибанил, являются эффективными при лечении некоторых форм новообразований благодаря стимулированию активности натуральных киллеров и выработке ряда цитокинов, таких как фактор некроза опухоли и интерлейкин-12[13][14]. Для активации защитных иммунных механизмов может применяться эпигенетическая терапия[15][16][17][18].
- Фотодинамическая терапия — в основе лежит применение фотосенсибилизаторов, которые избирательно накапливаются в клетках опухоли и повышающих её чувствительность к свету. Под действием световых волн определённой длины эти вещества вступают в фотохимическую реакцию, что приводит к образованию активных форм кислорода, который действует против клеток опухоли[19].
На данный момент наиболее хорошие результаты в лечении рака наблюдаются при использовании комбинированных методов лечения (хирургического, лучевого и химиотерапевтического)[20].
Перспективным направлением в лечении являются методы локального воздействия на опухоли, такие как химиоэмболизация.
В июне 2016 года газета Australian сообщила, что международная группа учёных «близка к разработке универсальной вакцины против рака». Препарат, о котором идёт речь, будет эффективным в отношении всех раковых заболеваний. По словам Угура Сахина, директора института изучения онкологических заболеваний Майнцского университета имени Иоганна Гутенберга, учёным впервые удалось создать внутривенную вакцину с использованием наночастиц. Он также рассказал, что она имеет не превентивный, а «терапевтический характер», и призвана не предотвращать раковые заболевания, а использоваться при их лечении. По его словам, вакцина уже прошла «обнадёживающие тесты» на мышах и нескольких людях, больных меланомой. Однако окончательные результаты её воздействия на этих больных людях будут известны примерно через год. После этого исследователи планируют провести более масштабные тесты на больных людях. Угур Сахин предположил, что препарат будет разрешён к применению «примерно через 5 лет»[21].
В августе 2018 года австралийские учёные разработали вещество, воздействующие на белки KAT6A и KAT6B, способствующие развитию раковой опухоли. Клинические исследования показали, что новое вещество лишает раковые клетки возможности начинать клеточный цикл. Участник исследования профессор Энн Восс уточнил, что ингибитор приводит клетки рака к старению, и они теряют способность к делению и размножению. Лабораторные тесты на мышах с раком крови показали, что вещество увеличило продолжительность жизни животных в 4 раза, а также предотвратило рост и распространение злокачественных опухолей. ДНК-тест выявил, что ингибитор никак не повлиял на здоровые клетки организма. На основе полученных данных учёные начали разработку лекарственного препарата, способного «усыплять» раковые клетки[22][23].
В мае 2024 года в Великобритании начались испытания первой в мире индивидуальной вакцины от рака. Британская национальная служба здравоохранения заявила, что первыми вакцину испытают пациенты с раком легких, прямой кишки, мочевого пузыря, кожи, почек и поджелудочной железы. Затем программу расширят и на пациентов, страдающих от других форм этого заболевания[24].
Прогноз
Прогноз для больных раком зависит от множества факторов: своевременное обнаружение опухоли, её локализация, стадия развития, уровня медицинского обслуживания в стране (регионе) и т. д. Выявление рака на ранних стадиях развития, как правило, ведёт к полному выздоровлению больного под действием адекватного лечения. Наличие распространённых метастазов, как правило, определяет неблагоприятный прогноз.
См. также
Примечания