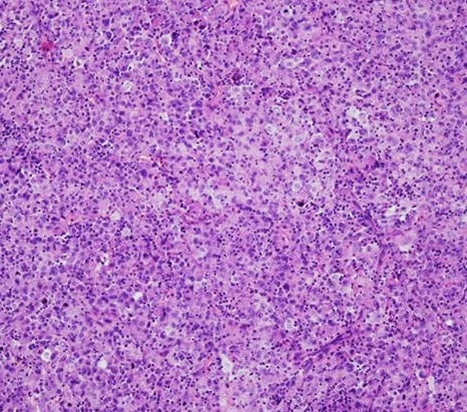
Аденокарцинома лёгкого
Аде́нокарцинома лёгкого — злокачественная опухоль, берущая начало из клеток железистого эпителия, который выстилает слизистую бронхов, продуцирующих бронхиальный секрет[1]. Аденокарцинома лёгкого представляет собой один из основных подтипов немелкоклеточного рака лёгких (НМРЛ), который является наиболее распространённым типом рака лёгкого[2].
Что важно знать
| Аденокарцинома лёгкого | |
|---|---|
| МКБ-11 | 2C25.0 |
| MeSH | D000077192 |
Классификация по TNM
- Ts — неинвазивная аденокарцинома.
- T1 — диаметр ≤3 см, окружённая лёгочной или висцеральной плеврой и без бронхоскопических признаков инвазии в главный бронх.
- T1mi — минимально инвазивная аденокарцинома:
- T1a — диаметр ≤1 см,
- T1b — диаметр >1 см, но ≤2 см,
- T1c — диаметр >2 см, но ≤3 см.
- T2 — диаметр >3 см, но ≤5 см или наличие любой из следующих характеристик: поражение главного бронха без вовлечения киля трахеи, инвазия в висцеральную плевру, ателектаз или обструктивный пневмонит, который распространяется на область ворот лёгкого, захватывая часть или все лёгкое.
- T2a — диаметр >3 см, но ≤4 см.
- T2b — диаметр >4 см, но ≤5 см в наибольшем измерении.
- T3 — диаметр >5 см, но ≤7 см или инвазия в париетальную плевру, грудную стенку, диафрагмальный нерв или париетальный перикард, или отдельные опухолевые узлы в той же доле, что и первичная опухоль.
- T4 — диаметр >7 см или инвазия в диафрагму, средостение, сердце, крупные сосуды, трахею, возвратный гортанный нерв, пищевод, тело позвонка или киль трахеи, или отдельные опухолевые узлы в другой доле того же лёгкого[3].
Этиология
Факторы риска:
- курение;
- вдыхание асбеста, кремния, радона, тяжёлых металлов и паров дизельного топлива;
- работа в угольных шахтах, рыболовство, строительство;
- семейный анамнез рака лёгкого;
- мутации гена p53[4][5].
Однако аденокарцинома является преобладающим видом рака и среди никогда не куривших. Кроме того, 84,9 % сельских и 76,1 % городских женщин, которые никогда не курили, подтвердили воздействии загрязнённого воздуха внутри помещений (пассивное курение, топливо для приготовления пищи)[5]. Пассивное курение повышает риск развития РЛ на 20-30 %[6].
Патогенез
Аденокарцинома возникает из альвеолярных клеток, расположенных в эпителии мелких дыхательных путей; экспрессирует иммуногистохимические маркеры, тиреоидный фактор транскрипции 1 и напсин А, цитокератин 5, цитокератин 6, белок p40 и десмоглеин 3[2]. Опухоль прорастает в плевру, диафрагму, перикард, бронхи, средостение, крупные сосуды, трахею, пищевод, позвоночник или соседнюю долю лёгкого. Метастазы сначала возникают в перибронхиальных лимфатических узлах, затем в средостенных или субкаринальных узлах, в последнюю очередь в другом лёгком. Отдалённые метастазы возникают в противоположной доле лёгкого и плевральных узелках, головном мозге, костях или печени. Аденокарцинома приводит к злокачественному плевральному или перикардиальному выпоту[4].
Эпидемиология
В России в 2019 году выявлено 49 145 новых случаев рака лёгкого. С 2009 по 2019 год отмечался рост заболеваемости с 83,6 до 100,5 случаев на 100 тыс. населения. При этом показатель летальности снизился с 54,1 до 48,4 случаев на 100 тыс. населения[6]. Встречаемость аденокарциномы 15-20 %. Это наиболее распространённый тип немелкоклеточного рака лёгкого (примерно 40 % случаев)[2] и преобладающий вид рака у некурящих[5]. У женщин аденокарцинома встречается чаще, а показатель пятилетней выживаемости выше, чем у мужчин[5].
Диагностика
Выраженность симптомов зависит от формы, локализации, размеров и типа роста опухоли, наличия метастазов. Возможно бессимптомное течение, при котором опухоль становится случайной рентгенологической находкой. Главные симптомы:
- сухой надсадный кашель;
- кровохарканье;
- одышка;
- боль в грудной клетке;
- синдром Панкоста — боль в плечевом суставе и плече, атрофия мышц предплечья, синдром Горнера;
- синдром сдавления верхней полой вены — цианоз и отёк лица, шеи, верхних конечностей, развитые подкожные венозные коллатерали на туловище.
Возможны тромбофлебит, нейро- и миопатии, дерматозы, нарушениями жирового и липидного обмена, артралгические и ревматоидноподобные состояния.
- Бронхоскопия с биопсией
- Компьютерная томография органов грудной клетки и брюшной полости
- Позитронная эмиссионная томография, совмещённая с компьютерной томографией
- Спирометрия
- Остеосцинтиграфия
- Эндобронхиальное или эндоскопическое ультразвуковое исследование региональных лимфатических узлов
- Магнитно-резонансная томография головного мозга[3]
- Гистологическое или цитологическое[7] исследование биоптата
- Клинический анализ крови
- Исследование печёночных ферментов и функции почек
- Определение концентрации лиганда запрограммированной смерти 1[3]
Дифференциальная диагностика
Осложнения
- Метастазы в кости и головной мозг
- Дыхательная недостаточность
- Лёгочное кровотечение
- Тромбофлебит
- Нейропатия
- Опухолевый плеврит
- Пневмония[6]
Лечение
Хирургическое удаление доли или всего лёгкого — основа лечения, особенно на начальных стадиях опухоли. Химиотерапия — цисплатин в комбинации с гемцитабином, доцетакселом или пеметрекседом — рекомендована при вовлечении висцеральной плевры, сосудистой инвазии или низкой степень дифференцировки клеток опухоли. Лучевую терапию выполняют при невозможности хирургического лечения отдельно или в комбинации с химиотерапией комбинации. Ведутся исследования иммунотерапевтических методов для лечения ранних стадий аденокарциномы[3][7].
Прогноз
При полноценном предоперационном обследовании доля пациентов, у которых интраоперационно процесс признаётся нерезектабельным, не превышает 5-10 %. Радикальную операцию удаётся выполнить только у 10-20 % всех заболевших. При всех формах рака лёгкого 5-летняя выживаемость составляет 20-25 %[7].
Диспансерное наблюдение
После лечения пациентов наблюдают для выявления рецидива опухоли. Каждые 3 месяца в течение первых 3 лет и каждые 6 месяцев в течение 4 и 5 годов выполняют ультразвуковое исследование и рентгенографию грудной клетки или компьютерную томографию. Магнитно-резонансную томографию головного мозга и остеосцинтиграфию проводят 1 раз в год. По истечении 5 лет после операции обследование проходят раз в год[6].
Профилактика
Отказ от курения, избегание пассивного курения, защита дыхательных путей во время работы с канцерогенами[6].
Скрининг с помощью низкодозовой компьютерной томографии показал многообещающие результаты — снижение смертности от рака лёгких у лиц с высоким риском (курильщиков в возрасте 55-74 лет со стажем курения ≥30 лет или ≤15 лет с момента прекращения курения). Внедрению в широкую практику препятствуют спорные вопросы об определении групп риска, интервале между скринингами, возрасте прекращения скрининга, методе компьютерной томографии, экономической эффективности и частоте ложноположительных диагнозов. Периодическая рентгенография грудной клетки, цитология мокроты или анализ биомаркеров не рекомендуются для скрининга[3].
Примечания
Ссылки
- Рак лёгкого
- Сложности диагностики аденокарциномы лёгкого (клинический случай) Коханова Н. Б.
- Комплексная морфологическая диагностика аденокарциномы лёгкого. Наблюдение из практики
- Литература по теме в базе данных PubMed
- Fishman, Jay A. Fishman's pulmonary diseases and disorders / Jay A. Fishman, Robert Kotloff, Michael A. Grippi … [и др.]. — McGraw-Hill Education, 2015-04-14. — ISBN 9780071807289.