Псевдомембранозный колит
Псевдомембрано́зный коли́т (ПМК, псевдомембрано́зный энтероколи́т) — заболевание толстой кишки, характеризующееся воспалением и повышенным образованием бело-жёлтых бляшек, в совокупности представляющих собой псевдомембрану на поверхности слизистой оболочки кишечника[1][2]. Как правило, вызывается спорообразующей анаэробной бактерией Clostridium difficile, однако может возникать и по другим причинам[3].
Общие сведения
Эпидемиология
От 10 до 25 % всех случаев антибиотик-ассоциированной диареи обусловлены инфекцией C. dificile. Частота заболеваемости колеблется от 5 до 30 % в зависимости от используемого антибиотика. Заболеваемость диареей, вызванной С. Difficile, среди населения составляет от 7 до 18 на 100 000 человек[4].
Факторы риска
Факторы риска развития заболевания могут быть обусловлены состоянием пациента, возможностями инфицирования спорами C. difficile и нарушением кишечного микробиома.
Доказанные факторы риска развития:
- возраст >65 лет;
- сопутствующая патология (воспалительные заболевания кишечника, ВИЧ, сахарный диабет и др.);
- пациенты с язвенным колитом и болезнью Крона при обострении болезни без очевидных причин, после проведённого курса антибиотикотерапии или пребывания в стационаре;
- хирургические вмешательства на органах ЖКТ;
- энтеральное питание;
- снижение кислотности желудочного сока (при приёме ингибиторов протонной помпы);
- приём иммуносупрессивных и противоопухолевых препаратов[5].
Этиология
Причиной ПМК является нерациональное применение антибиотиков, приводящее к избыточному размножению определённого условно-патогенной бактерии — Cl. difficile.
Хотя этиологически Cl. difficile является наиболее частой причиной заболевания, до эры антибиотиков заболевания часто ассоциировалось с ишемической болезнью, обструкцией, сепсисом, уремией и отравлением тяжёлыми металлами[3].
Помимо C. difficile, из числа бактерий заболевание могут вызывать Clostridium ramosum, Escherichia coli O157:H7, Klebsiella oxytoca, Plesiomonas shigelloides, Salmonella enterica, шигеллы, золотистый стафилококк и Yersinia enterocolitica[6]. Из числа вирусных возбудителей заболевание может вызывать цитомегаловирус[6], однако у людей без нарушений работы иммунной системы колиты, вызванные цитомегаловирусом, встречаются редко[7]. Также заболевание могут вызывать несколько паразитов: дизентерийная амёба, Schistosoma mansoni и угрица кишечная[6]. В случае с Schistosoma mansoni под наибольшей угрозой находятся люди с нарушениями работы иммунной системы[8].
Патогенез
Заболевание начинается с нарушения нормальной микрофлоры кишечника, что приводит к колонизации C. difficile после приёма антибиотиков, хотя инфекция также может развиться в результате приёма химиотерапевтических и иммуносупрессивных препаратов. После первичной колонизации бактерии вырабатывают токсины, которые являются причиной появления клинической картины заболевания[9].
Патогенные свойства проявляют бактерии, способные продуцировать токсины: токсин А, токсин В, бинарный токсин. Эти токсины обладают синергичным действием, разрушают межклеточные контакты и lamina propria слизистой оболочки, способствуют дезорганизации цитоскелета клеток, выработке провоспалительных медиаторов колоноцитами, макрофагами, дендритными и тучными клетками с последующей инфильтрацией слизистой оболочки нейтрофилами, которые проникают в просвет толстой кишки.
- Токсин А (энтеротоксин) повреждает межклеточные контакты и lamina propria слизистой оболочки.
- Токсин В (цитотоксин) обладает цитотоксическим действием, проявляющимся в деполимеризации актиновых нитей цитоскелета, нарушении внутриклеточной передачи сигналов, блокировании клеточного цикла и активации продукции активных форм кислорода.
- Бинарный токсин также имеет выраженные цитотоксические свойства, включая адгезию бактерий к эпителию слизистой оболочки через липолиз-стимулируемые липопротеиновые рецепторы и разрушение нитей актина.
Воспалительные изменения в слизистой оболочке толстой кишки, вызванные воздействием токсинов, включают повышение проницаемости кишечной и сосудистой стенок, секрецию жидкости в просвет кишечника, образование псевдомембран из нейтрофилов, погибших клеток эпителия и нитей фибрина. Эти изменения способствуют развитию эндотоксемии и системного воспалительного ответа[10] .
Патоморфология
Патоморфологические изменения у большинства пациентов локализуются в прямой кишке и левых отделах ободочной кишки, у 20 % наблюдается тотальное поражение толстой кишки. Воспалительный процесс может затрагивать слизистую оболочку тонкой кишки.
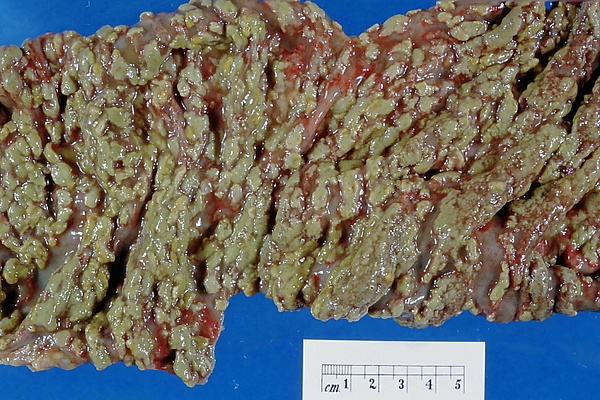
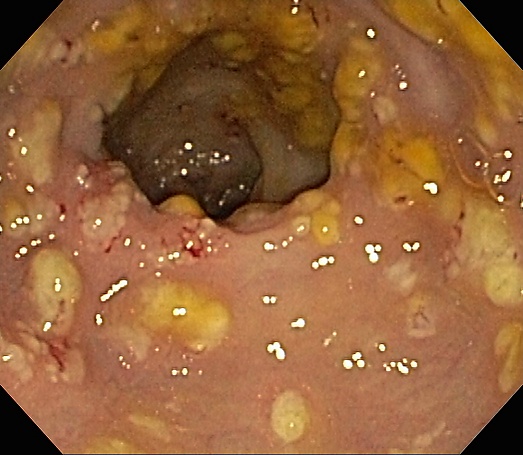
Эндоскопическая картина воспаления толстой кишки, ассоциированного с C. difficile, проявляется гиперемией и отёком слизистой оболочки, а также характерными фибринозными плёнками. Они покрывают участки некроза слизистой оболочки и представляют собой серовато-жёлтые бляшки от 0,5 до 2,0 см диаметром, слегка возвышающиеся над поверхностью.
Гистологическое исследование подтверждает наличие некроза эпителия с фибриновым налётом, нейтрофильным инфильтратом и глубокими язвами слизистой оболочки с формированием псевдомембран[11].
Классификация
По течению заболевания:
- лёгкая форма: диарея и незначительная боль в животе;
- среднетяжёлая форма: диарея, боль в животе и повышение температуры тела до 38 градусов;
- тяжёлая форма: диарея, боли в животе спастического характера, лихорадка вплоть до гектических значений, лейкоцитоз выше 15×109/л, гипоальбуминемия менее 30 г/л. Отсутствие диареи может свидетельствовать о развитии молниеносной формы заболевания[12];
- осложнённое течение: кровавая диарея в сочетании с одним из признаков (артериальная гипотензия, лихорадка более 38,5 градуса, кишечная непроходимость, нарушение сознания, лейкоцитоз более 35х109/л или менее 2х109/л, полиорганная недостаточность);
Клиническая картина
Клинические проявления вариабельны. Пациенты могут быть бессимптомными носителями или переносить молниеносный ПМК с токсическим мегаколоном[13].
К типичным проявлениям ПМК относят диарею, боли в животе, которые усиливаются перед дефекацией, могут быть тенезмы, субфебрильную температуру, признаки интоксикации — слабость, тошнота, рвота. Частота стула достигает 10 раз в сутки, при тяжёлых формах до 20—30 раз. Диарея носит упорный характер, и при отсутствии лечения у пациентов быстро развиваются водно-электролитные нарушения. Нередко регистрируют лейкоцитоз и гипоальбуминемию. При объективном исследовании живот умеренно вздут, отмечается болезненность при пальпации по ходу толстой кишки[14].
Лёгкие формы ПМК часто остаются недиагностированными. При тяжёлом течении наблюдаются спутанность сознания, гектическая лихорадка, вентиляционные нарушения, выраженный лейкоцитоз и значительные электролитные расстройства, гипотензия, энтеропатия с потерей белка[13]. У пациентов с таким вариантом течения заболевания может развиваться токсическая дилатация толстой кишки при отсутствии диареи[14].
Рецидивы отмечаются примерно в 20 % случаев вследствие неполной санации кишечника от спор или повторного заражения[14].
Диагностика
- Клинический анализ крови для выявления анемии, лейкоцитоза, высокой СОЭ;
- Биохимический анализ крови для выявления гипопротеинемии и повышения маркёров воспаления (С-реактивный белок, прокальцитонин);
- Копрологическое исследование для определения лейкоцитов, скрытой крови и эритроцитов;
- Бактериологический посев кала для исключения патогенной флоры и определения условно патогенной;
- Определение глутаматдегидрогеназы методом ИФА в образцах просветных фекалий подтверждает наличие C. difficile, но фермент продуцируется токсигенными и нетоксигенными штаммами[14];
- Определение в кале токсинов А и В C. difficile методом ИФА для подтверждения наличия токсин продуцирующих бактерий[11];
- Определение ДНК C. difficile в кале методом полимеразной цепной реакции;
- Гистологическое исследование биоптата кишки. Характерны скопления фибрина и нейтрофилов между криптами, а затем и на их поверхности[11].
- УЗИ органов брюшной полости используют для определения утолщения стенок кишки из-за отёка, газа и выпота в брюшной полости;
- Колоноскопия позволяет визуализировать протяжённость и выраженность воспаления толстой кишки, псевдомембраны, язвы;
- КТ брюшной полости и/или КТ-энтерография позволяет выявить воспаление, определить толщину стенки кишки, выявить осложнения;
- Рентгенография органов брюшной полости для визуализации признаков кишечной непроходимости, перфорации кишечника и токсического мегаколона[11].
Дифференциальная диагностика
- Дивертикулярная болезнь толстой кишки с дивертикулитом;
- Язвенный колит;
- Болезнь Крона;
- Туберкулёз кишечника;
- Ишемический колит;
- Инфекционный гастроэнтерит: сальмонеллёз, шигеллёз, иерсиниоз, диарея путешественников;
- Гастроэнтероколиты, ассоциированные с астровирусом, норовирусом, ротавирусом, энтеровирусом, герпесвирусами[13][11].
Лечение
Пациенты с клиническими формами инфекции подлежат контактной изоляции с проведением текущей и заключительной дезинфекции[11].
Необходимо отменить приём антибиотика, спровоцировавшего развитие ПМК. Этиотропная терапия заключается в назначении антибактериальных средств, к которым чувствителен C. difficile. Это ванкомицин, метронидазол, фидаксомицин[14].
При лёгком течении препаратом выбора является метронидазол в течение 7—10 дней. В тяжёлых случаях, когда пероральный приём затруднён, метронидазол можно назначать внутривенно. У больных с тяжёлым течением заболевания используют ванкомицин. Он плохо всасывается в кишечнике, что позволяет создать высокие концентрации препарата в просвете толстой кишки и избежать развития побочных эффектов при длительном применении[14].
Для лечения первого рецидива ПМК рекомендуется использовать ванкомицин. При развитии второго и последующих рецидивов ванкомицин назначают на 5—7-й неделе с постепенным снижением дозы и кратности приёма. Такой режим позволяет спорам C. difficile перейти в вегетативную форму, которая чувствительна к ванкомицину[14].
В рандомизированных испытаниях безлотоксумаб, представляющий собой моноклональные антитела, показал себя эффективным по сравнению с плацебо в предотвращении повторной инфекции C. difficile, снижая вероятность её появления[15].
При развитии множественных рецидивов ПМК возможно применение трансплантации кишечной микробиоты (англ. fecal microbiota transplantation). Фекальные трансплантации безопасны и высокоэффективным методом лечения рецидивирующей инфекции, но такое лечение можно проводить только в специализированных центрах с опытом подбора доноров[14].
Крайне важна патогенетическая терапия, особенно у больных тяжёлыми формами заболевания. Основные её направления — коррекция водно-электролитных расстройств и белкового обмена, восстановление нормального состава кишечной микрофлоры, связывание токсина C. difficile.
Пациентам с ПМК назначается частое, дробное и щадящее питание. При этом из рациона нужно исключить продукты, содержащие лактозу, сырые овощи и фрукты, цитрусовые, алкоголь и кофе. Мясо, рыбу и яйца можно употреблять в термически обработанном виде[11].
При молниеносном течении ПМК или развитии осложнений показана тотальная или субтотальная колэктомия[14].
Прогноз
Прогноз благоприятный при своевременном лечении[16].
Профилактика
Профилактика заболевания заключается в рациональном применении антибиотиков, сокращении сроков госпитализации, особенно у лиц старше 65 лет[5].
Примечания
Литература
- Немцов Л. М. Псевдомембранозный колит как мультидисциплинарная проблема // Вестник Витебского государственного медицинского университета. — 2014. — № 3.
- Priya D. Farooq, Nathalie H. Urrunaga, Derek M. Tang, Erik C. von Rosenvinge. Pseudomembranous Colitis : [англ.] // Disease-a-month : DM. — 2015. — Vol. 61, no. 5 (May). — P. 181–206. — ISSN 0011-5029. — doi:10.1016/j.disamonth.2015.01.006. — PMID 25769243. — PMC 4402243.