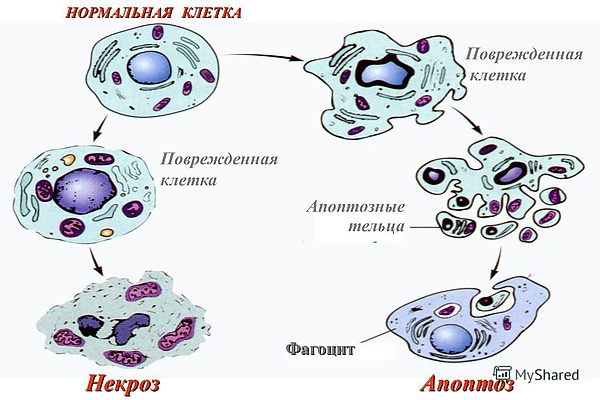
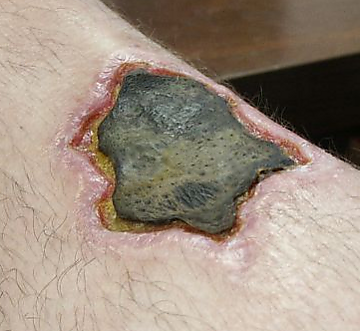
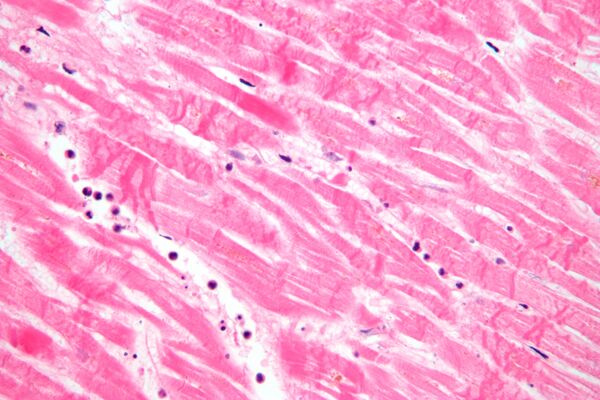
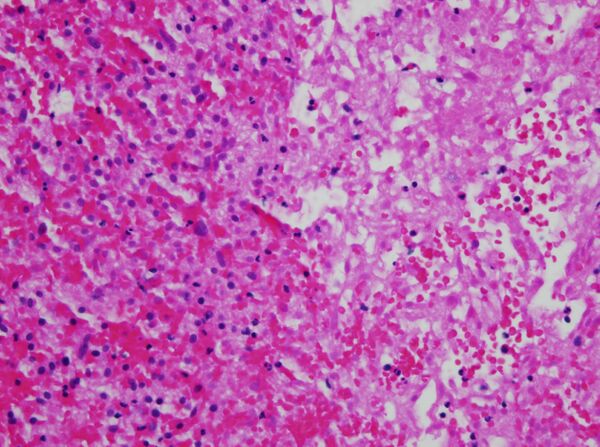
Некроз
Некроз (от древнегреческого νέκρωσις, некрозис, «смерть») — повреждение клетки, которое приводит к их преждевременной гибели в живой ткани путем аутолиза.[1]
Некроз является результатом воздействия внешних факторов на клетку или ткань, такими как инфекция или травма, которые пагубно влияют на жизнедеятельность клеток. Напротив, апоптоз — это естественно запрограммированная и целенаправленная причина смерти клетки. В то время как апоптоз часто оказывает благотворное воздействие на организм, некроз почти всегда вреден и может привести к летальному исходу.[2]
Клеточная гибель вследствие некроза не следует по пути апоптотической трансдукции сигнала, но при этом активируются различные рецепторы, что приводит к потере целостности клеточной мембраны[3] и неконтролируемому высвобождению продуктов клеточной гибели во внеклеточное пространство.[1] Это инициирует в окружающих тканях воспалительную реакцию, которая привлекает лейкоциты и близлежащие фагоциты, которые устраняют мертвые клетки путем фагоцитоза. Однако вредные микробные вещества, высвобождаемые лейкоцитами, создают сопутствующие повреждения окружающих тканей.[4] Это избыточное сопутствующее повреждение тормозит процесс заживления. Таким образом, необработанный некроз приводит к накоплению разлагающейся мертвой ткани и остатков клеток в месте или вблизи места гибели клеток. Классический пример — гангрена. По этой причине часто приходится удалять омертвевшие ткани хирургическим путем — процедура, известная как санация.
Классификация
Структурные признаки, указывающие на необратимое повреждение клеток и прогрессирование некроза выражаются в виде плотной массы и прогрессирующего разрушения генетического материала, а также разрушения мембран клеток и органелл.[5]
Существует шесть отличительных морфологических паттернов некроза: [6]
- Коагуляционный некроз характеризуется образованием студенистого (гелеобразного) вещества в мёртвых тканях, в которых сохраняется архитектура ткани,[6] и может наблюдаться с помощью световой микроскопии. Коагуляция происходит в результате денатурации белка, в результате чего Альбумин превращается в твёрдое и непрозрачное состояние.[5] Этот паттерн некроза обычно наблюдается в гипоксических (низкокислородных) средах, таких как инфаркт. Коагуляционный некроз возникает преимущественно в таких тканях, как почки, сердце и надпочечники.[5] Тяжёлая ишемия чаще всего вызывает некроз этой формы.[7]
- Колликвационный некроз (или разжижающий некроз), в отличие от коагуляционного некроза, характеризуется разложением мёртвых клеток с образованием вязкой жидкой массы.[6] Это типично для бактериальных, а иногда и грибковых инфекций из-за их способности стимулировать воспалительную реакцию. Некротическая жидкая масса часто кремово-желтого цвета из-за присутствия мёртвых лейкоцитов и обычно известна как гной.[6] Гипоксические инфаркты в головном мозге представляют собой этот тип некроза, потому что мозг содержит мало соединительной ткани, но большое количество пищеварительных ферментов и липидов, и поэтому клетки могут быть легко перевариваемы их собственными ферментами.[5]
- Гангренозный некроз можно считать разновидностью коагуляционного некроза, напоминающего мумифицированную ткань. Это характерно для ишемии нижних конечностей и желудочно-кишечного тракта. Если происходит наложение инфекции на мертвые ткани, то возникает разжижающий некроз (влажная гангрена).[8]
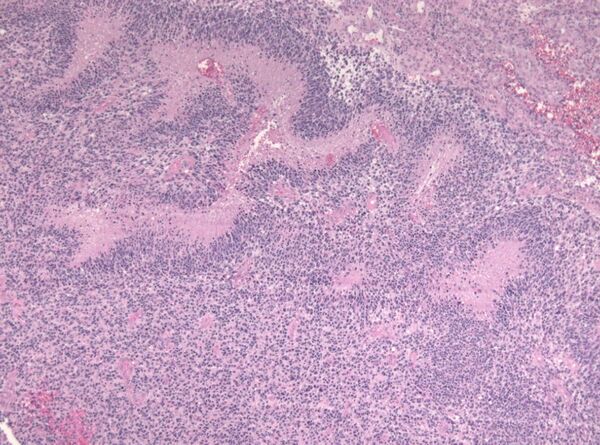
- Казеозный некроз можно рассматривать как комбинацию коагуляционного и разжижающего некроза[5], обычно вызываемого микобактериями (например, туберкулезом), грибами и некоторыми инородными веществами. Некротическая ткань выглядит белой и рыхлой, как комковатый сыр. Мёртвые клетки распадаются, но не разлагаются полностью, оставляя гранулированные частицы.[5] Микроскопическое исследование показывает аморфные зернистые остатки, заключённые в характерный воспалительный мешочек. [6] Некоторые гранулемы содержат этот паттерн некроза.[9]
- Жировой некроз — это некроз исключительно жировой ткани,[9] возникающий в результате действия активированных липаз на жировые ткани, такие как поджелудочная железа. В поджелудочной железе это приводит к острому панкреатиту, состоянию, при котором панкреатические ферменты просачиваются в брюшную полость и разжижают мембрану, расщепляя сложные эфиры триглицеридов на жирные кислоты путём омыления жира.[6] Кальций, магний или натрий могут связываться с этими повреждениями, образуя мелово-белое вещество.[5] Отложения кальция микроскопически различимы и могут быть достаточно большими, чтобы быть видимыми при рентгенографическом исследовании.[7] Невооружённым глазом отложения кальция кажутся зернистыми белыми пятнами.[7]
- Фибриноидный некроз — это особая форма некроза, обычно вызываемая иммунно-опосредованным повреждением сосудов. Он маркируется комплексами антигена и антител, называемых иммунными комплексами, депонированными в стенках артерий[6] вместе с фибрином.[6]
- Существуют также очень специфические формы некроза, такие как гангрена (термин, используемый в клинической практике для конечностей, перенёсших тяжёлую гипоксию), гумматозный некроз (из-за спирохетальных инфекций) и геморрагический некроз (из-за закупорки венозного дренажа органа или ткани).
- Некоторые укусы пауков могут привести к некрозу. В Соединённых Штатах только укусы пауков от коричневого паука-отшельника (род Loxosceles) достоверно прогрессируют до некроза. В других странах пауки того же рода, такие как чилийский паук-отшельник в Южной Америке, также вызывают некроз. Утверждения о том, что желтосумный колющий паук и пауки-бродяги обладают некротическим ядом, не были подтверждены.
- У слепых кротовых крыс (род слепыши) процесс некроза заменяет роль систематического апоптоза, обычно используемого во многих организмах. Низкие кислородные условия как в норах слепых кротов, обычно вызывают апоптоз клеток. В процессе адаптации к более высокой склонности к гибели клеток слепые кротовые крысы развили мутацию в белке-супрессоре опухоли p53 (который также есть у людей), чтобы предотвратить апоптоз клеток. Люди, страдающие раком, имеют сходные мутации, и считалось, что слепые кротовые крысы более восприимчивы к раку, потому что их клетки не могут подвергаться апоптозу. Однако через определённое время (в течение 3 дней, согласно исследованию, проведённому в Университете Рочестера) клетки слепых кротовых крыс высвобождают интерферон бету (который иммунная система обычно использует для борьбы с вирусами) в ответ на чрезмерную пролиферацию клеток, вызванную подавлением апоптоза. В этом случае интерферон-бета вызывает некроз клеток, и этот механизм также убивает раковые клетки у слепых кротовых крыс. Из-за таких механизмов подавления опухоли слепые кротовые крысы и другие слепышовые устойчивы к раку.[10][11]
Причины
Некроз может возникнуть из-за внешних или внутренних факторов.
Внешними факторами могут быть механическая травма (физическое повреждение организма, которое вызывает разрушение клеток), повреждение кровеносных сосудов (которое может нарушить кровоснабжение ассоциированных тканей) и ишемия.[12] Термическое воздействие (чрезвычайно высокая или низкая температура) тоже может привести к некрозу из-за разрушения клеток.
При обморожении образуются кристаллы, повышающие давление оставшейся ткани и жидкости, вызывающие разрыв клеток.[12] В экстремальных условиях ткани и клетки погибают в результате неправильного процесса разрушения мембран и цитозоля.[13]
К внутренним факторам, вызывающим некроз, относятся: трофоневротические нарушения (заболевания, возникающие вследствие дефектного нервного действия в части органа, приводящего к нарушению питания); повреждение и паралич нервных клеток. Панкреатические ферменты (липазы) являются основной причиной жирового некроза. [12]
Некроз может быть активирован компонентами иммунной системы, такими как система комплемента, токсины бактерий, активные естественные киллеры и перитонеальные макрофаги.[1] Программа некроза, вызывающие патоген в клетках с иммунологическими барьерами (слизистая оболочка кишечника) могут смягчить их инвазию через поверхности, пораженные воспалением. [1] Токсины и патогены могут вызывать некроз; токсины, такие как змеиный яд, могут ингибировать ферменты и вызывать гибель клеток.[12] Некротические раны также появились в результате укусов Vespa mandarinia.[14]
Недостаточная секреция цитокинов вызывает патологические состояния. Оксид азота (NO) и активные формы кислорода (АФК) также влияют на интенсивную некротическую гибель клеток.[12] Классическим примером некротического состояния является ишемия, которая приводит к резкому истощению кислорода, глюкозы, и других причин дистрофии, и индуцирует массивную некротическую гибель эндотелиальных клеток и непролиферирующих клеток окружающих тканей (нейронов, кардиомиоцитов, почечных клеток и т. д.).[1] Последние цитологические данные свидетельствуют о том, что некротическая гибель происходит не только во время патологических событий, но и является составной частью какого-то физиологического процесса.[12]
Активационно-индуцированная гибель первичных Т-лимфоцитов и других важных составляющих иммунного ответа является каспазно-независимой и некротической по морфологии; следовательно, современные исследователи продемонстрировали, что некротическая гибель клеток может происходить не только во время патологических процессов, но и во время нормальных процессов, таких как обновление тканей, эмбриогенез и иммунный ответ.[12]
Патогенез
До недавнего времени некроз считался нерегулируемым процессом. Однако есть два масштабных пути, по которым в организме может произойти некроз.
Первый изначально связан с онкозом, при котором происходит отёк клеток. Затем поражённые клетки начинают появляться волдыри, и за этим следует пикноз, при котором происходит ядерная усадка. На заключительном этапе этого пути клеточные ядра растворяются в цитоплазме, что называется кариолизом.
Второй путь — это вторичная форма некроза, которая, как выясняется, возникает после апоптоза и почкования. При этих клеточных изменениях некроза ядро распадается на фрагменты (известные как кариорексис).[15]
Изменения ядра при некрозе и характеристики этого изменения определяются тем, каким образом его ДНК разрушается:
- Кариолизис: хроматин ядра исчезает из-за потери ДНК в результате деградации.
- Кариорексис: сморщенные фрагменты ядра до полного рассеивания.
- Пикноз: ядро сжимается, а хроматин конденсируется. [6]
Другие типичные клеточные изменения при некрозе включают:
- Гиперэозинофилия цитоплазмы на образцах с гематоксилином и эозином.[16] Он виден как более темное пятно цитоплазмы.
- При рассмотрении в электронный микроскоп клеточная мембрана выглядит прерывистой. Эта прерывистая мембрана вызвана появлением пузырьков на клетках и потерей микроворсинок.[6]
В более широком гистологическом масштабе псевдорозетки (ложные розетки) представляют собой гиперцеллюлярные зоны, которые обычно окружают некротическую ткань. Псевдорозеточный некроз указывает на агрессивную опухоль.[17]
Лечение
Существует много причин некроза, и как таковое лечение зависит от того, как возник некроз. Лечение некроза обычно включает в себя два различных процесса: как правило, первопричина некроза должна быть устранена до того, как можно будет заняться самой мёртвой тканью.
- Санация, относящаяся к удалению омертвевших тканей хирургическим или нехирургическим путём, является стандартной терапией при некрозе. В зависимости от тяжести некроза, может варьироваться от удаления небольших участков кожи до полной ампутации поражённых конечностей или органов. Химическое удаление омертвевшей ткани – это ещё один вариант, при котором ферментативные средства, классифицируемые как протеолитические, фибринолитические или коллагеназы, используются для воздействия на различные компоненты омертвевшей ткани.[18] В отдельных случаях для удаления некротических тканей и инфекции применяется специальная терапия личинками Lucilia sericata.[19]
- В случае ишемии, к которой относится инфаркт миокарда, ограничение кровоснабжения тканей вызывает гипоксию и образование активных форм кислорода (АФК), которые вступают в реакцию с белками и мембранами и повреждают их. Антиоксидантные процедуры могут быть применены для очистки АФК.[20]
- Раны, вызванные физическими агентами, включая физические травмы и химические ожоги, можно лечить антибиотиками и противовоспалительными препаратами для предотвращения бактериальной инфекции и воспаления. Сохранение раны чистой от инфекции также предотвращает некроз.
- Химические и токсические вещества (например, фармацевтические препараты, кислоты, основания) вступают в реакцию с кожей, что приводит к потере кожи и в конечном итоге к некрозу. Лечение включает в себя выявление и прекращение действия вредного агента с последующим лечением раны, включая профилактику инфекции и, возможно, использование иммуносупрессивной терапии, такие как противовоспалительные препараты или иммунодепрессанты.[21] На примере укуса змеи использование противоядия останавливает распространение токсинов, в то время как прием антибиотиков препятствует инфекции.[22]
- Даже после того, как первоначальная причина некроза будет остановлена, некротическая ткань останется в организме. Иммунный ответ организма на апоптоз, который включает автоматическое разрушение и переработку клеточного материала, не запускается некротической гибелью клеток из-за отключения апоптотического пути.[23]
В растениях
Если кальция недостаточно, пектин не может быть синтезирован, и поэтому клеточные стенки не могут быть связаны и, таким образом, препятствуя меристемам. Это приведёт к некрозу кончиков стеблей, корней и краёв листьев.[24] Например, некроз тканей может произойти у резуховидки таля из-за растительных патогенов.
Кактусы, такие как Сагуаро и Кардон в пустыне Сонора, регулярно испытывают образование некротических пятен; вид двукрылых, называемый Drosophila mettleri, обладает способностью детоксикации p450, позволяющая ему использовать экссудаты, выделяющиеся в этих пятнах, как для гнезда, так и для кормления личинок.