Гистиоцитарная саркома
Гистиоцита́рная сарко́ма (ГС; англ. histiocytic sarcoma) представляет собой редкое злокачественное новообразование, относящееся к опухолям кроветворной ткани. Заболевание характеризуется пролиферацией клеток, обладающих морфологическими и иммунофенотипическими свойствами зрелых тканевых гистиоцитов, при этом оно не ассоциировано с моноцитарным лейкозом. ГС может возникать как самостоятельное (спорадическое) заболевание, так и развиваться в ассоциации с другими гемобластозами. Описаны случаи её клональной связи с фолликулярной лимфомой, хроническим лимфолейкозом, острым лимфобластным лейкозом, которые могут возникать одновременно или последовательно. Также имеются данные о развитии ГС после миелодиспластического синдрома[1][2].
Общие сведения
История
Термин «гистиоцитарная саркома» был введён в 1970 году Мате и соавторами. При этом первоначальные описания данного заболевания основывались исключительно на гистологическом сходстве опухолевых клеток с макрофагами. Согласно классификации 2016 года Всемирная организация здравоохранения определяет гистиоцитарную саркому как злокачественное новообразование, обладающее морфологическими и иммунофенотипическими характеристиками зрелых тканевых гистиоцитов[3].
Классификация
Этиология
ГС представляет собой редкое новообразование гематопоэтического (кроветворного) происхождения, которое характеризуется пролиферацией злокачественных клеток, обладающих морфологическими и иммуногистохимическими признаками зрелых тканевых гистиоцитов. Этиология данного заболевания остаётся неизвестной[5].
Патогенез
Патогенез ГС изучен недостаточно. Установлена чёткая связь между различными гематологическими новообразованиями (особенно В-клеточного происхождения) и развитием ГС. Для объяснения этой трансформации предложены три основных механизма:
- трансдифференцировка, при которой В-клетки изменяют фенотип при сохранении генотипических особенностей;
- дедифференцировка, предполагающая возврат В-клеток к стадии ранних предшественников с последующей новой дифференцировкой (не подтверждена наблюдениями);
- и теория общего неопластического предшественника.
Наиболее вероятным и хорошо описанным патогенетическим механизмом считается трансдифференцировка, поскольку исследования демонстрируют наличие клональных перестроек генов иммуноглобулинов тяжёлой цепи и/или T-клеточного рецептора в случаях ГС, развившейся одновременно или после лимфопролиферативных заболеваний, что свидетельствует об общем клональном происхождении[6].
Дополнительным механизмом злокачественной трансформации считается активация пути RAS/RAF, о чём свидетельствует обнаружение мутации BRAF V600E при ГС. Кроме того, определённую роль в патогенезе играют нарушения в гене KMT2D, которые приводят к дисрегуляции хроматина[6].
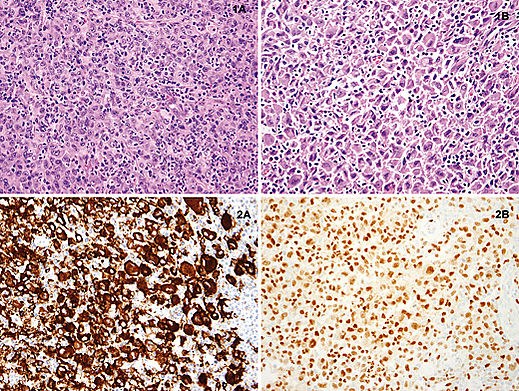
Гистологически ГС состоит из пластов крупных полигональных клеток с эпителиоидной морфологией, обильной эозинофильной, вакуолизированной или пенистой цитоплазмой, овальными или неправильной формы ядрами и вариабельно выраженными ядрышками. В части случаев могут наблюдаться фокальные участки со веретеновидными клетками. Митотическая активность и опухолевый некроз являются выраженными. Гемофагоцитоз может присутствовать, но часто бывает незначительным и маскируется выраженным воспалением. Гистологическая картина ГС в остальном не является специфичной и демонстрирует значительное морфологическое сходство с различными другими опухолевыми процессами[7].
Эпидемиология
ГС представляет собой крайне редкое заболевание, на долю которого приходится менее 1 % всех гемопоэтических и лимфоидных новообразований. Во всей мировой медицинской литературе описано лишь несколько сотен случаев данной патологии, зарегистрированных во всех возрастных группах, однако наиболее часто она встречается у пожилых пациентов. Согласно анализу 159 случаев ГС из базы данных американского реестра SEER, средний возраст пациентов на момент установления диагноза составляет 63 года при диапазоне от 1 до 96 лет. Не выявлено каких-либо досторверно известных экологических или наследственно-генетических факторов, которые могли бы предрасполагать к развитию этого заболевания[1][8].
Диагностика
Клинические проявления ГС отличаются значительным разнообразием и зависят от локализации поражённых органов. У большинства пациентов заболевание проявляется в виде унифокальных или мультифокальных экстранодальных новообразований, с наиболее частым поражением кишечника, кожи и мягких тканей. Для этой редкой опухоли не существует типичной локализации — в медицинской литературе описаны случаи вовлечения костной системы, лимфатических узлов, печени, селезёнки и лёгких. Изолированное поражение лимфатических узлов наблюдается менее чем в 20 % случаев[1].
Течение заболевания может быть бессимптомным, при этом опухоль нередко обнаруживается случайно во время плановых обследований или диагностических процедур, выполняемых по поводу других заболеваний. Однако чаще пациенты обращаются за медицинской помощью при появлении пальпируемого опухолевого образования, симптомов сдавления соседних органов (например, кишечной непроходимости) или системных проявлений, например, лихорадку и снижение массы тела. Кожные проявления заболевания отличаются особой вариабельностью и могут варьировать от малозаметных высыпаний до выраженных опухолевых узлов[1].
Первичное поражение центральной нервной системы относится к редким локализациям ГС. Заболевание может проявляться образованием одного или множественных солидных очагов в веществе головного мозга либо развитием лептоменингеального поражения. Случаи с вовлечением ЦНС характеризуются особенно агрессивным клиническим течением и неблагоприятным прогнозом. Могут наблюдаться различие симптомы (например, очаговая неврологическая симптоматика, головные боли, судороги и признаки внутричерепной гипертензии) в зависимости от локализации процесса[9].
Клинический анализ крови: возможно выявление панцитопении[1].
Гистологическое исследование биоптата костного мозга: характерен инфильтративный процесс с диффузным характером опухолевого роста, который сопровождается вытеснением нормальных элементов гемопоэза. Явления гемофагоцитоза при данном заболевании наблюдаются крайне редко[1].
Иммуногистохимическое исследование гистологического материала: большинство ГС экспрессируют CD68, CD163 и транскрипционный фактор PU.1. Часть случаев демонстрирует экспрессию CD31, цитоплазматического CD4 и CD45RO. Наиболее специфичным маркером гистиоцитарного происхождения является CD163, тогда как CD68 менее специфичен и может встречаться при других новообразованиях. Дополнительно может наблюдаться вариабельная экспрессия CD15, CD45, HLA-DR и фактора XIIIa[7].
Дифференциальная диагностика
Дифференциальная диагностика ГС проводится со следующими состояниями[7]:
- анапластическая крупноклеточная лимфома;
- крупноклеточная В-клеточная неходжкинская лимфома;
- лимфома Ходжкина;
- низкодифференцированная или недифференцированная карцинома;
- меланома;
- эпителиоидная ангиосаркома;
- эпителиоидная саркома;
- плеоморфная рабдомиосаркома;
- неклассифицированная плеоморфная саркома;
- саркома фолликулярных дендритных клеток;
- лангергансоклеточный гистиоцитоз;
- саркома из клеток Лангерганса;
- саркома из интердигитирующих дендритных клеток;
- миелоидная саркома;
- болезнь Эрдгейма — Честера;
- ювенильная ксантогранулёма;
- болезнь Розаи — Дорфмана.
Осложнения
В зависимости от локализации при ГС могут развиться следующие осложнения: перфорация полого органа, внутрибрюшное кровотечение, желудочно-кишечное кровотечение, обструкция полого органа с развитием непроходимости[1].
Лечение
Для пациентов с мультисистемной ГС методом выбора является полихимиотерапия. Поскольку оптимальная схема лечения не установлена, большинство клиницистов применяют протоколы, разработанные для агрессивных лимфом[1].
Хирургическое вмешательство при распространённых формах заболевания имеет ограниченное значение и применяется преимущественно для диагностической биопсии или лечения осложнений. Роль адъювантной лучевой терапии при мультисистемном поражении остаётся недоказанной и не рекомендуется для рутинного применения[1].
Прогноз
ГС характеризуется агрессивным течением. При проведении лечения общая выживаемость пациентов, как правило, не превышает двух лет. Без соответствующей терапии продолжительность жизни измеряется месяцами. Согласно исследованию, анализировавшему 330 случаев заболевания, медиана общей выживаемости для всей когорты составила 6 месяцев. Были выявлены потенциальные прогностические факторы, влияющие на исход заболевания: возраст пациента, локализация опухоли, наличие сопутствующих заболеваний и характер полученного лечения[6].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Гурьева О.Д., Валиев Т.Т., Павловская А.И. Гистиоцитарные опухоли: современные аспекты патогенеза, классификации, диагностики и лечения // Онкогематология : Журнал. — 2022. — № 1.
- Yamada R., Komohara Y. Histiocytic neoplasms: a brief review and differential diagnosis (англ.) // J Clin Exp Hematop : Журнал. — 2024. — Vol. 64, no. 3. — P. 156—165. — doi:10.3960/jslrt.24031.