Гнойный гидраденит
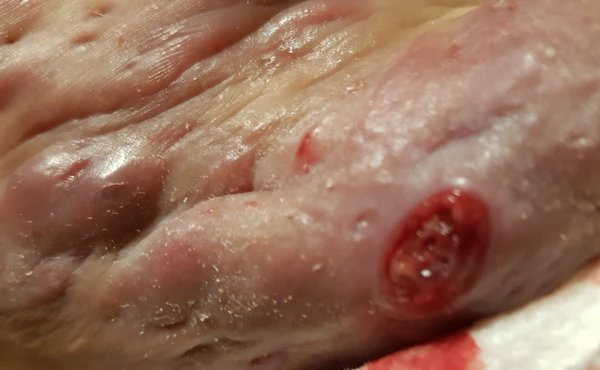
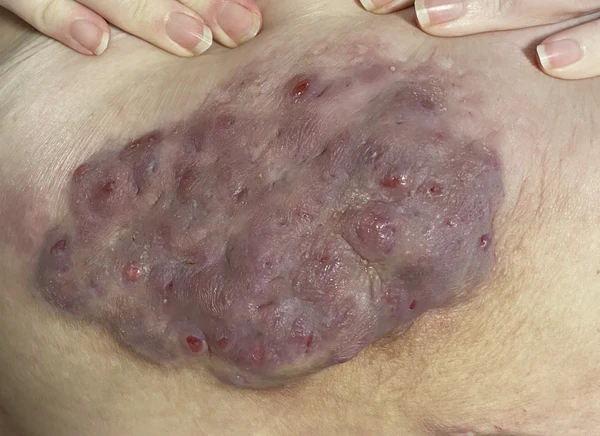
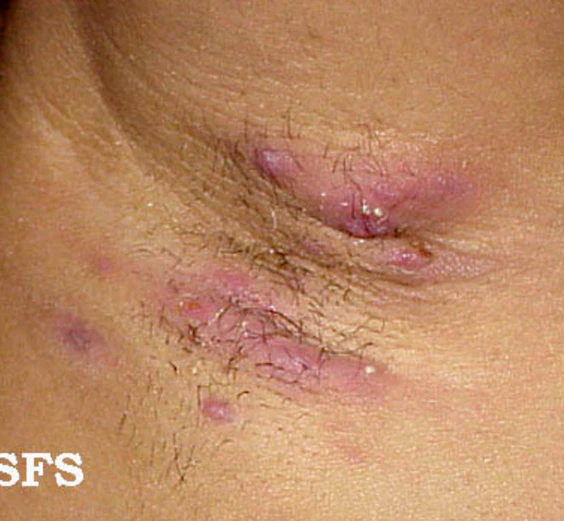
Гно́йный гидрадени́т (ГГ, суппурати́вный гидрадени́т, инве́рсные а́кне, боле́знь Верне́йля) — хроническое рецидивирующее воспалительное заболевание кожи, характеризующееся образованием болезненных узелков, абсцессов и свищевых ходов в областях, богатых апокриновыми потовыми железами[1]. В основе заболевания лежат процессы фолликулярной окклюзии, хронического воспаления и последующей деструкции тканей, что приводит к образованию глубоких узлов и рецидивирующих абсцессов. Наиболее типичными зонами поражения являются подмышечные впадины, паховая и аногенитальная области, а также область под молочными железами у женщин. Клинические проявления нередко сопровождаются болью, гнойными выделениями и неприятным запахом, что значительно влияет на повседневную активность и психосоциальное состояние пациентов[2][3]. Диагностика основывается на клинической картине[4]. Лечение зависит от тяжести и включает местные и системные противовоспалительные и антибактериальные средства, лазерную терапию, биологические препараты и хирургические методы[2].
Что важно знать
История
ГГ был впервые описан французским хирургом Альфредом Вельпо, который в период с 1833 по 1839 год опубликовал три публикации об особенностях воспалительного процесса в области подмышек, под молочными железами и в перианальной зоне[5]. В 1854 году другой французский врач, Аристид Вернейль, предложил для этого состояния термин «флегмонозный гидраденит». Впоследствии ГГ также называли как болезнь Вернейля[6].
В 1922 году немецкий дерматолог Пауль Шиффердекер высказал предположение о связи данного заболевания с апокриновыми потовыми железами, что послужило основой для формирования представлений о патогенезе гнойного гидраденита как воспаления потовых желёз[7].
В 1956 году Д. М. Пиллсбери и соавторы ввели термин «триада фолликулярной окклюзии», включающую гнойный гидраденит, конглобатные угри и рассекающий целлюлит волосистой части головы[8]. Позднее, в 1975 году, Г. Плевиг и А. М. Клигман расширили это понятие, добавив четвёртый компонент — эпителиальный копчиковый ход, и предложили термин «тетрада акне», подчёркивающий общность патогенетических механизмов этих состояний[9].
В 1989 году Г. Плевиг и М. Штегер предложили новое обозначение заболевания — acne inversa (инверсное акне), чтобы подчеркнуть его происхождение из фолликулярного аппарата, а не из потовых желёз. Этот термин не получил широкого распространения в медицинской номенклатуре, однако иногда продолжает использоваться как синоним ГГ[10].
Классификация
Клиническая классификация ГГ по Херли (1989 г.). Согласно системе стадирования Херли, выделяют 3 стадии ГГ, отражающих степень тяжести заболевания[1]:
- I стадия — единственный или множественные абсцессы, без свищей и рубцов.
- II стадия — один или несколько рецидивирующих абсцессов, расположенных на расстоянии друг от друга, с образование свищевых ходов и рубцов.
- III стадия — диффузное или близкое к диффузному поражение кожи или множественные сообщающиеся свищевые ходы и абсцессы, занимающие всю анатомическую область.
| Стадия | Описание
(число элементов сыпи) |
|---|---|
| 1 стадия (чисто) | абсцессы — 0, свищи с отделяемым — 0, узелки/узлы с признаками воспаления — 0, узелки/узлы без признаков воспаления — 0 |
| 2 стадия (минимальная) | абсцессы — 0, свищи с отделяемым — 0, узелки/узлы с признаками воспаления — 0, имеются невоспалительные узелки/узлы |
| 3 стадия (лёгкая) | абсцессы — 1, свищи с отделяемым — 0, узелки/узлы с признаками воспаления — от 1 до 4
или абсцесс или свищ с отделяемым — 1, узелки/узлы с признаками воспаления — 0 |
| 4 стадия (умеренная) | абсцессы — 0, свищи с отделяемым — 0, воспалительные узелки/узлы — ≥5
или абсцесс или свищ с отделяемым — 1 и воспалительные узелки/узлы — ≥1 или абсцессы или свищи с отделяемым — 2-5 и воспалительные узелки/узлы — <10 |
| 5 стадия (тяжёлая) | абсцессы или свищи с отделяемым — 2-5 и воспалительные узелки/узлы — ≥10 |
| 6 стадия (крайне тяжёлая) | абсцессы или свищи с отделяемым — >5 |
Тяжесть ГГ с помощью шкалы HS-PGA оценивают путём подсчёта количества абсцессов, свищей, воспалительных и невоспалительных узелков/узлов во всех областях тела. Согласно шкале HS-PGA выделяют шесть стадий заболевания[1].
| Количество баллов за показатель | Число поражённых областей тела | Площадь поражённой поверхности кожи (%) | Число очагов поражения (эритематозных, болезненных) | Дренаж (число перевязок в рабочую смену) | Боль (по визуальной аналоговой шкале боли) |
|---|---|---|---|---|---|
| 0 | 0 | 0 | 0 | 0 | 0—1 |
| 1 | 1 | 1 | 1—2 | 0 | 2—4 |
| 2 | 2 | 2—3 | 2—3 | 1 | 2—4 |
| 3 | 3 | 4—5 | 4—5 | >1 | 5—7 |
| 4 | ≥4 | >5 | >5 | >1 | 8—10 |
Использование HSSI подразумевает оценку качественных объективных показателей и качественных субъективных показателей. Оцениваются площадь поражённой поверхности тела, количество поражений кожи, выраженность боли и дренаж. При наборе от 0 до 7 баллов — лёгкая степень тяжести; от 8 до 12 баллов — умеренная степень тяжести; ≥13 баллов — тяжёлая степень тяжести[1].
Этиология
Точная причина ГГ неизвестна; развитие заболевания связывают с взаимодействием генетических, иммунных и внешних факторов. Болезнь рассматривают как хроническое иммуноопосредованное аутовоспалительное заболевание, в основе которого лежит патологический процесс в верхних отделах волосяного фолликула и выводных протоках сальных и апокринных желёз. Считается, что фолликулярный гиперкератоз в области перешейка и воронки приводит к окклюзии фолликулов и выводных протоков, что может быть как первичным событием, так и развиваться вторично в ответ на воспаление. Роль бактериальной микрофлоры рассматривают как вторичную: микроорганизмы кожи и волосяных фолликулов усиливают иммуновоспалительный ответ, но в развитии заболевания бактерии не являются этиологическим фактором[1][3].
Генетическая предрасположенность подтверждается семейным характером болезни у значительной части пациентов и ассоциациями с мутациями в генах NCSTN, PSEN1, PSENEN, кодирующих белки, которые входят в состав комплекса под названием гамма-секретаза, что приводит к нарушению сигнального пути Notch и может нарушать дифференцировку кератиноцитов и регуляцию иммунных ответов в волосяных фолликулах. Эти генетические и эпигенетические изменения повышают восприимчивость к патологической активации воспалительных путей[1][11].
Гормональные факторы влияют на течение болезни; клинически отмечают связь с колебаниями половых гормонов, а приём препаратов с андрогеноподобным эффектом может усугублять симптомы[1].
Факторы риска и провоцирующие факторы:
- генетическая предрасположенность[1];
- курение, индуцирующее эпидермальную гиперплазию, усиление фолликулярного гиперкератоза, стимуляцию продукции интерлейкина-1β и фактора некроза опухоли α и способствующее адгезии микроорганизмов[1];
- ожирение и механическое трение в складках кожи, приводящие к мацерации, окклюзии фолликулов и повышенному росту бактерий[1][3];
- гормональные факторы, в том числе дисбаланс андрогенов и эстрогенов, влияние гормональных препаратов[12];
- диета с высоким содержанием жиров[3];
- климатические условия, в частности жаркий влажный климат, способствующий ухудшению симптомов[12];
- психический стресс как фактор, способный провоцировать или усугублять обострения[3][12];
- ношение тесной, непроницаемой одежды, частое трение и местные травмы кожи[12];
- сопутствующие состояния, в том числе метаболический синдром и сахарный диабет, ассоциированные с повышенным риском более тяжёлого течения[3][12];
- изменения микробиоты кожи и кишечника с формированием анаэробной полимикробной флоры и биоплёнок, поддерживающих хроническое воспаление[3].
Патогенез
Начальным патогенетическим звеном чаще всего считают фолликулярный гиперкератоз в области перешейка и воронки и закупорку устья волосяного фолликула, что приводит к накоплению фолликулярного содержимого и расширению фолликула. Разрыв расширенного фолликула с последующим попаданием кератина, клеточного детрита и микроорганизмов в дерму и подкожную клетчатку инициирует выраженную локальную воспалительную реакцию и вторичную бактериальную инвазию, что усугубляет воспаление и способствует формированию абсцессов и свищевых ходов[1].
Попавшие в ткань фолликулярные компоненты и бактерии активируют клеточный компонент врождённого иммунитета, в частности макрофаги, дендритные клетки и фибробласты, с последующей продукцией провоспалительных цитокинов интерлейкина-1β и фактора некроза опухоли α, уровень которых значительно повышен в коже больных ГГ. Эти цитокины стимулируют кератиноциты к продукции хемокинов, привлекающих нейтрофилы, Т-лимфоциты и моноциты, и повышают экспрессию молекул адгезии на эндотелии, что усиливает приток иммунных клеток в очаги поражения. Фактор некроза опухоли α увеличивает содержание T-хелперов 17 типа. Сверхактивация макрофагов и клеток Т-хелперов 17 типа приводит к повышенному высвобождению интерлейкина-23 и интерлейкина-17 (ИЛ-17). Концентрация ИЛ-17 напрямую коррелирует с тяжестью заболевания. ИЛ-17 усиливает продукцию интерлейкина-1β и фактора некроза опухоли α макрофагами и способствует притоку нейтрофилов и других воспалительных клеток, создавая замкнутую воспалительную реакцию. Интерферон γ индуцирует секрецию хемокинов, привлекающих Т-хелперы 1-го типа, и стимулирует дифференцировку макрофагов в антигенпрезентирующие клетки, что способствует дальнейшей активации адаптивного иммунитета в очагах поражения[1][3].
Нейтрофилы играют ключевую роль в формировании гнойного компонента: они высвобождают различные гранулярные белки, включая миелопероксидазу, лизоцимы, нейтрофильные эластазы, пентраксины, коллагеназы и матриксные металлопротеиназы, что вызывает разрушение внеклеточного матрикса, способствуя прогрессированию некроза, образованию абсцессов и свищей и формированию грубых рубцов. Матриксные металлопротеиназы участвуют в разрушении дермы и способствуют разрыву фолликулов[1][3].
Свищевые ходы представляют собой эпителиализированные структуры, сходные с поверхностным эпидермисом; предполагается, что они образуются в результате разрушения фолликула и аномальной пролиферации и дифференцировки стволовых клеток, что приводит к формированию эпителиальных тяжей[1].
Кожный микробиом при заболевании характеризуется дисбиозом, снижением разнообразия комменсалов и сдвигом в сторону анаэробной флоры с образованием биоплёнок, что поддерживает персистенцию воспаления и снижает воспроизводимость результатов бактериологических исследований очагов поражения. Экзогенные факторы, такие как повышенная температура и влажность в кожных складках, способствуют размножению условно-патогенных бактерий и образованию биоплёнок[1].
Генетические дефекты, нарушение передачи сигнального пути Notch, избыток фактора некроза опухоли α, аномалии регуляции антимикробных пептидов и системная иммунная дисрегуляция дополняют картину патогенеза и объясняют вариабельность клинических фенотипов и тяжести течения. Хроническая активация провоспалительных путей приводит к персистирующему воспалению, некрозу тканей, образованию абсцессов, свищей и грубых рубцов, что определяет клиническую картину заболевания[1][3].
На ранних стадиях выявляют фолликулярную окклюзию, сопровождающуюся фолликулярным гиперкератозом, кератиновой закупоркой и гиперплазией эпителия воронки. Часто наблюдается эпидермальная псориазоформная гиперплазия, уменьшение объёма сальной железы и формирование фолликулярных кист. В дерме определяется перифолликулярное воспаление с преобладанием лимфоцитов, к которому могут присоединяться плазматические клетки[2][13].
По мере прогрессирования процесса формируются нейтрофильные абсцессы и синусы, окружённые хроническим воспалительным инфильтратом с участием гистиоцитов и гигантских клеток, а также значительное количество грануляционной ткани. Могут выявляться эозинофилы[2][13].
Эпидемиология
Распространённость ГГ варьирует по данным различных исследований от 0,1 % до 4,1 %. В странах Европы этот показатель обычно составляет 0,7—1,2 %. Заболевание развивается после полового созревания и наиболее часто выявляется в возрасте 20-40 лет. Женщины страдают ГГ примерно в 3 раза чаще, чем мужчины. Для женщин более характерно поражение подмышечной, паховой и субмаммарной областей, тогда как у мужчин высыпания чаще локализуются на коже ягодичной, перианальной и промежностной областей. У представителей африканской расы заболевание встречается в 3 раза чаще, чем у европеоидов[1][2].
У 44—63 % женщин отмечаются предменструальные обострения ГГ. Среди них примерно у 3/4 обострение возникло в течение недели перед менструацией. Во время беременности динамика заболевания может быть разной. В одних наблюдениях улучшение состояния фиксировалось у 20—30,2 % женщин, а ухудшение у 8—16,7 %. В другом исследовании ухудшение зарегистрировано у 61,9 % пациенток. Эти различия связывают с изменением уровня половых гормонов в разные триместры. После родов обострения описаны у 40—66 % женщин. В постменопаузе почти у половины пациенток отмечается ремиссия заболевания[3].
Диагностика
Диагноз устанавливается на основании анамнеза, клинической картины и результатах лабораторных и инструментальных методов исследования.
Основные критерии постановки диагноза[1]:
- характерное поражение кожи (двойные открытые псевдокомедоны, узлы, абсцессы, свищевые ходы, рубцы);
- склонность к локализации высыпаний в складках кожи в подмышечных областях, промежности и паховой области, в субмаммарной области и зонах молочных желёз;
- хроническое течение болезни, которое может быть персистирующим (наличие высыпаний на протяжении по меньшей мере 6 месяцев) и рецидивирующим (более 2 очагов поражения, возникших впервые или появившихся как рецидив в пределах последних 6 месяцев).
Дополнительные критерии постановки диагноза[1]:
- семейный анамнез заболевания;
- стерильное отделяемое свищевых ходов или наличие при бактериологическом исследовании комменсальной микрофлоры;
- наличие эпителиального копчикового хода.
ГГ характеризуется хроническим рецидивирующим течением с поражением областей кожи, богатых апокриновыми железами. Высыпания обычно локализуются в паховой, подмышечной, перианальной, перинеальной, ягодичной и лобковой областях, под молочными железами и в пахово-бедренной складке, реже — на животе, груди, спине, лице, волосистой части головы, заушной области и веках. Помимо этого высыпания могут появиться в областях где нет апокриновых желёз, например, в складках кожи, образовавшихся вокруг грыжи. Чаще всего первоначально поражается подмышечная или аногенитальная область, но по мере прогрессирования заболевания вовлекаются новые участки кожи, и у большинства пациентов отмечается поражение более одной анатомической зоны[1].
Высыпания полиморфны и представлены глубоко расположенными болезненными плотными узелками ярко-красного цвета, диаметром до 1—2 см или узлами, которые сливаясь могут образовывать шнуровидные возвышения кожи. Узлы и узелки могут самопроизвольно регрессировать, длительно сохраняться или абсцедировать. Образующиеся абсцессы могут сливаться глубоко в дерме и самопроизвольно вскрываться наружу с выделением гнойного или серозно-геморрагического содержимого. Со временем воспалительные элементы становятся персистирующими. Узлы увеличиваются в размерах, занимают большую площадь, кожа над ними приобретает синюшно-красный оттенок. Поверхность элементов может изъязвляться, образуя множественные полости, напоминающие структуру «медовых сот», с формированием абсцессов и свищевых ходов. В результате хронического воспаления развивается выраженный фиброз с формированием гипертрофических мостовидных рубцов[1].
Заболевание протекает волнообразно: периоды ремиссии сменяются обострениями с появлением новых воспалительных узлов. Появление высыпаний обычно сопровождается болью, жжением или зудом. У части пациентов наблюдается продромальная симптоматика — покалывание, ощущение жара, гипергидроз за 12—48 часов до возникновения новых элементов[1][2].
При поражении аногенитальной области возможно развитие стриктур уретры, заднего прохода и прямой кишки, а также образование параректальных и парауретральных свищей. В тяжёлых случаях заболевание приводит к значительному дискомфорту, неприятному запаху и ограничению трудоспособности[1].
Для классификации степени тяжести используются различные классификации; наиболее часто используемая — система стадирования по Херли[1].
ГГ является компонентом тетрады фолликулярной окклюзии наряду с конглобатным акне, рассекающим целлюлитом волосистой части головы и эпителиальным копчиковым ходом[2].
- Клинический анализ крови — может наблюдаться повышение скорости оседания эритроцитов, анемия; применяется для определения выраженности обострения или выявления осложнений, а также для контроля проводимой терапии[1].
- Биохимический анализ крови — может наблюдаться гипопротеинемия; повышение концентрации C-реактивного белка при выраженном воспалительном процессе[1].
- Клинический анализ мочи — применяется для контроля безопасности проводимой системной терапии[1].
- Микробиологическое исследование отделяемого язв и свищевых ходов на чувствительность к антибактериальным и противогрибковым препаратам — для определения наиболее эффективного лекарственного препарата[1].
- Гистологическое исследование поражённых участков кожи[2]
- Ультразвуковое исследование мягких тканей или кожи — применяется при необходимости выявления ранних морфологических элементов, дифференциации абсцессов и подкожных свищевых ходов, для постоперационного контроля и контроля при введении глюкокортикоидов[1].
- Магнитно-резонансная томография мягких тканей — могут наблюдаться выраженное утолщение кожи, уплотнение тканей и формирование множественных абсцессов. Также возможна визуализация свищевых ходов[1].
- Фистулография — применяется для определения локализации и протяжённости свищевых ходов[1].
Дифференциальная диагностика
Дифференциальную диагностику следует проводить со следующими заболеваниями:
- лимфомы кожи;
- гангренозная пиодермия;
- скрофулодерма;
- актиномикоз[1];
- паховая гранулёма;
- венерическая лимфогранулёма;
- обыкновенные угри;
- эпидермоидная киста;
- дермоидная киста;
- киста бартолиновой железы;
- болезнь Крона (особенно с поражением перианальной области);
- саркоидоз;
- гистиоцитоз X;
- фолликулотропный грибовидный микоз;
- фолликулярная пиодермия (фолликулит, фурункулы, карбункулы)[2];
- бластомикоз;
- фелиноз;
- нокардиоз;
- рожа;
- сифилис[14].
Осложнения
Могут наблюдаться следующие осложнения ГГ:
- вторичное инфицирование;
- образование рубцов[15];
- хроническая боль;
- контрактура конечностей;
- ограничение подвижности;
- периферическая лимфедема;
- анемия;
- гиперпротеинемия;
- амилоидоз;
- аксиальная артропатия;
- периферическая артропатия;
- плоскоклеточная карцинома[2],
- флегмона мягких тканей с последующим развитием сепсиса;
- элефантиаз[1];
- пилонидальная болезнь;
- дислипидемия[16];
- артрит мелких суставов кистей и стоп;
- полиартрит;
- полиартралгия[17].
Данные наблюдений свидетельствуют о повышенном риске развития рака полости рта и гепатоцеллюлярной карциномы. Психологические последствия ГГ включают депрессию, социальную изоляцию, снижение удовлетворённости отношениями, сексуальную дисфункцию, снижение продуктивности на работе, тревожное расстройство, суицидальные мысли или попытки суицида[2][18].
У пациентов с ГГ наблюдается повышенный риск развития сахарного диабета, высокого кровяного давления, сердечных приступов, метаболического синдрома[19], синдрома поликистозных яичников[20], развития аутоиммунных заболеваний, в том числе анкилозирующего спондилита, ревматоидного артрита, псориатического артрита и воспалительных заболеваний кишечника[16][21].
Лечение
Лечение ГГ комплексное и зависит от тяжести, распространённости и клинического фенотипа заболевания. Цели терапии — уменьшение воспаления, контроль боли, предотвращение формирования новых узлов/абсцессов и свищей, санация хронических очагов и улучшение качества жизни[1].
Рекомендуются всем пациентам независимо от стадии: отказ от курения, контроль массы тела и метаболических нарушений, соблюдение личной гигиены, избегание экзогенных провоцирующих факторов (высокие температуры, физические упражнения, потливость, стресс, усталость, растирание, ношение тесной одежды, использование дезодорантов и бритьё)[3].
Консервативная терапия гнойного гидраденита включает наружные антисептики, противомикробные препараты, системные антибиотики, противовоспалительные средства, гормональные препараты и биологическую терапию. Выбор методики зависит от тяжести заболевания, наличия свищей, сопутствующих состояний и ответа на предыдущие методы лечения[1].
Для наружной обработки используют антисептические растворы (например, хлоргексидин, повидон-йод, перекись водорода), а также препараты, применяемые при акне — бензоила пероксид, сульфадиазин серебра, пиритион цинка. Они уменьшают бактериальную нагрузку и воспаление в активных очагах[1].
При поверхностных воспалительных элементах назначают наружные антибиотики, чаще всего клиндамицин 1 %, который снижает число папул и пустул, но слабее влияет на глубокие узлы и абсцессы. В отдельных случаях при острых болезненных узлах проводят локальное введение кортикостероидов (триамцинолона), что способствует быстрому уменьшению боли и отёка[1].
Системные препараты назначаются при среднетяжёлом и тяжёлом течении заболевания, частых рецидивах или неэффективности местных средств. Антибактериальные препараты являются основой консервативного лечения[1]:
- доксициклин применяется как препарат первой линии и обладает как антибактериальными, так и противовоспалительными свойствами;
- при недостаточном эффекте используется комбинация клиндамицина и рифампицина, эффективная при I—II стадии заболевания;
- при выраженной резистентности назначают дапсон или эртапенем, применяемый как препарат резерва и при подготовке к хирургическому лечению.
Если антибактериальная терапия недостаточна, возможен переход к системным ретиноидам. Используются как ретиноиды для лечения псориаза, так и изотретиноин, уменьшающий гиперкератоз и воспаление. При тяжёлом или рефрактерном течении возможно применение иммунодепрессантов, например циклоспорина. Краткие курсы системных кортикостероидов (преднизолон) применяют для купирования выраженных обострений[1].
У женщин с I—II стадией заболевания могут быть эффективны антиандрогенные препараты (спиронолактон), а у мужчин — ингибиторы 5-альфа-редуктазы (финастерид), которые воздействуют на гормональные механизмы, участвующие в заболевании[1].
У пациентов с сопутствующей инсулинорезистентностью, синдромом поликистозных яичников или сахарным диабетом может назначаться метформин, который улучшает чувствительность к инсулину и опосредованно снижает выраженность воспаления[1].
При тяжёлом и резистентном течении II—III стадии по Херли назначается генно-инженерная биологическая терапия, включая ингибиторы фактора некроза опухоли-альфа (адалимумаб, инфликсимаб) и секукинумаб. Эти препараты уменьшают системное воспаление, частоту рецидивов и являются наиболее эффективными средствами при устойчивом гидрадените[1].
В качестве дополнительных методов рассматривают криотерапию[22], назначение цинка с никотинамидом[23], а также ботулотоксин, который, согласно данным исследований, способен улучшать состояние у пациентов, не отвечающих на стандартную терапию[24].
Симптоматическое лечение включает[1]:
- нестероидные противовоспалительные препараты (диклофенак, ибупрофен, целекоксиб, напроксен, индометацин или кеторолак);
- местные анестетики (лидокаин).
Хирургическое вмешательство показано при наличии флюктуирующих абсцессов, множественных свищевых ходов, выраженном болевом синдроме. Хирургическое лечение не следует проводить пациентам с высокой воспалительной активностью гнойного гидраденита. В таких случаях требуется подготовка пациентов, во время которой проводится системная лекарственная терапия[1].
Одним из вариантов хирургического лечения является лазерная деструкция (чаще CO₂-лазером). Её применяют при болезненных активных очагах или наличии свищей. Обрабатывают участки с воспалением, выделениями или подозрением на абсцесс. После местной анестезии (лидокаином) лазером удаляют поражённую ткань до уровня глубокой дермы или верхней части подкожной клетчатки[1].
При формировании флюктуирующих абсцессов выполняют вскрытие и дренирование, с обязательным выскабливанием полости и выявленных свищевых ходов[1].
Если консервативная терапия неэффективна, пациентам со свищами и сильными болями показано иссечение поражённой кожи. Наиболее надёжным считается широкое иссечение, поскольку частичные операции связаны с более частыми рецидивами[1].
При обширных поражениях возможно проведение свободной кожной пластики дерматомным перфорированным лоскутом или реконструктивных пластических операций с применением кожно-мышечных и фасциально-кожных лоскутов. Данные методы используются преимущественно при рецидивирующем течении и позволяют закрыть большие дефекты, в том числе в трудных анатомических областях[1].
Прогноз
Прогноз при ГГ зависит от стадии заболевания, своевременности диагностики и наличия сопутствующих факторов риска. Заболевание имеет хроническое, рецидивирующее течение и считается неизлечимым. Задержка постановки диагноза, а также действие факторов риска нередко ухудшают течение и способствуют прогрессированию воспаления. Наиболее неблагоприятным считается течение при III стадии по Херли, когда высока вероятность осложнений и формируются выраженные рубцовые изменения. Ранняя диагностика и своевременное начало терапии имеют ключевое значение для снижения риска необратимых последствий и улучшения качества жизни[2][15].
Диспансерное наблюдение
Наблюдение у врача-дерматовенеролога.
Профилактика
Меры первичной профилактики не разработаны. К мерам вторичной профилактики относят[1]:
- диету с ограничением потребления молочных продуктов и исключением из рациона пивных дрожжей;
- снижение массы тела;
- отказ от курения;
- ограничение воздействия факторов, раздражающих кожу, в том числе избегание бритья и использование лазерной эпиляции.
Примечания
| Правообладателем данного материала является АНО «Интернет-энциклопедия «РУВИКИ». Использование данного материала на других сайтах возможно только с согласия АНО «Интернет-энциклопедия «РУВИКИ». |