Врождённый дискератоз
Врождённый дискерато́з (синдро́м Ци́нссера — Э́нгмана — Ко́ула) — редкое прогрессирующее наследственное заболевание из группы теломеропатий, характеризующееся выраженной фенотипической вариабельностью. Классическая триада симптомов включает ониходистрофию, патологическую пигментацию кожи и лейкоплакию слизистых оболочек. У большинства пациентов развивается синдром костномозговой недостаточности, обусловленный прогрессирующим угнетением кроветворения. Заболевание может наследоваться по X-сцепленному рецессивному, аутосомно-доминантному или аутосомно-рецессивному типу. В зависимости от генетического варианта, клиническое течение может сопровождаться задержкой роста, фиброзом лёгких, поражением печени, остеопенией, гипогонадизмом, а также высоким риском развития миелодиспластического синдрома, острого миелоидного лейкоза и злокачественных новообразований различных локализаций[1][2][3].
Общие сведения
История
Врождённый дискератоз впервые был описан в 1906 году австрийским дерматовенерологом М. Цинссером, который представил клиническое наблюдение пациента с сочетанием кожной пигментации, поражения слизистых оболочек и дистрофии ногтей. В 1910 году шведский врач Энгман расширил описание кожных проявлений заболевания. В 1930 году американский дерматовенеролог Коул обобщил сведения о синдроме, выделив его как самостоятельную нозологическую единицу. В 1960-х годах было установлено, что у большинства пациентов с этим синдромом развивается прогрессирующая апластическая анемия, а позднее — злокачественные заболевания системы крови. В конце XX — начале XXI века были идентифицированы генетические мутации, лежащие в основе болезни, включая мутации в генах DKC1, TERT, TERC и других. Это позволило отнести заболевание к группе теломеропатий[3][4].
Классификация
В зависимости от типа наследования и молекулярно-генетических особенностей врождённый дискератоз подразделяется на несколько форм[3][5]:
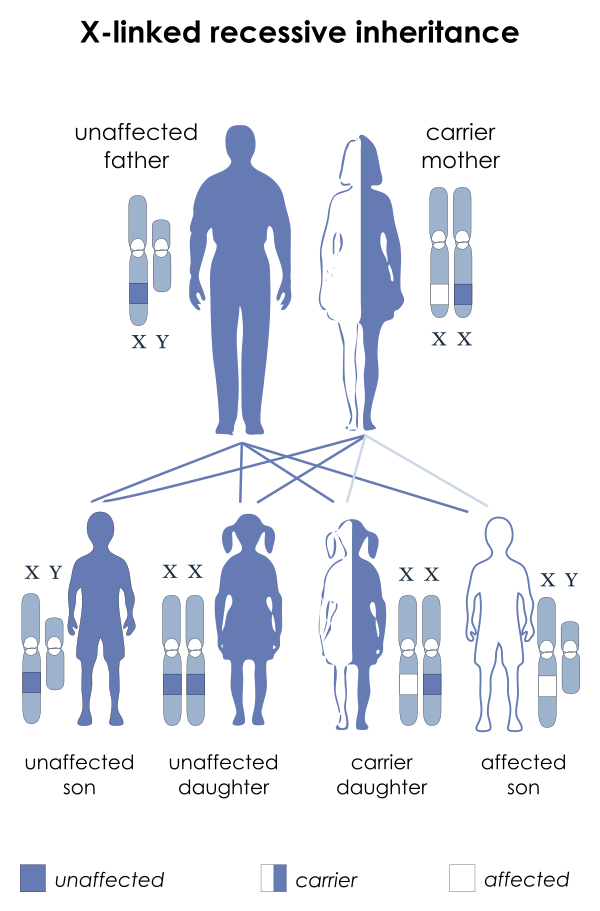
- Х-сцепленный рецессивный врождённый дискератоз (классическая форма) — наиболее распространённый вариант заболевания, обусловленный мутациями в гене DKC1, кодирующем белок дискерин. Характеризуется тяжёлым течением, ранним началом и преимущественным поражением лиц мужского пола.
- Аутосомно-доминантная форма — связана с мутациями в генах TERT, TERC, TINF2. Отличается более вариабельным фенотипом и, как правило, более поздней манифестацией.
- Аутосомно-рецессивная форма — обусловлена мутациями в генах NOP10, NHP2, TERT, TERC, TINF2. Характеризуется ранним началом, тяжёлым течением и частым вовлечением нескольких органов и систем.
Этиология
Врождённый дискератоз является наследственным заболеванием, относящимся к группе теломеропатий — патологических состояний, обусловленных нарушениями в работе генов, обеспечивающих стабильность и целостность теломер. Теломеры представляют собой специализированные концевые участки хромосом, защищающие генетический материал от деградации и нарушений репликации. Нарушения в регуляции структуры и функций теломер приводят к их преждевременному укорочению, что вызывает дефицит пролиферативной активности стволовых и соматических клеток[6][7].
Наиболее частой формой заболевания является Х-сцепленный рецессивный тип, обусловленный мутацией в гене DKC1, кодирующем белок дискерин. Этот белок принимает участие в процессах созревания рибосомальной РНК и стабилизации теломеразного комплекса. Нарушение функции DKC1 приводит к сбоям в регенерации быстро обновляющихся тканей — кожи, слизистых оболочек и костного мозга[3][8].
Аутосомно-доминантные формы заболевания связаны с мутациями в генах TERT, TERC, RTEL1, TINF2 и др. Эти гены кодируют компоненты фермента теломеразы и белки, обеспечивающие поддержание стабильности теломер. В частности, TERT и TERC участвуют в синтезе теломерных последовательностей, RTEL1 регулирует процессы репликации[8][9].
Аутосомно-рецессивные формы ассоциированы с мутациями в генах NOP10, NHP2, PARN, WRAP53, ACD и других. Эти гены обеспечивают сборку и стабильность теломеразного комплекса, а также участвуют в контроле транскрипции и процессинге РНК. Нарушения их функций также ведут к ускоренному укорочению теломер и прогрессирующему истощению пролиферативного резерва тканей[10].
Патогенез
Патогенез врождённого дискератоза обусловлен критическим укорочением теломер, возникающим в результате мутаций в генах, участвующих в регуляции длины теломер и поддержании геномной стабильности. Уменьшение длины теломер приводит к активации механизмов клеточного старения и апоптоза, что наиболее выражено в тканях с высокой пролиферативной активностью: эпителии кожи и слизистых оболочек, костном мозге, гепатоцитах и клетках лёгких.
Нарушение регенераторного потенциала костного мозга приводит к истощению пула гемопоэтических стволовых клеток и нарушению процессов кроветворения, что проявляется в развитии панцитопении и прогрессирующего синдрома костномозговой недостаточности. В эпителии кожи и слизистых оболочек наблюдаются нарушения дифференцировки и процессов ороговения, а также дегенеративные изменения. В паренхиматозных органах, таких как лёгкие и печень, теломерная дисфункция сопровождается хроническим воспалением и прогрессирующим формированием фиброзных изменений[11].
Системная теломерная дисфункция значительно увеличивает риск злокачественной трансформации клеток. У пациентов с врождённым дискератозом отмечается высокая частота миелодиспластического синдрома, острого миелоидного лейкоза, а также плоскоклеточного рака слизистых оболочек и солидных опухолей. Эти процессы связаны с нарушениями механизмов репарации ДНК, геномной нестабильностью и дисрегуляцией клеточного цикла[11].
Эпидемиология
Врождённый дискератоз относится к числу крайне редких наследственных заболеваний. Распространённость оценивается как 1 случай на 1 000 000 человек. Заболеваемость не имеет выраженной географической или этнической предрасположенности. Классическая Х-сцепленная форма преимущественно диагностируется у мальчиков и составляет до 50—60 % всех случаев заболевания. Соотношение заболевших мужчин и женщин составляет примерно 3:1, что связано с особенностями наследования. Аутосомно-доминантные и аутосомно-рецессивные формы встречаются у представителей обоих полов. Клинические проявления могут дебютировать в детском, подростковом или взрослом возрасте, в зависимости от генетического варианта и степени укорочения теломер[3][12].
Клиническая картина
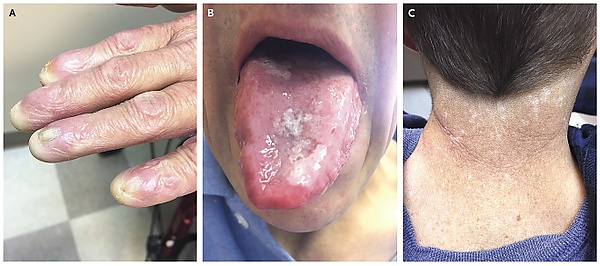
Врождённый дискератоз характеризуется поражением различных органов и систем. Начало заболевания может приходиться на детский, подростковый или взрослый возраст. Классические проявления включают дистрофические изменения ногтевых пластин, сетчатую гиперпигментацию кожи и лейкоплакию слизистых оболочек. Указанные симптомы обычно развиваются последовательно и прогрессируют по мере нарастания теломерной дисфункции[3][5].
Поражение ногтевых пластин является одним из ранних признаков врождённого дискератоза. Оно проявляется ониходистрофией с характерными изменениями: истончением, продольной исчерченностью, тусклостью, ломкостью, утратой прозрачности и блеска. В более поздних стадиях возможно развитие онихолизиса и онихомадеза, вплоть до полной деструкции ногтей, преимущественно на руках[3][5].
Кожные проявления включают сетчатую или пятнисто-сетчатую гиперпигментацию, преимущественно в области шеи, груди и разгибательных поверхностей верхних конечностей. Данные изменения могут сопровождаться ксерозом, телеангиэктазиями, очаговой атрофией и гиперкератозом. В отдельных случаях наблюдаются участки депигментации, алопеция, а также нарушения функции потовых желёз — гипогидроз или ангидроз[3][13].
Лейкоплакия поражает преимущественно слизистую оболочку полости рта — язык, внутреннюю поверхность щёк и мягкое нёбо. В редких случаях патологический процесс распространяется на слизистые оболочки гортани и пищевода. Учитывая повышенный онкологический риск, лейкоплакия рассматривается как предраковое состояние[11].
Синдром костномозговой недостаточности развивается у большинства пациентов и проявляется прогрессирующей панцитопенией — анемией, лейкопенией и тромбоцитопенией, обусловленными истощением пула гемопоэтических стволовых клеток[3].
Поражение дыхательной системы характеризуется развитием интерстициального фиброза лёгких с клиническими проявлениями в виде прогрессирующей экспираторной одышки, сухого кашля, гипоксемии и дыхательной недостаточности. Со стороны печени возможно развитие гепатомегалии, лабораторных признаков цитолиза и холестаза, портальной гипертензии с последующим развитием гиперспленизма, варикозного расширения вен пищевода и асцита[5][14].
Эндокринные расстройства могут включать гипогонадизм, задержку полового развития, бесплодие, сахарный диабет 2-го типа. У детей возможна задержка роста. Со стороны иммунной системы выявляется повышенная восприимчивость к бактериальным, вирусным и грибковым инфекциям, обусловленная развитием комбинированного иммунодефицита клеточного и гуморального звеньев[14][15].
У части пациентов развивается онкопатология: плоскоклеточный рак слизистых оболочек ротовой полости, аногенитальной области и пищевода, миелодиспластический синдром, острый миелоидный лейкоз, а также солидные опухоли различных локализаций. К дополнительным проявлениям относятся облитерация слезоотводящих путей с развитием хронического конъюнктивита, снижение минеральной плотности костей (остеопения) и неврологические нарушения, включая мозжечковую атрофию и когнитивные расстройства[5][16].
Диагностика
Диагностика врождённого дискератоза основывается на комплексной оценке клинической картины, данных лабораторных и инструментальных исследований, а также молекулярно-генетическом анализе[14].
- Клинический анализ крови — определяется выраженность панцитопении (снижение уровня гемоглобина, тромбоцитов и лейкоцитов).
- Биохимический анализ крови — позволяет выявить признаки цитолиза и холестаза при поражении печени (определение активности аланинаминотрансферазы, аспартатаминотрансферазы, гамма-глутамилтрансферазы, щелочной фосфатазы, общего билирубина и его фракций).
- Иммунофенотипирование клеток периферической крови методом проточной цитометрии — для оценки субпопуляций лимфоцитов и иммунного статуса.
- Молекулярно-генетическое исследование мутаций в генах DKC1, TERT, TERC, RTEL1, TINF2, NOP10, NHP2, PARN, WRAP53 — позволяет подтвердить форму заболевания.
- Определение длины теломер и активности теломеразы клеток — проводится для оценки функционального состояния теломерного комплекса.
- Патолого-анатомическое исследование биопсийного материала костного мозга — позволяет оценить клеточный состав и степень угнетения гемопоэза.
- Ультразвуковое исследование органов брюшной полости — применяется для выявления гепатоспленомегалии, асцита и признаков портальной гипертензии.
- Рентгенография органов грудной клетки — используется при подозрении на интерстициальный фиброз лёгких.
- Эзофагогастродуоденоскопия — исследование слизистой пищевода и выявление лейкоплакии или расширения вен.
- Магнитно-резонансная томография головного мозга — при наличии неврологических симптомов с целью исключения мозжечковой атрофии.
Дифференциальная диагностика
- Апластическая анемия;
- Анемия Фанкони;
- Синдром Швахмана — Даймонда;
- Врождённая пахионихия;
- Идиопатический лёгочный фиброз;
- Трахионихия;
- Синдром ногтя — надколенника;
- Изолированная лейкоплакия;
- Анемия Даймонда — Блекфена;
- Синдром Рейтера;
- Болезнь Дарье — Уайта;
- Болезнь Боуэна;
- Синдром Негели — Франческетти — Ядассона;
- Пигментная ретикулярная дерматопатия;
- Другие теломеропатии (синдром Хойераала — Хрейдарссона, синдром Ротмунда — Томсона, синдром Пейтца — Егерса и др.).
Осложнения
Врождённый дискератоз может приводить к развитию следующих осложнений[14][16]:
- Интерстициальный фиброз лёгких;
- Лёгочная гипертензия;
- Портальная гипертензия;
- Гиперспленизм;
- Варикозное расширение вен пищевода;
- Хронические и рецидивирующие инфекции;
- Иммунодефицитные состояния (преимущественно Т-клеточная недостаточность);
- Миелодиспластический синдром;
- Острый миелоидный лейкоз;
- Плоскоклеточный рак слизистых оболочек ротовой полости, пищевода, аногенитальной области;
- Солидные опухоли различных локализаций (рак лёгкого, печени, желудка, поджелудочной железы);
- Бесплодие;
- Тиреоидит;
- Хроническая печёночная недостаточность;
- Сахарный диабет II типа.
Лечение
Терапия врождённого дискератоза направлена на коррекцию синдрома костномозговой недостаточности, профилактику и лечение системных осложнений, а также диспансерное наблюдение с целью раннего выявления злокачественных новообразований[14].
Основным методом лечения при выраженной костномозговой недостаточности является аллогенная трансплантация гемопоэтических стволовых клеток. До выполнения трансплантации проводится симптоматическая и поддерживающая терапия. Она включает переливание компонентов крови (эритроцитарной массы и тромбоцитов по показаниям), назначение колониестимулирующих факторов при нейтропении. При наличии выраженного иммунодефицита и рецидивирующих инфекциях может рассматриваться назначение иммуноглобулина человека нормального внутривенно[14][11][18].
Лечение интерстициального фиброза лёгких включает длительную кислородотерапию и, при наличии показаний, назначение антифибротических препаратов. При поражении печени с развитием портальной гипертензии показано назначение урсодезоксихолевой кислоты при холестазе, диуретиков при асците, а также выполнения эндоскопических процедур — лигирования варикозно расширенных вен пищевода или склеротерапии. При неэффективности — обсуждается спленэктомия или выполнение трансъюгулярного внутрипечёночного портосистемного шунтирования[14][11].
Гормональные нарушения (например, гипогонадизм) являются показанием к заместительной гормональной терапии, проводимой под контролем эндокринолога. Сахарный диабет II типа требует стандартной гипогликемической терапии с учётом метаболического статуса пациента. Злокачественные новообразования при врождённом дискератозе встречаются часто, поэтому необходим регулярный скрининг[14][16].
Прогноз
Прогноз при врождённом дискератозе зависит от формы заболевания, возраста манифестации, выраженности системных проявлений и своевременности начала наблюдения и терапии. Наиболее тяжёлое течение наблюдается при Х-сцепленном рецессивном варианте, сопровождающемся ранним развитием апластической анемии, фиброза лёгких и поражения печени. В таких случаях продолжительность жизни значительно сокращается и в среднем составляет 20—30 лет. Аутосомно-доминантные и аутосомно-рецессивные формы характеризуются более благоприятным течением, однако также сопряжены с высоким риском развития миелодиспластического синдрома, острого миелоидного лейкоза и злокачественных новообразований различной локализации[13][18].
При регулярном диспансерном наблюдении, своевременной поддерживающей терапии и, при необходимости, трансплантации гемопоэтических стволовых клеток возможно существенное продление жизни и повышение её качества[18].
Профилактика
Специфическая профилактика врождённого дискератоза отсутствует. Основное внимание уделяется ранней диагностике и мониторингу состояния здоровья пациентов с целью предупреждения тяжёлых осложнений, в первую очередь — синдрома костномозговой недостаточности и онкогематологических заболеваний. Семьям с отягощённым генетическим анамнезом рекомендуется проведение медико-генетического консультирования. Больным с подтверждённым диагнозом необходимо избегать факторов, способных усугубить течение заболевания, таких как ионизирующее излучение, некоторые химиотерапевтические препараты, табакокурение и инфекции[14][16].
Регулярное клиническое наблюдение с оценкой функции костного мозга, лёгких, печени и слизистых оболочек, а также диспансерное наблюдение с участием профильных специалистов — гематолога, дерматовенеролога, пульмонолога, гастроэнтеролога, стоматолога, эндокринолога и офтальмолога — позволяет своевременно выявлять осложнения и корректировать терапию[14][16].
Примечание
Литература
- Читанава Т. В. Врождённый дискератоз // Генокарта. — 2019. — 23 сентября.
- Серебрякова И. С., Корнишева В. Г., Суслова И. Е., Фролова Е. В., Разнатовский К. И. Клинический случай врождённого дискератоза у мальчика 13 лет // Проблемы медицинской микологии. — 2024. — № 4. — doi:10.24412/1999-6780-2024-4-37-42.
- Ершов Н. М., Овсянникова Г. С., Хачатрян Л. А., Цетлина В. А., Сунцова Е. В., Байдильдина Д. Д., Татаринова О. С., Горонкова О. В., Шелихова Л. Н., Масчан М. А., Плясунова С. А., Коновалов Д. М., Терещенко Г. В., Сметанина Н. С. Врождённый дискератоз: анализ клинических случаев // Клиническая генетика в педиатрии. — 2014. — Т. 93, № 6. — С. 90—94.
- Amanda J. Walne, Inderjeet Dokal. Dyskeratosis Congenita: A historical perspective // Mechanisms of Ageing and Development. — 2008. — Январь (т. 129). — С. 48—59. — ISSN 0047-6374.
- Craig Garofola, Ali Nassereddin, Gary P. Gross. Dyskeratosis Congenita // StatPearls. — 2023-06-26.
- Evgeniy E. Bessonov, Andrey N. Surkov, Anna L. Arakelyan, Stanislav D. Getmanov, Natalia V. Zhurkova, Leyla S. Namazova-Baranova. The Course of Dyskeratosis Congenita Masked by Crohn’s Disease in a Primary School-Age Child: Case Report // Pediatric pharmacology. — 2025-01-09. — Т. 21. — С. 503–509. — ISSN 1727-5776 2500-3089, 1727-5776.
- Sharon A. Savage, Elizabeth F. Cook. Dyskeratosis Congenita and Telomere Biology Disorders: Diagnosis and Management Guidelines // International Telomere Biology Disorder Diagnosis and Management Guideline Development Group, Team Telomere. — 2018. — Июль.
- Julie Feldstein, Soledad Fernandez Garcia. The diagnosis and treatment of dyskeratosis congenita: a review // Journal of Blood Medicine. — 2014. — С. 157. — ISSN 1179-2736.