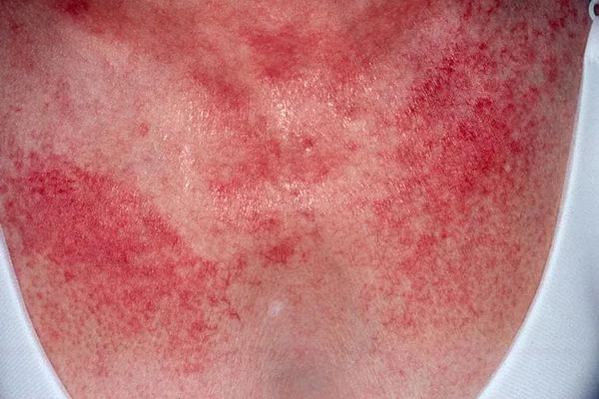
Синдром Киндлер
Синдро́м Ки́ндлер (Ки́ндлер-синдро́м, буллёзный эпидермо́лиз Ки́ндлер) — редкая форма врождённого буллёзного эпидермолиза, обусловленная мутациями в гене FERMT-1 (также известном как KIND1). Заболевание наследуется по аутосомно-рецессивному типу и характеризуется многообразием клинических проявлений, развивающихся с момента рождения и прогрессирующих с возрастом. Клиническая картина синдрома Киндлер включает образование пузырей на коже и слизистых оболочках с последующим рубцеванием, приводящим к контрактурам, псевдосиндактилии, микростомии и анкилоглоссии (короткая уздечка языка). Характерны фоточувствительность, генерализованная прогрессирующая пойкилодермия, поражения желудочно-кишечного тракта, а также нарушения со стороны урогенитального тракта. Отмечаются изменения ногтевых пластин, дистрофия зубочелюстной системы, гиперплазия дёсен, поражения слизистых оболочек ротовой полости и глаз. Диагностика синдрома Киндлер основывается на характерной клинической картины, семейном анамнезе, данных лабораторной диагностики и молекулярно-генетического исследования гена FERMT-1[1][2][3]. Синдром Киндлер был впервые описан в 1954 году Терезой Киндлер[4].
Что важно знать
История
Синдром Киндлер был впервые описан в 1954 году Терезой Киндлер[4]. В 2005 году Дж. А. Фишер с соавторами систематизировали клинические признаки синдрома на большие, малые и ассоциированные[2]. В 2008 году Киндлер-синдром был добавлен в классификацию буллёзного эпидермолиза и описан, как конкретная нозологическая форма, которая характеризуется наличием клинических фенотипических признаков, уникальных среди остальных форм врождённого буллёзного эпидермолиза[1]. По состоянию на 2016 год в мировой медицинской литературе было зарегистрировано около 400 случаев заболевания[5]. Согласно данным за 2015—2019 годы, в России под наблюдением находились более 480 пациентов с врождённым буллёзным эпидермолизом, из них синдром Киндлер был подтверждён у шести человек[6].
Этиология
Синдром Киндлер вызывается мутациями в гене FERMT-1 (также известном как KIND1), расположенном на коротком плече хромосомы 20 (20p12.3). Заболевание наследуется по аутосомно-рецессивному типу. Ген FERMT-1 кодирует белок киндлин-1 — мультидоменный фосфопротеин фокальной адгезии, который экспрессируется преимущественно в базальных кератиноцитах. Выделяют миссенс- и нонсенс-мутации, сплайсинговые мутации, инсерции, делеции, нуль-мутации, а также Alu-опосредованные перестройки. Эти мутации приводят к отсутствию белка киндлина-1 или продукции нефункционального белка. Имеются данные о корреляции типа мутации с тяжестью фенотипа: нуль-мутации вызывают более тяжёлое течение заболевания, тогда как миссенс-варианты и делеции в рамке считывания могут быть связаны с более лёгкими формами[6][7][8].
Патогенез
Киндлин-1 играет ключевую роль в формировании фокальных контактов между актиновым цитоскелетом клетки и внеклеточным матриксом, участвуя в активации интегринов и регуляции клеточной адгезии, миграции, пролиферации и полярности кератиноцитов. Дефицит или отсутствие функционального киндлина-1 нарушает интегрин-зависимую адгезию базальных клеток эпидермиса, что приводит к их дезорганизации, нестабильности дермо-эпидермального соединения и повышенной травматичности кожи. У пациентов наблюдается повышенная чувствительность к механическим воздействиям и ультрафиолетовому излучению, а также нарушение репарации ДНК. Эти механизмы лежат в основе развития буллёзных поражений, фоточувствительности и прогрессирующего атрофического дерматоза, характерных для синдрома Киндлер. Вариабельность клинических проявлений может быть обусловлена воздействием факторов окружающей среды[7][8].
Эпидемиология
Синдром Киндлер наследуется по аутосомно-рецессивному типу. Риск рождения больного ребёнка в семье носителей мутации составляет 25 %[9].
Диагностика
Диагностика синдрома Киндлер основывается на характерной клинической картины, данных лабораторной диагностики и молекулярно-генетического исследования гена FERMT-1[1][3].
Клинические проявления синдрома Киндлер дебютируют с рождения и включают образование пузырей на коже и слизистых оболочках. Буллы могут формироваться как в поверхностных, так и в глубоких слоях эпидермиса, что атипично для других форм буллёзного эпидермолиза. Наиболее часто пузыри возникают на тыльных поверхностях кистей и стоп, а также в области слизистых оболочек, в частности полости рта, пищевода и наружных половых органов. На месте булл могут формироваться эрозии. В последующем наблюдается их рубцевание с формированием контрактур, псевдосиндактилии, микростомии и анкилоглоссии. По мере взросления пузырей становится меньше, но на первый план выходит прогрессирующая пойкилодермия — сочетание атрофии кожи, телеангиэктазий и нарушений пигментации, развивающееся в том числе вне зон предшествующего повреждения. Почти у всех пациентов выявляется фоточувствительность, усиливающаяся при воздействии солнечного света и иногда ослабевающая с возрастом[1][10][11].
Значимыми являются и внекожные проявления. Со стороны желудочно-кишечного тракта типичны эзофагит, гастрит, колит, сужение пищевода, нарушения стула. Со стороны урогенитального тракта наблюдаются стриктуры уретры, влагалища, мочеточников[1][3][11]. Поражение слизистых приводит к затруднённому глотанию, мочеиспусканию и болевому синдрому. Нередко поражается слизистая ротовой полости: выявляется гиперплазия дёсен, лейкокератоз, кератотические бляшки, нарушение прорезывания зубов, кариес, периодонтит и постепенная потеря зубов вплоть до полной адентии[1][3][10].
Среди других поражений кожи и её придатков наблюдаются — дистрофия ногтевых пластин (истончение, искривление, дорсальный птеригиум), эктропион нижних век, ладонно-подошвенная кератодермия, псевдоангиум (циркулярные фиброзные перетяжки пальцев). Также может наблюдаться ангидроз или гипогидроз, скелетные аномалии (короткие пястные кости, аномалии рёбер, челюсти), лейкокератоз губ[1][3][10]. Во взрослом возрасте повышается риск развития плоскоклеточного рака кожи и слизистых оболочек, особенно в зонах хронического воспаления и рубцевания[1][3].
Согласно классификации Дж. А. Фишера r и соавторов выделяют большие, малые и ассоциированные признаки синдрома Киндлер[2][3]:
- большие признаки: раннее акральное образование пузырей, прогрессирующая пойкилодермия, атрофия кожи, фоточувствительность, структурная слабость и гиперплазия дёсен;
- малые признаки: псевдосиндактилия, поражение слизистых оболочек мочеполовой системы, анальной области, пищевода, гортани;
- ассоциированные признаки: дистрофия ногтей, эктропион нижнего века, ладонно-подошвенная кератодермия, псевдоангиум, лейкокератоз губ, ангидроз/гипогидроз, скелетные аномалии, нарушение прорезывания зубов, кариес, периодонтит, плоскоклеточный рак кожи и слизистых.
Диагноз считается достоверным при наличии у пациента четырёх больших признаков, вероятным — при сочетании трёх больших и двух малых признаков, возможным — при наличии двух больших и двух малых либо двух больших и двух ассоциированных признаков[2].
- Гистологическое исследование поражённых участков кожи — используется для подтверждения клинического диагноза и проведения дифференциальной диагностики между различными пузырными дерматозами. Дополнительное окрашивание базальной мембраны (PAS-реакция) позволяет выявить особенности базальной мембраны, что помогает отнести заболевание к определённому типу врождённого буллёзного эпидермолиза[3]
- Иммунофлюоресцентное антигенное картирование (ИАК) — с помощью ИАК можно не только определить основной тип буллёзного эпидермолиза, но и установить, какой именно белок, вероятнее всего, поражён мутацией. Данным методом определяется присутствие, отсутствие или сниженная экспрессия структурных белков кератиноцитов или дермо-эпидермального соединения, а также их распределение в пузыре и в коже пациентов. Он позволяет установить уровень образования пузырей и широко применяется как альтернатива электронной микроскопии. ИАК предоставляет быструю информацию о течении заболевания, его прогнозе и исходе, а также даёт основание для проведения молекулярно-генетического анализа. Метод позволяет косвенно уровень экспрессии дефектного белка, входящего в состав той или иной структуры, обеспечивающей связь эпидермиса и дермы[1][3].
- Реакция непрямой иммунофлуоресценции с использованием панели антител к разным компонентам дермо-эпидермального соединения (ламининам, цитокератинам 5 и 14, коллагенам VII и ХVII типов, плектину, десмоплакину, плакофилину, киндлину, интегринам) — позволяет выявить, какой именно белок повреждён, а также исключить участие других структур, минимизируя вероятность диагностической ошибки. В рамках антигенного картирования такой подход обеспечивает комплексную оценку, необходимую для точной диагностики подтипов буллёзного эпидермолиза[3].
- Трансмиссионная электронная микроскопия — позволяет детально исследовать ультраструктуру кожи и точно определить уровень формирования пузырей. С помощью электронной микроскопии можно выявить патологические изменения в кератиновых филаментах, десмосомах, полудесмосомах, а также якорных филаментах и фибриллах. При определённых формах врождённого буллёзного эпидермолиза эти структуры могут отсутствовать, либо содержаться в коже в недостаточном количестве, либо иметь дефектную структуру. Преимущество метода заключается в его высокой чувствительности: он способен обнаруживать тончайшие дефекты, которые могут быть незаметны при проведении ИАК, особенно при лёгких клинических формах заболевания[1][3].
- Молекулярно-генетическое исследование — выявление мутаций в гене FERMT-1[10]
Пренатальная диагностика проводится с целью раннего выявления генетических аномалий у плода и основывается на результатах генетического консультирования. Важнейшим условием является предварительное установление генетического дефекта у больного члена семьи — это позволяет целенаправленно искать мутацию у плода. Современные молекулярно-генетические методы позволяют проводить диагностику на основе анализа ДНК, полученной из ворсин хориона или амниотической жидкости. Среди методов — биопсия ворсин хориона (10—12 недель), амниоцентез (после 15 недель) и, реже, биопсия кожи плода (16—24 недели). Наиболее безопасной и информативной считается биопсия ворсин хориона, позволяющая получить результат в короткие сроки и при минимальном риске для матери и плода[1][3].
Однако, даже при точном знании мутации, диагностика может быть затруднена в случае мозаицизма — наличия у плода клеток с разным генетическим составом. Кроме того, инвазивные методы диагностики несут риск осложнений: выкидыша, инфицирования, излития околоплодных вод[3].
Показания к проведению пренатальной диагностики включают[3]:
- наличие в семье больного ребёнка;
- тяжёлые наследственные заболевания у родителей;
- близкородственные браки;
- случаи спонтанных абортов и мертворождений в анамнезе.
Дифференциальная диагностика
- простой буллёзный эпидермолиз,
- пограничный буллёзный эпидермолиз,
- дистрофический буллёзный эпидермолиз,
- эпидермическая пузырчатка новорождённых,
- световая оспа,
- рубцующийся пемфигоид,
- поздняя кожная порфирия,
- врождённая порфирия,
- энтеропатический акродерматит,
- буллёзное импетиго,
- кандидоз,
- герпес,
- эксфоллиативный дерматит Риттера фон Риттерсхайна,
- ихтиозиформная эритродермия,
- недержание пигмента,
- синдром Блума,
- синдром Коккейна,
- врождённый дискератоз,
- пойкилодермия Ротмунда — Томсона,
- пигментная ксеродермия,
- наследственная акрокератическая пойкилодермия Вери,
- сосудистая атрофическая пойкилодермия Якоби,
- сетчатая пигментная пойкилодермия Сиватта.
Осложнения
- анемия,
- кариес,
- адентия,
- стриктуры пищевода,
- остеопороз,
- плоскоклеточный рак кожи и слизистых оболочек.
Лечение
Специфической терапии синдрома Киндлер на сегодняшний день не существует. Лечение носит симптоматический характер и направлено на облегчение состояния пациента, предупреждение осложнений и повышение качества жизни.
Уход за кожей требует бережного отношения и ежедневной гигиены. Для обработки пузырей применяется антисептическая терапия: пузыри вскрывают стерильной иглой с сохранением покрышки, после чего участки кожи обрабатываются растворами хлоргексидина, метиленового синего, повидон-йода, фурацилина или фукорцина. Для ускорения заживления используются средства на основе декспантенола, диоксометилтетрагидропиримидина, солкосерила, актовегина, гиалуроната цинка и других регенерирующих препаратов[3][12].
Повязки должны быть неадгезивными, с мягкой текстурой, гипоаллергенными и воздухопроницаемыми. Используются силиконовые, гидрогелевые, абсорбирующие и антибактериальные повязки с минимальным трением[3][12].
Для предотвращения бактериальных осложнений и лечения вторичных инфекций применяются местные и системные антибактериальные препараты (клиндамицин, амоксициллин/клавуланат, фторхинолоны). А также антисептики для полости рта — хлоргексидин, гели стабилизирующие слизистую. При выраженном воспалении допускается кратковременное применение наружных кортикостероидов (бетаметазон, метилпреднизолон, триамцинолон). Для уменьшения зуда назначаются антигистаминные препараты (лоратадин, цетиризин). Болевой синдром купируется нестероидными противовоспалительными средствами (парацетамол, ибупрофен)[3][12].
Витаминная терапия включает витамины A, C, E, D3, а также витамины группы B и микроэлементы (железо, цинк), особенно при наличии признаков дефицита или для профилактики осложнений[3][12].
Рацион должен быть калорийным и богатым белком. Рекомендуется мягкая, щадящая пища — протёртые супы, каши, пюреобразные блюда, особенно при поражении слизистой полости рта или пищевода. Пища и напитки не должны быть слишком горячими или холодными[3][10].
В тяжёлых случаях, при наличии рубцовых стриктур пищевода, может потребоваться парентеральное или зондовое питание[3].
При развитии псевдосиндактилий, контрактур и других деформаций кистей или стоп возможно проведение реконструктивных операций. В случае формирования рубцовых стриктур пищевода проводится эндоскопическое бужирование или хирургическое расширение[3][10][12].
Прогноз
Прогноз при синдроме Киндлер относительно благоприятный. С возрастом количество пузырей, как правило, уменьшается, однако сохраняются фоточувствительность и пойкилодермия. Серьёзным осложнением является высокий риск развития плоскоклеточного рака кожи и слизистых оболочек, поэтому пациенты нуждаются в регулярном диспансерном наблюдении[8][9].
Диспансерное наблюдение
Динамическое наблюдение у дерматолога, педиатра, стоматолога, офтальмолога, отоларинголога, гастроэнтеролога, кардиолога, невролога, хирурга (по необходимости) с целью своевременного выявления патологий органов и систем, профилактики осложнений и коррекции проводимой терапии[1]. С подросткового возраста проводится ежегодный скрининг предраковых заболеваний и ранней плоскоклеточной карциномы[2].
Профилактика
- защиту кожи от травм и солнечных лучей,
- защиту от ультрафиолетового излучения,
- применение увлажняющих средств,
- регулярный уход за зубами,
- гигиену полости рта,
- мониторинг железодефицитной анемии,
- пренатальную диагностику, медико-генетическое консультирование,
- предотвращение стеноза глотки и пищевода с помощью диеты,
- регулярный осмотр всего кожного покрова,
- снижение возможности развития псевдосиндактилии — соблюдение правил бинтования стоп и кистей,
- сбалансированное питание,
- ношение свободной одежды из мягких натуральных тканей, без грубых швов и этикеток.