Синдром Блоха — Сульцбергера
Синдро́м Бло́ха — Су́льцбергера (пигме́нтная инконтине́нция, синдро́м недержа́ния пигме́нта) — редкое генетически детерминированное заболевание, манифестирующее в неонатальном периоде. Для него характерна классическая тетрада поражений: кожи, глаз, центральной нервной системы и зубов[1].
Что важно знать
История
Впервые синдром был описан английским врачом Гарродом А. в 1906 году, однако систематическое изучение началось лишь два десятилетия спустя. Своё название болезнь получила по именам швейцарского дерматолога Б. Блоха (1926 г.) и американского педиатра М. Сульцбергера (1929 г.), чьи работы стали ключевыми для её идентификации[1].
Классификация
Кожные проявления характеризуются стадийным течением, при котором отдельные стадии могут последовательно сменять друг друга или существовать одновременно[2]:
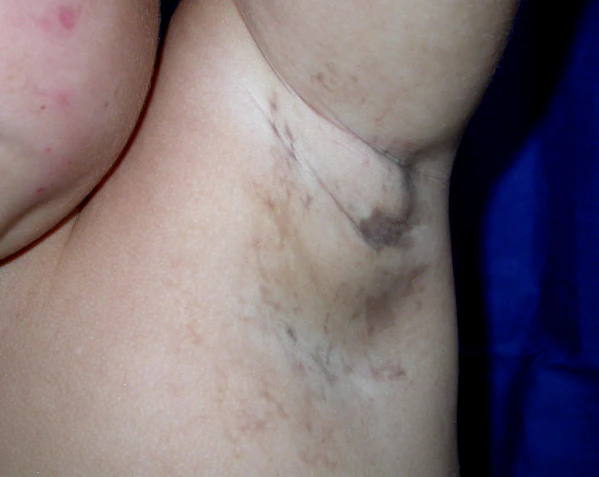
- I стадия, воспалительная (везикулобуллезная), проявляется возникновением везикулярных высыпаний на эритематозном фоне, расположенных строго по линиям Блашко. Эти поражения обычно появляются при рождении или в течение первых восьми недель жизни и сохраняются от двух недель до четырех месяцев. Типичная локализация включает конечности и туловище. Данные образования обычно регрессируют к 18-месячному возрасту, однако возможны рецидивы в более старшем возрасте даже после полного исчезновения, особенно на фоне лихорадочных состояний.
- II стадия, веррукозная, характеризуется появлением линейных бородавчатых папул и бляшек, расположенных вдоль линий Блашко, но не обязательно совпадающих с локализацией предыдущих воспалительных изменений. Поражения затрагивают дистальные отделы конечностей и волосистую часть головы. Кожные проявления второй стадии возникают в первые месяцы жизни, часто на фоне регрессирующих проявлениях первой стадии.
- II стадия, гиперпигментная, проявляется характерными вихревидными гиперпигментированными бляшками синевато-серого оттенка (напоминающими «мраморный торт»), расположенными по линиям Блашко и медленно регрессирующими. Эти высыпания отсутствуют при рождении и появляются в возрасте от 6 месяцев до 1 года на смену веррукозным поражениям. Основная локализация включает туловище, подмышечные впадины и паховую область, однако необходимо тщательное обследование всей поверхности кожи в связи с возможностью минимальных проявлений. Данные изменения обычно исчезают к подростковому возрасту.
- IV стадия, гипопигментно-атрофическая, характеризуется появлением бледных безволосых линейных пятен и бляшек с отсутствием потовых желез, наиболее часто локализующихся на задней поверхности голеней и предплечий. Указанные изменения отличаются хроническим персистирующим течением[2].
Этиология
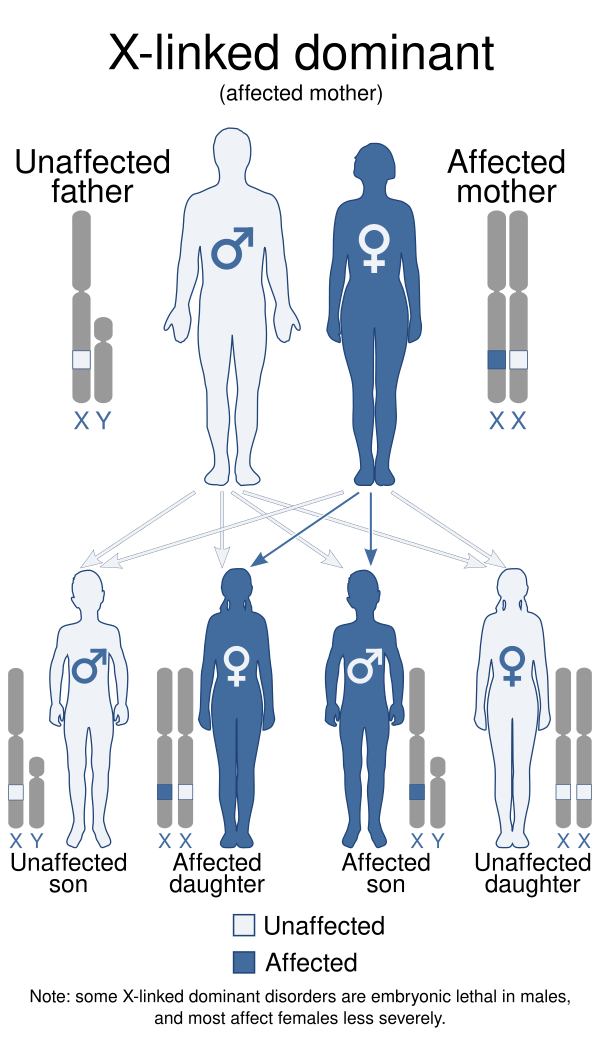
Пигментная инконтиненция представляет собой заболевание, наследуемое по Х-сцепленному типу. У большинства пациентов наблюдается вновь возникшая мутация в гене IKBKG, который также известен как ингибитор гамма-киназы каппа-В, или IKK-гамма, или важный модулятор NF-kappa-B (NEMO). Этот ген расположен на участке Xq28. Белок IKBKG активирует ядерный фактор каппа-бета-цепь-энхансер активированных В-клеток (NF-кB), который играет критическую роль в регулировании клеточных процессов: апоптоз, клеточный цикл, воспалительные реакции, иммунный ответ и многих других. В нормальных физиологических условиях NF-кB выполняет защитную функцию, предохраняя клетки от гибели. Он пребывает в клетках в неактивном состоянии и переходит в активную форму для инициации воспалительной реакции в ответ на такие угрозы, как бактериальная или вирусная инфекция, а также на клеточный стресс. Нарушение нормального функционирования белка IKBKG приводит к тому, что он теряет свою способность защищать клетки от запрограммированной клеточной гибели (апоптоза). Как следствие, в ответ на внешние или внутренние раздражители происходит чрезмерная гибель клеток. Вследствие доминантного характера наследования, сцепленного с Х-хромосомой, пигментная инконтиненция обычно приводит к летальному исходу у эмбрионов мужского пола во внутриутробном периоде развития (эмбриогенезе). Тем не менее в медицинской литературе зафиксированы случаи заболевания у лиц мужского пола. Это явление может быть объяснено такими механизмами, как соматический мозаицизм (присутствие в организме клеток с разным генетическим набором), гипоморфные мутации (мутации, лишь частично снижающие функцию гена), или наличием дополнительной Х-хромосомы, как это происходит, например, при синдроме Клайнфельтера. Женщины наследуют по одной Х-хромосоме от каждого из родителей, и в процессе раннего эмбриогенеза в их клетках происходит случайная инактивация одной из двух Х-хромосом (процесс, известный как лионизация). Однако инактивация одной Х-хромосомы происходит не во всех клетках одинаково. Таким образом, у женщин формируется функциональная мозаичность, означающая, что в их организме присутствуют две различные клеточные линии. Поражения кожи при данном заболевании развиваются строго вдоль так называемых линий Блашко. Эти линии визуально отражают путь миграции эмбриональных клеток-предшественников во время внутриутробного развития и в норме, при отсутствии пигментных аномалий кожи, остаются незаметными[2].
Патогенез
Патогенез синдрома Блоха — Сульцбергера детерминирован мутацией гена IKBKG (NEMO) в локусе Xq28, кодирующего регуляторный белок модулятора NF-κB. Данный белок является критическим компонентом сигнального каскада NF-κB, регулирующего экспрессию генов, ассоциированных с апоптозом, воспалением и клеточным выживанием. Наиболее частый генетический дефект — делеция экзонов 4—10 — приводит к синтезу нефункционального укороченного белка или его полному отсутствию, что обусловливает блокаду активации пути NF-κB. Следствием указанной блокады является утрата антиапоптотической защиты и повышенная чувствительность клеток, несущих мутантный аллель, к апоптозу в условиях воспалительных стимулов. Данный молекулярный механизм объясняет стадийность кожных проявлений. На буллёзной стадии наблюдается массовый апоптоз кератиноцитов с формированием интраэпидермальных пузырей и инфильтрацией эозинофилами. Веррукозная стадия характеризуется компенсаторной гиперплазией эпидермиса и гиперкератозом. На стадии гиперпигментации происходит деструкция базального слоя эпидермиса с высвобождением меланина и его фагоцитозом дермальными макрофагами. Финальная атрофическая стадия сопровождается дегенерацией меланоцитов и придатков кожи. Системные проявления, включая неврологические (эпилепсия, задержка развития), офтальмологические (ретинальная ишемия, неоваскуляризация) и стоматологические (адентия, конические зубы) аномалии, связаны с нарушением регуляции апоптоза, васкулогенеза и клеточной дифференцировки в процессе эмбрионального развития вследствие дисфункции NF-κB-зависимых сигнальных путей[3].
Эпидемиология
Синдром Блоха — Сульцбергера относится к группе системных меланобластозов. Частота синдрома составляет 1 на 10 000 девочек или 1 на 75 000 новорожденных. Болеют почти исключительно девочки, так как развитие патологии связано с Х-хромосомой, генная мутация летальна для плодов мужского пола[1].
Диагностика
Ключевым диагностическим критерием является наличие характерной прогрессирующей кожной сыпи, проходящей четыре классические стадии: везикулобуллёзную, веррукозную, гиперпигментную и атрофически-гипопигментную[4].
В ходе осмотра глазного дна выявляют ретинальную ишемию, неоваскуляризацию, кровоизлияния в стекловидное тело, а также атрофию зрительного нерва, которые являются частыми проявлениями заболевания[4].
Неврологическое обследование направлено на выявление структурных аномалий мозга (микроцефалия, пороки развития коры, кисты) и связанных с ними неврологических симптомов (судороги, задержка психомоторного развития)[4].
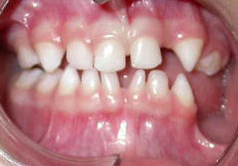
Стоматологический осмотр направлен на выявление частичной адентии, конической или уплощенной формы зубов, а также позднего прорезывания[4].
Молекулярно-генетическое исследование — золотой стандарт диагностики. Оно заключается в поиске делеции экзонов 4—10 гена IKBKG (NEMO) на Х-хромосоме (локус Xq28), которая составляет примерно 80 % случаев. При отсутствии данной делеции проводится полное секвенирование кодирующих последовательностей гена для выявления точечных мутаций. У пациентов мужского пола с кариотипом 46,XY и клиническими признаками пигментной инконтиненции необходимо исключение соматического мозаицизма или синдрома Клайнфельтера (47,XXY)[4].
При цитологическом исследовании патогномоничным признаком считается эозинофилия содержимого пузырей на первой стадии и феномен «рассыпанного пигмента» по типу завихрений и линий Блашко на третьей стадии[4].
Гистологическое исследование кожи на буллезной стадии выявляет интраэпидермальные пузыри со скоплениями эозинофилов, спонгиоз и апоптоз кератиноцитов; на веррукозной стадии — акантоз, гиперкератоз и дискератоз; на пигментной стадии — депигментацию базального слоя и наличие меланина в дерме со скоплениями меланофагов[4].
Дифференциальная диагностика
Дифференциальная диагностика требует учета стадийности кожных проявлений. На везикулобуллёзной стадии заболевание дифференцируют с врожденной герпетической инфекцией, для которой характерно появление сгруппированных геморрагических везикул на волосистой части головы и в местах травматизации кожи, а также с буллезным импетиго, буллезным эпидермолизом и врожденной ихтиозиформной эритродермией. На веррукозной стадии дифференциальный диагноз проводят с линейным эпидермальным невусом и линейным лишаем. Гиперпигментная стадия требует исключения линейного и вихревидного невоидного гипермеланоза. На атрофически-гипопигментной стадии дифференциация осуществляется с гипомеланозом Ито и очаговой гипоплазией дермы (синдром Гольца)[2].
Офтальмологические проявления, включая ретинальные васкулопатии с экссудацией и геморрагиями, необходимо дифференцировать с ретинопатией недоношенных, семейной экссудативной витреоретинопатией и болезнью Норри. Недержание пигмента признается одной из значимых причин лейкокории в детской офтальмологической практике[2].
Лечение
Этиотропной терапии, направленной на устранение генетической причины синдрома Блоха — Сульцбергера. Лечение носит мультидисциплинарный характер и является исключительно симптоматическим и профилактическим, направленным на купирование острых проявлений и предотвращение осложнений со стороны различных органов и систем[2].
Ведение пациента начинается с подтверждения диагноза и всеобъемлющего обследования для оценки степени вовлеченности кожи, нервной системы, органов зрения и зубочелюстной системы. На кожной везикулобуллезной стадии основной задачей является профилактика вторичной бактериальной инфекции. Для этого проводится тщательный уход за кожей с применением антисептических средств (например, хлоргексидина, растворов анилиновых красителей) и наложением асептических повязок. При признаках бактериального инфицирования назначаются топические или системные антибиотики на основе результатов бактериологического посева. В случаях выраженного воспалительного процесса и зуда могут применяться местные глюкокортикостероиды средней силы действия и антигистаминные препараты. Категорически противопоказано вскрытие пузырей в связи с высоким риском инфицирования[2].
Системное лечение может потребоваться при тяжелых, рецидивирующих формах заболевания. Описаны отдельные случаи успешного применения системных кортикостероидов в остром везикулярном периоде, однако их использование остается дискутабельным и должно быть взвешено против потенциальных побочных эффектов. При развитии резистентных форм может быть рассмотрен вопрос о назначении иммуносупрессивной терапии[2].
Неврологическое лечение направлено на контроль судорожного синдрома. Подбор противосудорожной терапии (вальпроевая кислота, карбамазепин, леветирацетам) осуществляется детским неврологом в соответствии с типом приступов и данными ЭЭГ. При структурных аномалиях мозга (пороки развития, кисты) может потребоваться наблюдение нейрохирурга[3].
При развитии пролиферативной ретинопатии выполняют лазерную фотокоагуляцию или криокоагуляцию периферических зон сетчатки для предотвращения отслойки сетчатки и сохранения зрения[2].
Стоматологическое вмешательство включает ортодонтическую коррекцию аномалий прикуса, вызванных частичной адентией или конической формой зубов. В дальнейшем может быть показано протезирование для восстановления функции жевания и эстетического вида[3].
Психологическая поддержка и реабилитация показаны пациентам с задержкой психомоторного развития и неврологическим дефицитом. Рекомендуется проведение занятий с дефектологом, логопедом, физиотерапия[2].
Прогноз
Прогноз для пациентов с синдромом Блоха — Сульцбергера определяется выраженностью висцеральных проявлений, преимущественно со стороны органа зрения и центральной нервной системы. Кожные изменения, несмотря на полиморфность клинической картины, не оказывают существенного влияния на общий прогноз заболевания. Наибольшие риски заболеваемости и смертности ассоциированы с офтальмологическими осложнениями, такими как ретинальные кровоизлияния, отслойка сетчатки и атрофия зрительного нерва, а также с неврологической патологией, включая резистентную эпилепсию, церебральные инфаркты и структурные аномалии развития головного мозга. Наличие труднокурабельных судорожных приступов и грубых органических поражений ЦНС коррелирует с высокой частотой задержки психомоторного развития и стойкого неврологического дефицита. Пациенты без значимого поражения сетчатки и центральной нервной системы имеют благоприятный прогноз с сохранной когнитивной функцией и нормальной ожидаемой продолжительностью жизни[2].
Диспансерное наблюдение
Диспансерное наблюдение пациентов с синдромом Блоха — Сульцбергера представляет собой комплексную систему пожизненного мониторинга и направленного обследования, осуществляемую мультидисциплинарной командой специалистов. Основной целью является динамическая оценка состояния органов-мишеней, раннее выявление и коррекция осложнений, а также медико-генетическое консультирование семьи[5].
Офтальмологический мониторинг проводится с частотой, определяемой тяжестью ретинопатии. В младенческом возрасте осмотр с обязательной офтальмоскопией при медикаментозном мидриазе выполняется ежеквартально до достижения 1 года, затем каждые 6 месяцев до 3 лет, а в дальнейшем — ежегодно при стабильном состоянии. При выявлении признаков ишемии периферии сетчатки или неоваскуляризации интервалы между осмотрами сокращаются[5].
Неврологическое наблюдение включает регулярную оценку психомоторного развития, электроэнцефалографический контроль при наличии судорожного синдрома и нейровизуализацию (МРТ головного мозга) при диагностике структурных аномалий. Частота осмотров определяется индивидуально, но не реже двух раз в год в раннем детском возрасте[5].
Дерматологический контроль необходим для оценки динамики кожных проявлений и подбора местной терапии в соответствии со стадийностью процесса. Осмотр проводится 1—2 раза в год, а также при обострениях[5].
Стоматологическое наблюдение предусматривает регулярные осмотры с момента прорезывания зубов для своевременной ортодонтической коррекции аномалий прикуса и планирования зубного протезирования[5].
Медико-генетическое консультирование направлено на разъяснение характера наследования заболевания, оценку рисков для потомства и обеспечение пренатальной диагностики при последующих беременностях[5].
Профилактика
Специфическая первичная профилактика синдрома Блоха — Сульцбергера не разработана ввиду генетической природы заболевания. Профилактические мероприятия носят вторичный характер и направлены на предотвращение развития тяжелых органных осложнений[6].
Примечания
Литература
- Анохина И. Г., Болгова И. В., Янченко Т. В., Иванова Е. В., Раскатова А. А., Елгина С. И., Рудаева Е. В., Мозес К. Б., Мозес В. Г., Черных Н. С. Синдром Блоха — Сульцбергера (клинический случай). // Мать и дитя в Кузбассе.— 2024.— № 3 (98).— doi:10.24412/2686-7338-2024-3-85-89.
- Yadlapati S, Tripathy K. Incontinentia Pigmenti (Bloch-Sulzberger Syndrome). 2023 Aug 25. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. PMID 35201722.
- Smahi, A., Courtois, G., Vabres, P., Yamaoka, S., Heuertz, S., Munnich, A., … & Israël, A. (2000). Genomic rearrangement in NEMO impairs NF-κB activation and is a cause of incontinentia pigmenti. Nature, 405(6785), 466—472.