Синдром Грисцелли
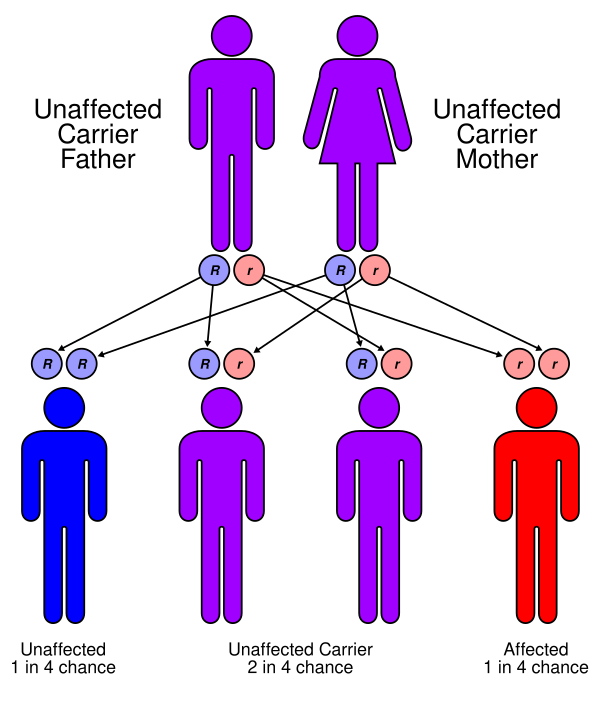
Синдром Грисцелли (СГ) — это редкое аутосомно-рецессивное заболевание, характеризующееся альбинизмом в сочетании с иммунодефицитом и неврологическими проявлениями. Заболевание проявляется частичным снижением пигментации кожи и волос, частыми инфекциями, неврологическими нарушениями и фатальным исходом вследствие неконтролируемой активации Т-лимфоцитов и макрофагов[1].
История
Синдром впервые был описан Клодом Грисцелли и его коллегами в 1978 году во Франции. В их исследовании описывались два пациента с частичным альбинизмом, частыми гнойными инфекциями и кризами, сопровождавшимися увеличением печени и селезёнки, а также снижением уровня нейтрофилов и тромбоцитов в крови. Позже этот фенотип был отнесён ко 2-му типу заболевания. В 1997 году была установлена связь синдрома с мутациями в гене MYO5A. Позже, в 2000 году, после открытия мутаций в гене RAB27A, впервые были чётко разграничены 1-й и 2-й типы синдрома. В 2003 году был описан 3-й тип заболевания, связанный с мутациями в гене MLPH[2].
Этиология
Существует три типа СГ:
- Тип 1 — это крайне редкий аутосомно-рецессивный синдром (в литературе описано около 10 случаев), cвязанный с мутациями в гене MYO5A, который кодирует белок миозин Va. Этот белок играет ключевую роль в транспорте меланосом и нейрональных везикул. Для данного типа характерен альбинизм с выраженными неврологическими отклонениями.
- Тип 2 вызван мутациями в гене RAB27A, который кодирует ГТФ-связывающий белок Rab27a. Этот белок участвует в регуляции экзоцитоза цитотоксических гранул в иммунных клетках. Для этого типа характерны характерны нарушения иммунитета со склонностью к развитию гемофагоцитарного синдрома.
- Тип 3 обусловлен мутациями в гене MLPH, который кодирует белок меланофилин. Этот белок участвует в формировании тройного комплекса с Rab27a и миозином Va для транспорта меланосом. При этом типе изменения пигментации развиваются изолированно[1][2][3].
Патогенез
Транспорт меланосом от центра клетки к её периферии представляет собой двунаправленный процесс, который осуществляется с помощью микротрубочек и моторных белков — динеинов и кинезинов. Ключевую роль в этом процессе играет тройной комплекс, состоящий из белков Rab27a, меланофилин и миозин Va.
Основные этапы транспорта меланосом включают:
- Rab27a связывается с меланосомами и активирует меланофилин .
- Меланофилин выступает в роли адаптерного белка, связывая Rab27a с миозин Va.
- Миозин Va — процессный моторный белок, который перемещает меланосомы по актиновым филаментам к периферии клетки.
Нарушение транспорта меланосом при СГ происходит, если любой из компонентов тройного комплекса дефектен. В результате:
- меланосомы не могут достичь периферии клетки и не передаются от меланоцитов к кератиноцитам;
- происходит накопление меланосом вблизи ядра (перинуклеарное накопление).
Это приводит к характерным клиническим проявлениям, таким как гипопигментация кожи и серебристо-серые волосы, что обусловлено нарушением передачи меланосом и их накоплением в меланоцитах[4].
Диагностика
Все три типа синдрома Грисцелли проявляются гипопигментацией, которая включает:
- серебристо-серые волосы;
- бледная кожа;
- изменения глаз, связанные с уменьшением пигментации.
При этой каждый из типов имеет свои особенности клинической картины:
- тип 1: тяжёлые неврологические нарушения, включая задержку развития, мышечную гипотонию и умственную отсталость, которые проявляются в раннем возрасте;
- тип 2: нарушение экзоцитоза цитотоксических гранул в Т-клетках и NK-клетках, что приводит к снижению цитотоксической активности. Это приводит к развитию гемофагоцитарного синдрома, который может быть спровоцирован вирусными инфекциями.
- тип 3: характерная только гипопигментация кожи и волос. Отсутствие неврологических или иммунных нарушений[4].
- микроскопия волос: скопление меланина в медуллярной части;
- биопсия кожи с гистологическим исследованием: скопление меланина в околоядерной зоне меланоцитов при бледности кератиноцитов[2].
- снижение цитотоксичности и дегрануляции Т-лимфоцитов и NK-клеток in vitro (2-й тип);
- подтверждение диагноза проводится методом секвенирования генов RAB27A, MYO5A и MLPH[2].
Лечение
При СГ 1-го типа специфическое лечение отсутствует, поскольку клинические проявления связаны с неврологическими изменениями. Тяжёлые неврологические нарушения, включая задержку психомоторного развития, являются необратимыми и сохраняются на протяжении всей жизни. Терапия в данном случае направлена на симптоматическую поддержку и улучшение качества жизни пациента[3].
Трансплантация гемопоэтических стволовых клеток является единственным потенциально радикальным методом лечения СГ 2 типа.
СГ 3 типа в терапии не нуждается.
Прогноз
Прогноз при СГ зависит от типа заболевания. При СГ 2 типа прогноз остаётся неблагоприятным. Без агрессивного лечения и трансплантации костного мозга заболевание обычно приводит к летальному исходу в течение 1-4 лет. После трансплантации у некоторых пациентов наблюдаются длительные ремиссии, однако часть пациентов погибает. Средний возраст смерти составляет 5 лет. При СГ 1 и 3-го типов прогноз выживаемости более благоприятный по сравнению с СГ 2 типа. При 1 типе отмечаются долгосрочные неврологические последствия и инвалидизация, а 3 тип протекает легче, с преимущественно кожными проявлениями и минимальными системными нарушениями[3].