Врождённая аплазия кожи
Врождённая аплази́я ко́жи (ВАК, лат. aplasia cutis congenita) — редкая врождённая аномалия развития, характеризующаяся отсутствием участков кожи при рождении[2][3]. Поражения могут локализоваться на любом участке тела, однако в большинстве случаев выявляются на волосистой части головы. Глубина дефекта варьирует от поверхностного отсутствия эпидермиса до утраты дермы, подкожной клетчатки и подлежащих тканей. Аплазия кожи может возникать de novo вследствие различных причин или может быть в составе синдромов[3]. Точные этиология и патогенез остаются неустановленными[4]. Клинические проявления варьируют: поражения могут быть одиночными или множественными, с различной глубиной и протяжённостью. Выделяют 9 типов ВАК по И. Дж. Фридену в зависимости от локализации и характера дефекта кожи и наличия сопутствующих аномалий[3]. Лечение ВАК зависит от площади и глубины[2].
Что важно знать
История
Аплазия кожи нижних конечностей была впервые описана в 1767 году М. Кордоном. А в 1826 году У. Кэмпбелл описал аплазию кожи волосистой части головы[5].
Классификация
Классификация ВАК по И. Дж. Фридену (1986 г.)[2][6]:
- I группа — ВАК волосистой части головы без аномалий или исключительно с изолированными аномалиями;
- II группа — ВАК с аномалиями развития конечностей;
- III группа — ВАК с эпидермальными невусами и невусами внутренних органов;
- IV группа — ВАК с эмбриональными деформациями;
- V группа — ВАК на фоне инфаркта плаценты;
- VI группа — ВАК с буллёзным эпидермолизом;
- VII группа — ВАК на конечностях без буллёзного эпидермолиза;
- VIII группа — ВАК, вызванная специфическими тератогенами;
- IX группа — ВАК, связанный с пороками развития.
Этиология
Этиология ВАК недостаточно изучена. Считают, что это заболевание развивается вследствие воздействия целого комплекса эндогенных и экзогенных факторов[2]. Заболевание может иметь как спорадический, так и наследственный характер; установлены аутосомно-доминантные и аутосомно-рецессивные формы[7]. В ряде случаев обнаружены мутации в генах BMS1, DLL4, KCTD1 и KCTD15, вовлечённых в процессы формирования структур нервного гребня. Аплазия кожи может быть частью различных генетических синдромов, включая синдром Адамса — Оливера, синдром Барта, синдром Сетлиса, синдром SCALP, синдром очаговой кожной дисплазии лица, окулоцереброкутанного синдрома и др[6][8]. Также ВАК может сочетаться с другими эмбриональными пороками — омфалоцеле, гастросхизис и расщелина позвоночника[5].
Экзогенные факторы включают воздействие тератогенных веществ (метимазол, карбимазол, мизопростол, вальпроевая кислота, бензодиазепины, метамизол натрия, диклофенак натрия), а также употребление кокаина и марихуаны. Развитию дефекта способствует курение матери во время беременности[2]. К дополнительным экзогенным факторам относят внутриутробные инфекции, включая инфекции, вызванные вирусом герпеса, сосудистые факторы (аплазия кожи при «бумажном плоде»), а также внутриматочные и родовые травмы или механические причины: адгезия амниотической мембраны, внутриутробное сдавление черепа прилегающими костями таза матери, инфаркт плаценты, амниотические перетяжки, ранний разрыв плодных оболочек[5][8].
ВАК нередко сочетается с невоидными пороками развития, включая невус сальных желёз, пламенеющий невус и эпидермальный невус[7].
Патогенез
Патогенез ВАК остаётся недостаточно изученным[4]. Считается, что аплазия кожи формируется в результате минимального дефекта закрытия нервной трубки[7].
Гистологически в зоне дефекта эпидермис отсутствует полностью; если дерма сохранена, она характеризуется недостатком эластических волокон и плотным коллагеном[5].
Эпидемиология
Распространённость ВАК варьирует от 1 до 3 случаев на 10 000 новорождённых и в среднем составляет 0,3 %[2].
Диагностика
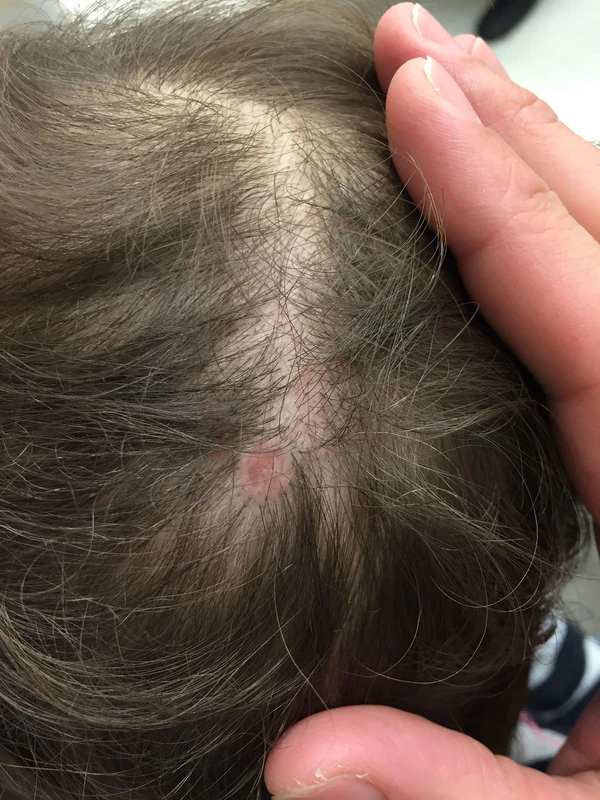
ВАК характеризуется наличием при рождении чётко ограниченного участка отсутствия кожного покрова, глубина и протяжённость которого значительно варьируют. В подавляющем большинстве случаев поражения располагаются на волосистой части головы, преимущественно в теменной области, по бокам от срединной линии. Однако дефекты могут возникать и на лице, туловище или конечностях (чаще в области коленей). На конечностях и туловище отмечается тенденция к симметричности очагов. Размеры очага колеблются от нескольких миллиметров до 10 см и более, чаще составляя 1—4 см. Форма дефектов неоднородна: наиболее часто они имеют округлые или овальные очертания, однако могут быть линейными, полосовидными или неправильной формы. У части пациентов регистрируются множественные очаги[5][6].
Одним из характерных клинических признаков считается симптом «волосяного воротничка» — пучок длинных тёмных волос, окружающий очаг аплазии[7].
Глубина поражения существенно варьирует — от изолированного отсутствия эпидермиса до вовлечения дермы, подкожной клетчатки, надкостницы и костных структур черепа. В редких случаях дефект распространяется на твёрдую мозговую оболочку и подлежащие мозговые структуры, что может сопровождаться энцефалоцеле, менингоцеле или гетеротопией мозговой ткани. Такие варианты протекают тяжело и ассоциированы с риском жизнеугрожающих осложнений. При поверхностных формах поражение может частично или полностью эпителизироваться ещё внутриутробно, формируя атрофические или фиброзные рубцы[4][5]. Крупные дефекты волосистой части головы могут сочетаться с нарушением целостности костей и повышенным риском рецидивирующих инфекций, кровотечений, эрозии саггитального синуса и менингита[5].
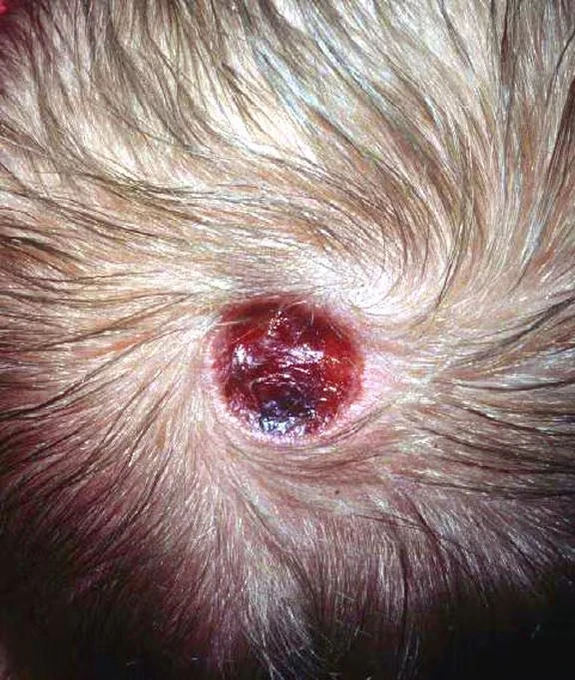
При рождении очаги выглядят как чётко ограниченные эрозии или язвы с красным, иногда гранулирующим дном. В ряде случаев дефект покрыт тонкой полупрозрачной мембраной, иногда заполненной серозной жидкостью и напоминающей волдырь. Буллёзный вариант представлен напряжённым пузырём или кистой на фоне отсутствия кожного покрова. После рассасывания пузырей формируются плоские атрофические рубцы, что позволяет рассматривать данный вариант как форму мембранозной аплазии кожи. У части новорождённых очаги напоминают буллёзный эпидермолиз, поскольку пузырьки быстро вскрываются, образуя раневую поверхность[5][6].
Заживление чаще происходит самостоятельно, с образованием атрофического, мембранозного или келоидного рубца. При наличии корок процесс заживления может длиться месяцы или годы[5][6].
Тяжёлые формы, особенно крупные дефекты волосистой части головы с разрушением костей, могут приводить к жизнеугрожающим состояниям. Описана смертность около 20 %, связанная с менингитом, кровотечениями, эрозией верхнего сагиттального синуса и дыхательной недостаточностью. В редких случаях отмечаются неврологические нарушения, включая спастический паралич и задержку психомоторного развития, обусловленные поражением подлежащих структур мозга[5].
- Гистологическое исследование поражённых участков кожи[5].
- Магнитно-резонансная томография головного мозга — проводится для выявления сопутствующих пороков развития костей и внутричерепных структур[8].
- Ультразвуковое исследование — можно использовать для оценки костных дефектов при более крупных поражениях передней черепной ямки[4].
- Дерматоскопия — может выявляться отсутствие фолликулярных отверстий, наличие телеангиэктатических сосудов и расположение волосяных фолликулов радиально и горизонтально по периферии, напоминающее «звёздочку»[6].
Дифференциальная диагностика
Дифференциальную диагностику следует проводить со следующими заболеваниями:
- невус сальных желёз;
- гнёздная алопеция;
- микозы волосистой части головы[7];
- дермоидная киста;
- изолированное энцефалоцеле;
- менингоцеле;
- узловая нейрональная гетеротопия;
- локализованная склеродермия;
- рубцовые алопеции;
- опухоли кожи головы;
- наследственный буллёзный эпидермолиз;
- эпидермальный невус;
- органоидные невусы[8];
- родовая травма;
- неонатальный герпес[6].
Осложнения
Лечение
Лечение аплазии кожи подбирается индивидуально и зависит от площади, глубины и расположения дефекта[3].
Небольшие (до 4 см) и поверхностные дефекты обычно заживают самостоятельно и требуют минимального вмешательства. Применяется бережное очищение с нанесением мягких увлажняющих или антибактериальных мазей, предназначенных для предотвращения высыхания раневой поверхности[2][6]. Для защиты поражённого участка применяются асептические и регенерирующие повязки[2][3].
В терапии также описаны методики, основанные на применении культивируемых эпителиальных аутотрансплантатов, биоразлагаемых матриц и клеточных технологий (трансплантация мультипотентных мезенхимальных стромальных клеток), которые используются с целью ускорения заживления и улучшения регенерации тканей. Основной фактор роста фибробластов применяется в консервативной терапии для ускорения заживления и предлагается в качестве средства для укрепления эпителия перед последующей реконструкцией[3][6].
Хирургическое вмешательство показано при крупных дефектах более 4 см, глубоком поражении с вовлечением дермы, подкожной клетчатки или кости, а также при угрозе осложнений. Применяются методы первичного закрытия, пластики кожными лоскутами и аутологичной или аллогенной кожной трансплантации. При отсутствии костных структур может потребоваться ранняя или отсроченная краниопластика[2].
Для реконструкции обширных дефектов на волосистой части головы используются тканевые расширители и ротационные лоскуты[4].
Прогноз
Прогноз зависит от глубины поражения и наличия сопутствующих аномалий или осложнений[6].
Диспансерное наблюдение
Индивидуально.
Профилактика
Профилактические меры при аплазии кожи включают раннее дерматологическое обследование новорождённых, наблюдение за возможными инфекционными осложнениями и своевременное проведение хирургического вмешательства при наличии показаний. Возможно проведение пренатальной диагностики[6].
Генетическое консультирование показано семьям с отягощённым наследственным анамнезом[8].
Примечания
| Правообладателем данного материала является АНО «Интернет-энциклопедия «РУВИКИ». Использование данного материала на других сайтах возможно только с согласия АНО «Интернет-энциклопедия «РУВИКИ». |