Мужской гипогонадизм
Гипогонади́зм у мужчи́н — клинико-биохимический симптомокомплекс, обусловленный дефицитом тестостерона, а также снижением чувствительности рецепторов к нему и его метаболитам, что приводит к патологическим изменениям в различных органах и системах, снижая качество жизни и ухудшая её прогноз[2].
Общие сведения
История
История изучения гипогонадизма как отдельного заболевания, требующего лечения, насчитывает более полутора веков. В 1849 году А. Бертольд в экспериментах по трансплантации яичек петухам впервые обосновал гуморальное влияние семенников на организм, заложив основы эндокринологии. В 1889 году Ш. Броун-Секар сообщил об омолаживающем эффекте самоинъекций вытяжки из яичек, что стимулировало интерес к гормональной терапии, хотя полученные им результаты, как предполагается, были связаны с эффектом плацебо. В 1935 году группа учёных компании Organon впервые выделила тестостерон и дала ему название. В том же году Адольф Бутенандт с коллегами, а также Леопольд Ружичка с коллегами независимо друг от друга осуществили химический синтез тестостерона из холестерина. Длительное время диагностика основывалась исключительно на клинических признаках. Современный этап изучения дефицита тестостерона начался в 1970-х годах с внедрением радиоиммунологического анализа, позволившего точно измерять концентрацию гормона в крови[3].
Классификация
По этиологии выделяют четыре типа гипогонадизма[2]:
- Первичный (гипергонадотропный) гипогонадизм: возникает при нарушении функции самих яичек, в то время как гипоталамо-гипофизарная функция сохранена.
- Вторичный (гипогонадотропный) гипогонадизм: обусловлен нарушением функции гипоталамо-гипофизарной системы при изначально интактных яичках.
- Смешанный гипогонадизм: диагностируется при сочетанном нарушении как гипоталамо-гипофизарной функции, так и функции яичек, а также в случаях нечувствительности рецепторного аппарата к андрогенам.
- Гипогонадизм, обусловленный нарушением отрицательной обратной связи «гипофиз-гонады»: этот тип развивается на фоне метаболических нарушений и отличается от первых трёх своей потенциальной обратимостью при устранении вызвавших его причин.
В качестве альтернативной классификации предлагается разделение на[2]:
- органический гипогонадизм: характеризуется наличием доказанной патологии, затрагивающей структуру или функцию любого уровня гипоталамо-гипофизарно-гонадной оси. Требует специфического лечения (гонадотропинами или тестостероном);
- функциональный гипогонадизм: возникает при отсутствии органических изменений в оси гипоталамус-гипофиз-гонады. Первоочередной задачей лечения является устранение или коррекция сопутствующих заболеваний и факторов, вызвавших это состояние.
Этиология
Первичный гипогонадизм является следствием дисфункции клеток Лейдига, что приводит к низкой концентрации тестостерона на фоне высоких гонадотропинов. Этиологические факторы включают[4]:
- наиболее частые: крипторхизм, травма яичек, орхит (например, паротитный — развивается у 25 % мужчин после полового созревания), последствия радио- или химиотерапии, возрастной гипогонадизм, а также синдром Клайнфельтера (кариотип 47,XXY или 48,XXX) — наиболее частая хромосомная анеуплоидия и причина первичного гипогонадизма;
- редкие причины: врождённая анорхия, гипоплазия клеток Лейдига вследствие инактивирующих мутаций рецептора лютеинизирующего гормона, миотоническая дистрофия, синдром Кеннеди.
Вторичный гипогонадизм возникает из-за недостаточной стимуляции яичек гонадотропинами (низкий или неадекватно нормальный уровень лютеинизирующего гормона и фолликулостимулирющего гормона) вследствие нарушений на уровне гипоталамуса или гипофиза. Подразделяется на[4]:
- врождённый:
- врождённый гипогонадотропный гипогонадизм — редкое состояние, вызванное изолированным дефицитом гонадотропин-рилизинг-гормона. При сочетании с аносмией называется синдромом Каллмана. Идентифицировано более 30 генов, мутации в которых вызывают данное состояние. Врождённый гипогонадотропный гипогонадизм может сочетаться с крипторхизмом, микрофаллосом, агенезией почек, потерей слуха, расщелиной губы или неба, скелетными аномалиями;
- сочетанный дефицит гормонов гипофиза и септо-оптическая дисплазия — выявляются в детстве, но дефицит гонадотропинов манифестирует отсутствием пубертата. Имеют генетическую природу (ряд генов, включая перекрывающиеся с врождённым гипогонадотропным гипогонадизмом).
- синдромы CHARGE, Барде — Бидля и Прадера — Вилли;
- врождённая гиперплазия надпочечников — редкая форма гипогонадотропного гипогонадизма, вызванная мутациями гена NR0B1, приводящая к ранней надпочечниковой недостаточности и отсутствию пубертата.
- приобретённый: развивается после завершения полового созревания вследствие повреждения гипоталамо-гипофизарной области (травмы, опухоли, воспаление, облучение, сосудистые нарушения, инфильтративные заболевания, последствия нейрохирургических вмешательств);
- функциональный: возникает при отсутствии органических изменений вследствие физического или эмоционального стресса, дефицита питания, системных заболеваний, приёма некоторых лекарств или рекреационных веществ, а также на фоне ожирения.
Патогенез
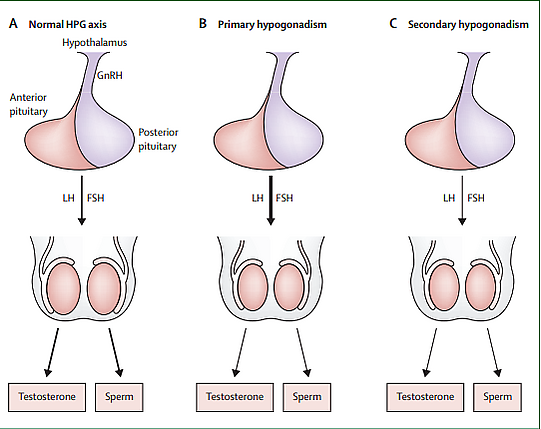
Гонады функционируют в составе гипоталамо-гипофизарно-гонадной оси. В аркуатном ядре гипоталамуса находится генератор импульсов, который высвобождает гонадотропин-рилизинг-гормон в портальную систему гипоталамуса и гипофиза. В ответ на эти импульсы аденогипофиз секретирует фолликулостимулирующий гормон и лютеинизирующий гормон, которые стимулируют активность гонад. Повышение концентрации половых гормонов подавляет секрецию фолликулостимулирующего гормона и лютеинизирующего гормона на уровне гипофиза, замыкая петлю отрицательной обратной связи. В яичках лютеинизирующий гормон стимулирует клетки Лейдига к секреции тестостерона, тогда как фолликулостимулирующий гормон необходим для поддержания функции семенных канальцев и сперматогенеза. Гипогонадизм может возникать при нарушении работы гипоталамо-гипофизарно-гонадной оси на любом уровне[5][6]:
- первичный гипогонадизм является следствием патологии самих яичек, которые не способны продуцировать достаточное количество тестостерона для подавления секреции лютеинизирующего гормона и фолликулостимулирующего гормона, что ведёт к их компенсаторному повышению;
- вторичный гипогонадизм обусловлен либо недостаточностью импульсной секреции гонадотропин-рилизинг-гормона гипоталамусом, либо неспособностью гипофиза адекватно секретировать лютеинизирующий гормон и фолликулостимулирующий гормон в ответ на стимуляцию. Чаще всего он наблюдается в рамках сочетанной недостаточности нескольких гормонов гипофиза, вызванной врождёнными пороками развития или приобретёнными поражениями гипофиза.
Независимо от уровня поражения, ключевым звеном патогенеза является дефицит тестостерона, который через андрогенные рецепторы оказывает многообразное системное действие. Снижение его биологических эффектов приводит к нарушению регуляции в различных органах и тканях[5][6].
Эпидемиология
Распространённость гипогонадизма у мужчин без сопутствующих хронических заболеваний составляет около 5 %. Однако при наличии сопутствующих хронических заболеваний, особенно висцерального ожирения и сахарного диабета 2 типа, распространённость гипогонадизма повышается до 30 %. Гипогонадизм часто остаётся недиагностированным, но при этом нередко подвергается избыточному лечению. Согласно исследованиям, примерно 40 % мужчин старше 45 лет и 50 % мужчин в возрасте 80 лет имеют гипогонадизм. Установлено, что концентрация тестостерона снижается в среднем на 100 нанограммов на децилитр каждые 10 лет. Распространённость гипогонадизма не зависит от расовой или этнической принадлежности[2][6].
Диагностика
К симптомам, с высокой долей вероятности указывающим на дефицит андрогенов, относятся снижение полового влечения, уменьшение количества спонтанных эрекций, выраженная утомляемость и вялость, выпадение волос в подмышечных впадинах и на лобке, изменения полей зрения, потеря обоняния, уменьшение объёма яичек, приливы жара, а также бесплодие, связанное с низким количеством сперматозоидов или их полным отсутствием. Менее специфичные проявления включают подавленное настроение, раздражительность, снижение концентрации внимания, увеличение доли жировой ткани в организме, уменьшение мышечной массы и физической работоспособности, снижение выносливости, потерю веса, упадок сил и ухудшение аппетита[6].
При физикальном обследовании необходимо подтвердить наличие обоих яичек и измерить их размеры. Максимальный размер яичка менее 4 сантиметров или объём менее 20 кубических сантиметров считается признаком уменьшения. Двусторонняя атрофия или отсутствие яичек с высокой долей вероятности указывают на гипогонадизм. Также следует оценить степень оволосения на лобке, в подмышечных впадинах и на лице и провести осмотр молочных желёз для выявления гинекомастии или болезненности. Следует обращать внимание на наличие врождённых аномалий развития половой системы, таких как гипоспадия, микропенис или крипторхизм[5][6].
Иммунохемилюминесцентный анализ крови: характерно снижение концентрации тестостерона ниже 8 нмоль/л при двукратном измерении утром. Возможно также повышение или снижение концентрации пролактина, фолликулостимулирующего и лютеинизирующего гормонов в зависимости от типа гипогонадизма[5][6].
Магнитно-резонансная томография головного мозга показана в случаях потери обоняния (аносмии) при подозрении на гипогонадотропный гипогонадизм, так как отсутствие обонятельных луковиц характерно для синдрома Каллмана. Кроме того, исследование назначается при любых вариантах гипогонадотропного гипогонадизма, как изолированного, так и сочетающегося с другими гипофизарными нарушениями[6].
Дифференциальная диагностика
Дифференциальная диагностика гипогонадизма проводится со следующими заболеваниями[5][6]:
- дефицит 3-бета-гидроксистероиддегидрогеназы;
- дефицит 5-альфа-редуктазы;
- гипоплазия надпочечников;
- синдром нечувствительности к андрогенам;
- нервная анорексия;
- врождённая дисфункция коры надпочечников;
- синдром Дениса — Драша;
- нарушения формирования пола;
- гиперпролактинемия;
- синдром Каллмана;
- идиопатический гипогонадотропный гипогонадизм;
- синдром Клайнфельтера;
- недостаточность питания;
- хроническая надпочечниковая недостаточность у детей;
- гипопитуитаризм у детей;
- гипотиреоз у детей;
- синдром Шерешевского — Тернера;
- депрессия;
- гиперпаратиреоз;
- злокачественные новообразования;
- атрофия яичек.
Осложнения
Помимо нарушений половой функции, гипогонадизм приводит к ряду серьёзных последствий[3]:
- костно-мышечная система: гипогонадизм является причиной вторичного остеопороза у мужчин, что проявляется низкой минеральной плотностью костной ткани и повышенным риском переломов;
- психоэмоциональная сфера: андрогенная недостаточность характеризуется снижением физической энергии и мотивации, подавленным настроением, раздражительностью, сонливостью, ухудшением внимания и памяти;
- система крови: тяжёлый дефицит тестостерона может приводить к развитию анемии;
- мышечная ткань и метаболизм: длительное снижение концентрации тестостерона вызывает уменьшение мышечной массы и силы, увеличение доли жировой ткани, центральное ожирение, ухудшение метаболического профиля, а также повышает риск развития сахарного диабета и метаболического синдрома.
- сердечно-сосудистая система: низкая концентрация тестостерона ассоциирована с повышением риска сердечно-сосудистых заболеваний, а также общей и сердечно-сосудистой смертности.
Лечение
Лечение гипогонадизма направлено на устранение симптомов дефицита тестостерона и профилактику осложнений. Основные цели терапии: улучшение настроения, физической формы, поддержание вторичных половых признаков, костной прочности и профилактика анемии. Наиболее часто используются трансдермальные гели и внутримышечные инъекции. Гель наносится ежедневно, обеспечивая стабильный уровень гормона. Инъекции бывают короткого и длительного действия. Короткие требуют введения каждые несколько недель и могут вызывать колебания самочувствия. Длинные вводятся раз в несколько месяцев, обеспечивая ровный фон. Выбор формы и режима терапии осуществляется индивидуально[4].
Диспансерное наблюдение
Диспансерное наблюдение за пациентами, получающими терапию тестостероном, направлено на контроль эффективности лечения и своевременное выявление возможных осложнений. Мониторинг клинических проявлений дефицита тестостерона рекомендуется проводить в первый год терапии один раз в три месяца, а в дальнейшем — ежегодно. Лабораторное обследование включает контроль клинического анализа крови: исходно, затем в первый год один раз в три месяца, далее ежегодно. Мужчинам старше 40 лет необходимо оценивать состояние предстательной железы с помощью пальцевого ректального исследования, ультразвукового исследования и определения общего простатспецифического антигена. Эти исследования проводятся исходно, в первый год терапии один раз в три месяца, а затем ежегодно. Также всем пациентам рекомендуется осмотр грудных желёз исходно, в первый год терапии один раз в три месяца, далее ежегодно. При подозрении или выявлении рака грудных желёз лечение тестостероном необходимо отменить[2].
Профилактика
Единый подход к профилактике гипогонадизма не разработан.
Примечания
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 3 4 5 Дедов И. И., Мокрышева Н. Г., Мельниченко Г. А., и др. Проект клинических рекомендаций «Синдром гипогонадизма у мужчин» // Ожирение и метаболизм. — 2021. — Т. 18, № 4. — С. 496—507. — doi:10.14341/omet12817.
- ↑ 1 2 Munari E. V., Amer M., Amodeo A., et al. The complications of male hypogonadism: is it just a matter of low testosterone? (англ.) // Frontiers in Endocrinology. — 2023. — Vol. 14. — P. 1201313. — doi:10.3389/fendo.2023.1201313.
- ↑ 1 2 3 Jayasena C. N., Anderson R. A., Llahana S., et al. Society for Endocrinology guidelines for testosterone replacement therapy in male hypogonadism (англ.) // Clinical Endocrinology. — 2022. — Vol. 96, no. 2. — P. 200—219. — doi:10.1111/cen.14633.
- ↑ 1 2 3 4 5 Vogiatzi M. V. Hypogonadism (англ.). Medscape (22 марта 2024). Дата обращения: 26 февраля 2026.
- ↑ 1 2 3 4 5 6 7 8 Sizar O., Leslie S. W., Schwartz J. Male Hypogonadism (англ.). Statpearls (25 февраля 2024). Дата обращения: 26 февраля 2026.
Литература
- Jayasena C. N., Anderson R. A., Llahana S., et al. Society for Endocrinology guidelines for testosterone replacement therapy in male hypogonadism (англ.) // Clinical Endocrinology. — 2022. — Vol. 96, no. 2. — P. 200—219. — doi:10.1111/cen.14633.
- Munari E. V., Amer M., Amodeo A., et al. The complications of male hypogonadism: is it just a matter of low testosterone? (англ.) // Frontiers in Endocrinology. — 2023. — Vol. 14. — P. 1201313. — doi:10.3389/fendo.2023.1201313.
- Дедов И. И., Мокрышева Н. Г., Мельниченко Г. А., и др. Проект клинических рекомендаций «Синдром гипогонадизма у мужчин» // Ожирение и метаболизм. — 2021. — Т. 18, № 4. — С. 496—507. — doi:10.14341/omet12817.