Синдром Чедиака — Хигаси
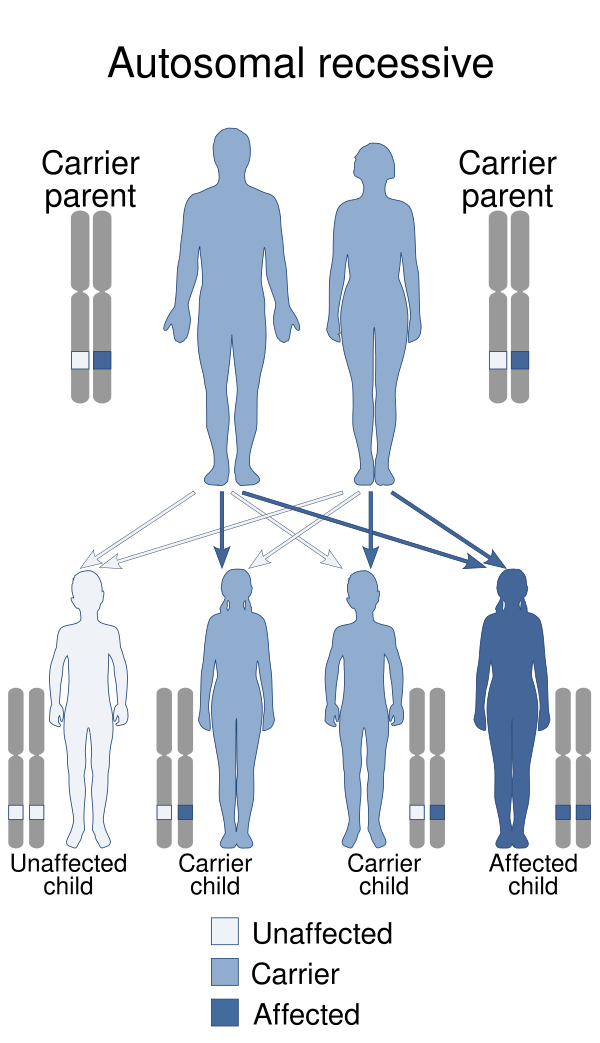
Синдро́м Че́диака — Хига́си — редкое аутосомно-рецессивное первичное иммунодефицитное заболевание, обусловленное мутацией в гене LYST, кодирующем белок-регулятор лизосомального транспорта. Нарушение функции этого белка приводит к дефекту лизиса фагоцитированных бактерий. Клинически заболевание проявляется рецидивирующими гнойными инфекциями бактериальной и грибковой природы, частичным кожно-глазным альбинизмом, косоглазием, нистагмом, светобоязнью, а также прогрессирующей периферической нейропатией и склонностью к кровотечениям вследствие тромбоцитарной дисфункции. Характерным морфологическим признаком синдрома является наличие гигантских пероксидазоположительных гранул в нейтрофилах, эозинофилах, моноцитах периферической крови, костного мозга и в клетках-предшественниках гранулоцитарного ряда[1][2][3].
Что важно знать
История
Синдром Чедиака — Хигаси впервые был описан в 1943 году испанским врачом Антонио Бегесом-Сесаром, наблюдавшим у ребёнка клиническую картину с повторяющимися инфекциями, альбинизмом и необычными клеточными включениями в лейкоцитах. В 1952 году кубинский гематолог Моисес Чедиак опубликовал данные о сходном клиническом случае, а в 1954 году японский педиатр Ота Хигаси независимо описал аналогичное заболевание. Впоследствии эти наблюдения были объединены, и заболевание получило название синдрома Чедиака — Хигаси. В 1980—1990-х годах, с развитием молекулярной генетики, была установлена причина заболевания — мутация в гене LYST, ответственном за регуляцию лизосомального транспорта[1][4].
Классификация
Синдром Чедиака — Хигаси классифицируют на основании патогенетических механизмов, лежащих в основе формирования иммунодефицита. Выделяют следующие формы[5]:
- лейкопеническая — развивается преимущественно под воздействием внешних факторов, таких как ионизирующее излучение, приводящее к угнетению костномозгового кроветворения и снижению количества лейкоцитов в периферической крови;
- дисрегуляторная — обусловлена нарушениями в регуляции клеточного иммунного ответа, включая дефекты в структуре фагоцитов, мембранных рецепторов и ферментных систем, что приводит к неэффективному устранению патогенов;
- дисфункциональная — включает как наследственные, так и приобретённые нарушения (мембранопатии, ферментопатии), а также дефекты структуры фагоцитов и иммуноглобулинов, что приводит к выраженному нарушению иммунитета.
В зависимости от клинического течения заболевания выделяют три формы[4][6]:
- Классическая (детская) форма;
- Атипичная (взрослая) форма;
- Акселерационная (ускоренная) форма.
Этиология
Синдром Чедиака — Хигаси представляет собой редкое аутосомно-рецессивное заболевание, возникающее в результате мутаций в гене LYST, локализованном на хромосоме 1q42.1 — q42.2. Продукт этого гена — цитозольный белок, участвующий в регуляции слияния и транспорта лизосом и других внутриклеточных везикул, включая меланосомы, азурофильные гранулы нейтрофилов и плотные гранулы тромбоцитов. Описано более 60 различных мутаций в гене LYST, включая миссенс-, нонсенс-мутации, а также делеции и инсерции, которые приводят к нарушению экспрессии или структуры соответствующего белка[6][7].
Патогенез
Синдром Чедиака — Хигаси характеризуется системным нарушением внутриклеточного транспорта, в первую очередь — в лизосомальных и секреторных гранулах. Основу патогенеза составляет дефект экзоцитоза и регуляции слияния везикул, вызванный мутациями в гене LYST. Эти мутации приводят к нарушению нормальной структуры и функции лизосомальных и секреторных органелл в клетках иммунной, кроветворной и нервной систем[1][7].
Морфологически у пациентов выявляются гигантские азурофильные гранулы в лейкоцитах, особенно в нейтрофилах, что связано с нарушением гранулогенеза. Эти аномальные включения формируются в результате слияния первичных и вторичных гранул, нарушая способность клеток к фагоцитозу и уничтожению патогенов. Иммунодефицит усугубляется снижением активности естественных киллеров (NK-клеток) и цитотоксических Т-лимфоцитов, что обусловливает высокую восприимчивость к бактериальным, вирусным и грибковым инфекциям[8][6].
Тромбоцитарные нарушения связаны с дефицитом плотных гранул, вследствие чего нарушается высвобождение факторов агрегации и удлиняется время кровотечения, что проявляется кожно-геморрагическим синдромом. Гранулы этих клеток оказываются нефункциональными и не способны адекватно выделять содержимое при сосудистой травме[6][7].
Неврологические проявления формируются вследствие накопления аномальных гранул в нейронах и глиальных клетках, приводя к дегенеративным изменениям центральной и периферической нервной системы. Эти изменения сопровождаются сенсомоторной нейропатией, атаксией, когнитивными расстройствами, паркинсонизмом, деменцией[8][6].
Одним из ключевых и наиболее опасных этапов патогенеза является развитие ускоренной фазы, соответствующей вторичному гемофагоцитарному лимфогистиоцитозу. Она характеризуется активацией макрофагов, панцитопенией и полиорганным поражением и наблюдается у большинства пациентов с классическим синдромом Чедиака — Хигаси[6][9].
Эпидемиология
Синдром Чедиака — Хигаси является крайне редким аутосомно-рецессивным наследственным заболеванием. Точная распространённость неизвестна в связи с существованием аномально мягких форм, однако за последние 20 лет зарегистрировано менее 500 случаев по всему миру. Заболевание не имеет выраженной расовой или этнической предрасположенности, обычно проявляется в раннем детском возрасте[8].
Клиническая картина
Синдром Чедиака — Хигаси характеризуется разнообразными клиническими проявлениями, связанными с нарушением функции лизосом в различных клетках организма. Заболевание, как правило, манифестирует в младенческом или раннем детском возрасте, нередко — уже в первые месяцы жизни[5][10].
Одним из характерных проявлений синдрома является глазокожный альбинизм. У пациентов наблюдаются светлая кожа, серо-голубые радужные оболочки, зрачок может иметь красный оттенок, выраженная фоточувствительность и снижение остроты зрения, светлые или серо-желтоватые волосы с серебристым оттенком[5][8].
Зрительные нарушения включают горизонтальный нистагм, астигматизм, косоглазие[11].
Отмечаются частые бактериальные инфекции, преимущественно стафилококковой и стрептококковой природы. Наиболее характерны рецидивирующие поражения кожи (гнойные пустулы, папулы, язвы, фурункулы, абсцессы), верхних дыхательных путей, ушей и лёгких — отиты, пневмонии, синуситы, гингивиты, стоматиты. Встречаются также вирусные (вирус герпеса человека 1, 2, 6-го типов, цитомегаловирус, вирус Эпштейна — Барр) и грибковые инфекции (кандидоз)[5][7].
Нарушение функции тромбоцитов, связанное с дефицитом плотных гранул, проявляется повышенной склонностью к кровотечениям: спонтанные носовые кровотечения, кровоточивость дёсен, обильные кровотечения при незначительных травмах или хирургических вмешательствах, легко формируются гематомы[7][12].
Неврологические нарушения разнообразны и прогрессируют с возрастом. У детей старшего возраста и подростков развиваются периферическая сенсомоторная нейропатия, атаксия, судороги, снижение когнитивных функций, мышечная слабость. Во взрослом возрасте описаны случаи паркинсонизма, деменции и энцефалопатий, ассоциированных с аутоиммунной дисрегуляцией[8][6].
В 50—85 % случаев развивается акселерационная фаза — гемофагоцитарный лимфогистиоцитоз. Это состояние характеризуется высокой лихорадкой, гепатоспленомегалией, панцитопенией и выраженной системной воспалительной реакцией. Эта фаза имеет тяжёлое течение и, при отсутствии трансплантации гемопоэтических стволовых клеток, заканчивается летально[1][13].
Диагностика
Диагностика синдрома Чедиака — Хигаси основывается на клинико-лабораторных данных, результатах инструментальных исследований, а также молекулярно-генетическом подтверждении мутаций в гене LYST[6].
- Клинический анализ крови — выявляются анемия, лейкопения, тромбоцитопения.
- Микроскопическое исследование окрашенного мазка периферической крови — обнаруживаются гигантские азурофильные гранулы в нейтрофилах, эозинофилах, лимфоцитах.
- Биохимический анализ крови — повышение концентрации ферритина и триглицеридов, снижение концентрации фибриногена; при поражении печени возможно повышение активности лактатдегидрогеназы, аспартатаминотрансферазы, аланинаминотрансферазы и концентрации общего билирубина.
- Молекулярно-генетическое исследование ДНК, выделенной из венозной крови — секвенирование гена LYST с последующим анализом на делеции или дупликации.
- Иммуноферментное определение концентрации иммуноглобулинов классов G, M, A в сыворотке крови — гипергаммаглобулинемия.
- Фенотипирование лимфоцитов методом проточной цитометрии — позволяет выявить нарушение созревания и дифференцировки лимфоцитов.
- Оценка цитотоксической активности NK-клеток методом проточной цитометрии — снижение активности естественных киллеров.
- Цитологическое исследование трепанобиоптата костного мозга — выявляются гигантские включения в клетках миелоидного ряда, а также признаки гемофагоцитоза при развитии ускоренной фазы.
- Гистологическое исследование биоптатов кожи — определяются макроглобулы меланина.
- Магнитно-резонансная томография головного мозга — могут выявляться диффузная атрофия вещества головного и спинного мозга, гиперинтенсивные участки в перивентрикулярной области, атрофия мозжечка и симметричное поражение бледного шара.
- Компьютерная томография головного мозга — при поражении нервной системы визуализируются диффузное снижение плотности перивентрикулярного белого вещества, расширение желудочков и субарахноидальных пространств, свидетельствующее об атрофии вещества головного мозга.
- Световая микроскопия волос — выявляются аномально крупные и неправильно распределённые меланосомы.
- Электронная микроскопия клеток крови — визуализируются гигантские лизосомы в гранулоцитах и тромбоцитах.
- Ультразвуковое исследование органов брюшной полости — диагностируется гепатоспленомегалия.
Дифференциальная диагностика
- Синдром Грисцелли II типа
- Синдром Германски — Пудлака II и IX типов
- Синдром дефицита MAPBPIP
- Синдром Кросса — Мак-Кьюсика — Брина
- Семейный гемофагоцитарный лимфогистиоцитоз
- Т-клеточная лимфома кожи[7][8]
Осложнения
- Лимфогистиоцитарная инфильтрация лимфатических узлов, печени и селезёнки
- Гемофагоцитарный лимфогистиоцитоз
- Злокачественные новообразования
- Тяжёлые рецидивирующие бактериальные инфекции
- Неврологические нарушения (сенсомоторная нейропатия, атаксия, паркинсонизм, деменция)[6][15]
Лечение
Единственным методом терапии, позволяющим скорректировать гематологические и иммунологические нарушения при синдроме Чедиака — Хигаси, является аллогенная трансплантация гемопоэтических стволовых клеток. Наибольшая эффективность достигается при проведении трансплантации до развития ускоренной фазы заболевания. Однако данный метод не предотвращает прогрессирования неврологических симптомов[7][13].
При развитии акселерационной формы необходимо предварительно добиться стабилизации состояния пациента. В таких случаях применяется иммуносупрессивная терапия, включающая этопозид, дексаметазон и циклоспорин А. При присоединении вируса Эпштейна — Барр может применяться ритуксимаб[7][6].
Поддерживающая терапия включает антибактериальные препараты, гамма-интерферон, глюкокортикостероиды. Применение антибактериальных средств направлено на профилактику и лечение инфекционных осложнений. Гамма-интерферон способствует повышению фагоцитарной активности. Пульс-терапия глюкокортикостероидными препаратами и спленэктомия в отдельных случаях позволяют достичь временной ремиссии. Для стимуляции гранулоцитарного ростка возможно применение гранулоцитарного колониестимулирующего фактора. Внутривенное введение иммуноглобулинов показано для компенсации недостаточности гуморального звена иммунитета[6][7][13].
При наличии геморрагического синдрома осуществляется коррекция гемостатических нарушений. Неврологические расстройства требуют симптоматического лечения. Применяются реабилитационные мероприятия. В случае развития паркинсонизма может использоваться леводопа. При фоточувствительности и нарушениях пигментации радужки рекомендуется применение корректирующих линз и солнцезащитных очков[8][6][7].
Прогноз
Прогноз при синдроме Чедиака — Хигаси крайне неблагоприятный при отсутствии специфического лечения. В большинстве случаев заболевание манифестирует в первые годы жизни и сопровождается тяжёлыми осложнениями. Большинство пациентов погибает в возрасте до 10—15 лет[1][12].
Трансплантация гемопоэтических стволовых клеток до наступления ускоренной фазы значительно улучшает прогноз. Пятилетняя выживаемость после процедуры составляет около 60 %. Однако даже после успешной трансплантации у пациентов могут сохраняться или прогрессировать неврологические нарушения[13][10].
Профилактика
Специфических мер первичной профилактики синдрома Чедиака — Хигаси не существует. Заболевание имеет аутосомно-рецессивный тип наследования, поэтому в семьях с отягощённым анамнезом рекомендовано проведение медико-генетического консультирования при планировании беременности[1].
Примечания
Литература
- Гундорова Л. В., Нажимов В. П., Масчан А. А. Синдром Чедиака-Хигаши с гемофагоцитарным лимфогистиоцитозом // Вестник Российского университета дружбы народов. Серия: Медицина. — 2000. — № 2.
- Зиновьева Ольга Михайловна, Батурская Ирина Петровна, Лысенко Татьяна Александровна, Проскурина Лариса Владимировна, Стародубова Наталья Викторовна, Просвирнова Ольга Геннадьевна. Случай диагностики первичного иммунодефицитного состояния у ребёнка раннего возраста // Амурский медицинский журнал. — 2017. — № 2 (18).
- Шаталова Е. Ю., Спичак И. И., Башарова Е. В., Рыжкова А. И., Васильева Л. А., Шилова Т. В., Куликовских О. В. Клинический случай синдрома чедиака-хигаси у ребёнка 4 лет // Педиатрический вестник Южного Урала. — 2016. — № 2.
- Yu.A. Rodina, V.E. Matveev, D.N. Balashov, M.E. Dubrovina, A.Yu. Shcherbina. Chediak–Higashi syndrome // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. — 2016. — Т. 15. — С. 27–33. — ISSN 2414-9314 1726-1708, 2414-9314.
- L. U. Ulukhanova, D. C. Amirkhanova, S. M. Attaeva, M. A. Ninalalov, N. C. Karnaeva. Clinical case: observation of a child with Chediak-Higashi syndrome // CHILDREN INFECTIONS. — 2023-04-01. — Т. 22, № 1. — С. 62–65. — ISSN 2072-8107.
- Roman J Nowicki. Chediak-Higashi Syndrome // Medscape. — 2019. — 7 июня.
- Camilo Toro, Marie Morimoto, May Christine Malicdan, David R Adams, Wendy J Introne. Chediak-Higashi Syndrome (англ.) // GeneReviews. — 2023-12-21.
- Aimee Molineux. What is Chediak-Higashi Syndrome? // News-Medical. — 2022. — 19 мая.