Синдром Эллиса — ван Кревельда
Синдро́м Э́ллиса — ван Креве́льда (хо́ндроэ́ктодерма́льная дисплази́я, ме́зоэ́ктодерма́льная дисплази́я, СЭВК) — редкое генетическое заболевание. Для него характерны аномалии развития скелета, укорочение конечностей, полидактилия и синдактилия. Также наблюдаются патологии ногтей, зубов и верхней губы. Часто встречаются врождённые пороки сердца, такие как дефект межпредсердной перегородки. Заболевание чаще всего вызвано мутациями в генах EVC и EVC2, наследуемыми по аутосомно-рецессивному типу[3].
Общие сведения
История
В конце 1930-х годов британский врач Ричард Эллис и голландский педиатр Симон ван Кревельд случайно встретились в поезде по пути на педиатрическую конференцию в Англии. Во время обсуждения своих исследований они обнаружили, что описанные ими пациенты имеют схожие симптомы — аномалии развития скелета, эктодермальные нарушения и пороки сердца. Это привело их к выводу, что речь идёт об одном и том же заболевании. В 1940 году Эллис и ван Кревельд официально описали эту патологию как хондроэктодермальную дисплазию, а впоследствии синдром получил их имена[3].
Этиология и патогенез
Синдром Эллиса — ван Кревельда в основном вызывается патогенными вариантами в двух генах — EVC1 и EVC2. Эти генетические изменения приводят к образованию аномально коротких белков EVC1 и EVC2. Хотя точная функция этих белков до конца не изучена, известно, что они локализуются на ресничках клеток и участвуют в правильном формировании костей и зубов. У некоторых пациентов с этим синдромом не обнаруживают мутации в данных генах, что позволяет предположить роль других генов (DYNC2LI1, GLI1, WDR35, DYNC2H1, PRKACA, PRKACB и SMO) в развитии заболевания[4].
Ген DYNC2LI1 кодирует белок, участвующий в высвобождении нейротрансмиттеров и обеспечивающий структурную поддержку нейронов. Гены WDR35, DYNC2H1, PRKACA, PRKACB и SMO кодируют синтез белков, необходимых для формирования и функционирования ресничек[4].
СЭВК, вызванный вариантами в генах DYNC2H1, DYNC2LI1, EVC, EVC2, GLI, SMO или WDR35, наследуется по аутосомно-рецессивному типу. В редких случаях (около 2 % пациентов), когда заболевание обусловлено вариантами в генах PRKACA или PRKACB, наблюдается аутосомно-доминантный тип наследования[4].
Эпидемиология
СЭВК является редким заболеванием. Точная распространённость остаётся неизвестной. Около 100 случаев было описано между первым полным описанием синдрома в 1940 году Эллисом и ван Кревельдом и 1968 годом. С 1968 года в литературе было зарегистрировано приблизительно 50 дополнительных случаев. СЭВК встречается с повышенной частотой среди общины амишей в США, где была описана самая крупная родословная: 52 случая в 30 семьях[5].
Диагностика
Пренатальные аномалии могут быть выявлены рано, после 18 недели гестации; они включают узкую грудную клетку, выраженное укорочение длинных костей, гексадактилию кистей и стоп и пороки сердца. Увеличение толщины воротникового пространства у плода в связи с СЭВК было описано на 13-й неделе гестации[5].
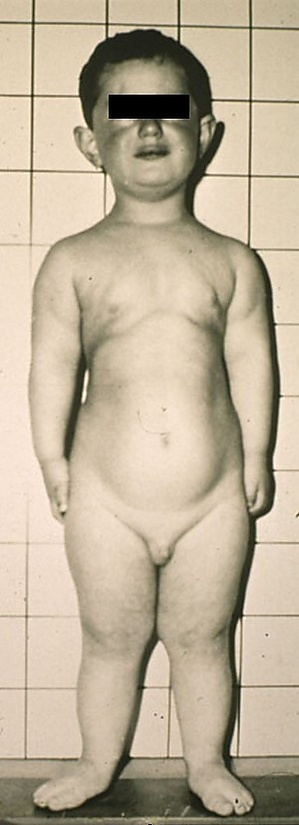
После рождения основными характерными признаками обычно являются[5]:
- диспропорционально низкий рост и укорочение средних и дистальных фаланг;
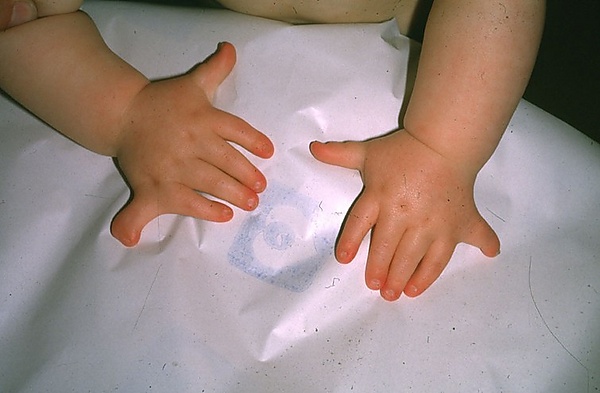
- полидактилия, затрагивающая кисти и, иногда, стопы;
- гидратическая эктодермальная дисплазия, преимущественно поражающая ногти, волосы и зубы;
- врождённые пороки сердца, встречающиеся примерно в 50—60 % случаев и включающие единое предсердие, дефекты митрального и трикуспидального клапанов, открытый артериальный проток, дефект межжелудочковой перегородки, дефект межпредсердной перегородки и синдром гипоплазии левых отделов сердца.
Спектр оральных проявлений широк и включает мальокклюзию, гипертрофию дёсен, гипертрофию уздечки, добавочные уздечки, зазубренные режущие края зубов, транспозицию зубов, диастему, конические зубы, гипоплазию эмали и гиподонтию. Зубы могут преждевременно прорезываться при рождении или преждевременно выпадать[5].
Некоторые непостоянные дополнительные клинические находки включают косоглазие, эписпадию и гипоспадию, крипторхизм, а также аномалии грудной стенки и лёгких[5].
Почечные аномалии встречаются в очень редких случаях и включают агенезию, дисплазию, мегауретер и нефрокальциноз[5].
Гематологические аномалии также редко описывались: один случай с дизэритропоэзом и другой, ассоциированный с перинатальным миелобластным лейкозом[5].
Рентгенологические признаки[6]:
- узкая грудная клетка с короткими рёбрами;
- короткие и утолщённые трубчатые кости;
- луковицеобразные концы проксимальных отделов локтевых и дистальных отделов лучевых костей;
- сращение костей запястья и пястных костей (обычно головчатой и крючковидной);
- конусовидные эпифизы фаланг;
- маленькие гребни подвздошных костей;
- выступы вертлужных впадин («трезубчатые» подвздошные кости);
- латеральный наклон большеберцового плато.
Диагноз СЭВК устанавливается у пациента с характерными клиническими признаками и биаллельными патогенными (или вероятно патогенными) вариантами в генах DYNC2H1, DYNC2LI1, EVC, EVC2, GLI, SMO или WDR35, либо гетерозиготным патогенным (или вероятно патогенным) вариантом в генах PRKACA или PRKACB выявленными с помощью молекулярно-генетического анализа[6].
Дифференциальная диагностика
Дифференциальная диагностика включает следующие синдромы:
- синдром Жёна (асимматричная торакохондродисплазия);
- орофациодигитальный синдром;
- синдром Мак-Кьюсика — Кауфмана;
- синдром Вейерса;
- синдром коротких рёбер и полидактилии;
- синдром Майнцера — Сальдино[6][7][8].
Лечение
При СЭВК лечение подбирается индивидуально в зависимости от проявлений: при полидактилии возможна хирургическая коррекция по желанию пациента, а при нарушениях опорно-двигательного аппарата проводится ортопедическая операция по показаниям. Если наблюдаются дыхательные нарушения, особенно у новорождённых, может потребоваться искусственная вентиляция лёгких. Параллельно назначается физиотерапия для улучшения двигательных функций, а при стоматологических проблемах — ортодонтическое или хирургическое лечение. Пациенты с врождёнными пороками сердца наблюдаются у кардиолога и при необходимости получают специализированное лечение. Дополнительно может потребоваться хирургическая коррекция мочеполовых аномалий, а при нарушениях слуха подбираются слуховые аппараты[6].
Прогноз
СЭВК характеризуется высокой смертностью в младенчестве и раннем возрасте из-за выраженных респираторных нарушений, вызванных короткими рёбрами и узкой грудной клеткой. Наличие врождённых пороков сердца также способствует ранней смертности. Около 33 % пациентов могут умереть в младенчестве или раннем возрасте из-за сердечно-сосудистой патологии. Описаны случаи длительной выживаемости пациентов: имеются сообщения о 15 случаях синдрома в семье с кровнородственными браками, где самый старший пациент достиг 82 лет[9].