Синдром Хоуэла-Эванса
Синдро́м Хо́уэла-Э́ванса (синдро́м Хо́уэла-Э́ванса — Кла́рка, тилёз с ра́ком пищево́да, керато́з ладо́ней и подо́шв) — крайне редкая форма врождённого ладонно-подошвенного гиперкератоза, наследуемая по аутосомно-доминантному типу. Заболевание обусловлено мутациями в гене RHBDF2 и ассоциируется с высоким риском развития рака пищевода. Различают два варианта клинического течения заболевания: при первом — наблюдается ограниченная кератодермия в первые месяцы жизни и протекает в лёгкой форме, при втором — гиперкератоз развивается в возрасте 5—15 лет с диффузным поражением ладоней и подошв. Диагностика основывается на клинической картине, семейном анамнезе, результатах гистологического исследования поражённых участков пищевода и кожи и подтверждения мутации RHBDF2 методом молекулярно-генетического анализа. Лечение носит симптоматический характер[1][2]
Что важно знать
История
Синдром Хоуэла-Эванса впервые был описан в 1958 году британскими исследователями У. Хоуэлом-Эвансом, К. А. Кларком и соавторами на основании наблюдений в двух крупных семьях из Ливерпуля. В дальнейшем, в 1994 году, была подробно изучена одна из этих семей, насчитывавшая 345 человек, из которых у 89 был диагностирован тилёз, причём 57 из них на тот момент были живы. Позднее было установлено, что обе семьи происходят от общего предка и представляют собой разные ветви одной родословной[1][3].
Классификация
Выделяют[4]:
- эпидермолитический (тип Вёрнера);
- неэпидермолитический тип синдрома Хоуэла-Эванса.
Также синдром Хоуэла-Эванса разделяют на[4]:
- тип A, который проявляется в возрасте от 5 до 15 лет и тесно связан с раком пищевода;
- тип B (ранний тип), который проявляется в первый год жизни и обычно протекает в лёгкой форме.
Этиология
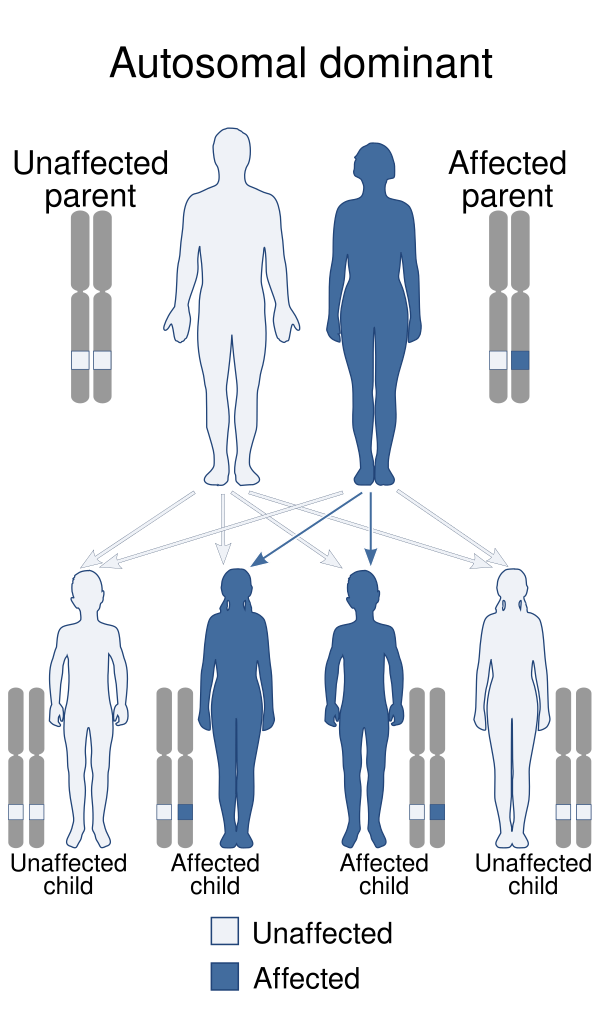
Синдром Хоуэла-Эванса вызывается мутациями в гене RHBDF2, расположенном на длинном плече 17-й хромосомы (17q25.1). Заболевание наследуется по аутосомно-доминантному типу. Ген RHBDF2 кодирует неактивный ромбовидный белок iRhom2, который регулирует работу сигнальных путей, включая путь эпидермального фактора роста (EGFR)[1][5].
Миссенс-мутации в гене RHBDF2 могут приводить к нарушению регуляции клеточного роста и обновления эпителия, особенно в пищеводе, что связано с повышенным риском развития плоскоклеточного рака. Белок iRhom2 также влияет на активность других белков, участвующих в восстановлении тканей и иммунных реакциях кожи и пищевода[1].
Факторы риска развития рака пищевода[1]:
- курение,
- употребление алкоголя.
Патогенез
В основе патогенеза лежит нарушение регуляции сигнального пути EGFR, связанное с мутациями в гене RHBDF2. Белок iRhom2 участвует в регуляции секреции лигандов, активирующих EGFR. Это приводит к нарушению процессов регенерации эпителия и повышенной склонности клеток пищевода к малигнизации.
Кроме того, iRhom2 взаимодействует с ромбовидной протеазой, регулирующей воспалительные и восстановительные процессы, в том числе расщепление белка тромбомодулина, участвующего в заживлении кожных повреждений. Мутации RHBDF2 также оказывают влияние на экспрессию фактора некроза опухоли альфа, что может снижать апоптоз и способствовать опухолевому росту.
Дополнительно, RHBDF2 и связанные с ним гены (RHBDD1[6], RHBDD2[7], RHBDF1[8]) вовлечены в развитие различных опухолей (желудка[9], молочной железы[7], яичников[10], лёгких[11], головы и шеи[8]) и некоторых других заболеваний, включая врождённые пороки сердца[12], глухоту[13], офтальмологические нарушения[14] и, возможно, диабет[15].
Гистологическая картина
При гистологическом исследовании поражённых участков пищевода у пациентов с тилёзом до развития рака специфические морфологические изменения, как правило, отсутствуют. Тем не менее, могут наблюдаться паракератоз, выраженные кератогиалиновые гранулы и воспалительный клеточный инфильтрат. Гистологическая картина поражённых участков кожи характеризуется акантозом, гиперкератозом и гипергранулёзом. При этом паракератоз и спонгиоз в эпидермисе обычно не выявляются[1].
Эпидемиология
Распространённость заболевания среди населения неизвестна, однако предполагают. что она составляет менее 1 случая на 1 000 000 человек[1].
Диагностика
Синдром Хоуэла-Эванса проявляется кожными и пищеводными симптомами. Основным кожным проявлением является ладонно-подошвенный гиперкератоз, при котором на ладонях и подошвах появляются жёлтоватые утолщённые бляшки в местах давления и трения. Эти изменения кожи, как правило, развиваются в возрасте от 5 до 15 лет. У детей в возрасте до одного года наблюдается ограниченная кератодермия. Также могут наблюдаться трещины, болезненность, вторичное инфицирование, гипергидроз, фолликулярные папулы на коже, а в отдельных случаях — полное или частичное отделение всех ногтей от ногтевого ложа на руках и ногах[1][2].
Наряду с кожными проявлениями возможно развитие лейкоплакии полости рта, чаще всего в области дёсен, а также родинок на губах. Хотя поражения слизистой оболочки рта обычно доброкачественные, описаны отдельные случаи развития рака ротоглотки[1][16][17].
Наиболее серьёзным осложнением синдрома является высокий риск развития плоскоклеточного рака пищевода — по данным наблюдений, он возникает у примерно 95 % пациентов к 65 годам[1][16]. При этом у некоторых больных на слизистой пищевода наблюдаются мелкие (2—5 мм) белесоватые полиповидные образования, рассеянные по всей длине органа. Эти изменения сами по себе не увеличиваются с возрастом, но могут служить маркёром риска неоплазии[1].
Симптомы развивающегося рака пищевода включают[1]:
- затруднённое глотание (дисфагия), сначала твёрдой, затем мягкой пищи и жидкостей;
- болезненное глотание (одинофагия);
- снижение аппетита, страх приёма пищи (ситофобия);
- потерю массы тела;
- при локализации опухоли в верхнем отделе — попёрхивание и кашель из-за аспирации.
На поздних стадиях возможны проявления метастатического процесса: одышка и кашель (при поражении лёгких), желтуха и асцит (при поражении печени), боли в костях, увеличение лимфатических узлов[1].
При этом у части пациентов злокачественная трансформация может протекать бессимптомно[1].
- Молекулярно-генетическое исследование — выявление мутаций в гене RHBDF2[1].
- Гистологическое исследование поражённых участков пищевода и кожи[1].
- Эзофагогастродуоденоскопия — выявляется видимый нарост, распространяющийся на различную глубину по стенке пищевода и по всей его длине. Он может быть плоским и напоминать бляшку или разрастаться, уменьшая просвет пищевода. Хромоэндоскопия — метод, при котором 20%-ный раствор йода распыляется через канюлю на слизистую оболочку пищевода. Участки дисплазии и опухолевые изменения выглядят как бледные зоны, не впитывающие йод[1].
- Компьютерная томография грудной клетки и брюшной полости — применяется для выявления регионарного и отдалённого метастазирования[1].
Дифференциальная диагностика
- болезнь Бушке — Фишера — Брауэра;
- ихтиоз Курта — Маклина;
- синдром Гамборга — Нильсена;
- синдром Хабера;
- наследственная точечная ладонно-подошвенная кератодермия;
- синдром Ядассона — Левандовского;
- фолликулярный кератоз;
- линейный кератоз с врождённым ихтиозом и синдромом склерозирующей кератодермии;
- кератодермия Меледа;
- гиперкератоз слизистой оболочки;
- синдром Негели — Франческетти — Ядассона;
- болезнь Наксоса;
- синдром Олмстеда;
- ладонно-подошвенная кератодермия и аногенитальный лейкокератоз;
- пандизавтономия;
- папилломатоз Гужеро — Карто;
- синдром Папийона — Лефевра;
- точечная порокератотическая кератодермия;
- тирозинемия II типа;
- синдром Шёпфа — Шульца — Пассажа;
- синдром Унны — Тоста;
- синдром Фовинкеля
Осложнения
Включают[1]:
- развитие плоскоклеточного рака пищевода,
- метастазирование.
Лечение
Лечение симптоматическое и включает меры по уходу за кожей, профилактику злокачественных новообразований и терапию уже развившихся опухолей[1]:
- Изменение образа жизни — включает коррекцию рациона с увеличением потребления свежих овощей и фруктов, отказ от курения и ограничение употребления алкоголя.
- Симптоматическое лечение гиперкератоза — включает регулярное применение смягчающих и увлажняющих средств, ношение специальной ортопедической обуви, а также лечение трещин и присоединившихся инфекций.
- Системная терапия — при выраженном утолщении кожи возможно применение пероральных ретиноидов (ацитретин). Эти препараты способствуют уменьшению толщины рогового слоя, однако могут вызывать побочные эффекты: сухость кожи и слизистых, носовые кровотечения, гиперлипидемию и нарушения функции печени.
- Лечение рака пищевода — зависит от стадии опухоли. При резектабельной опухоли проводится хирургическое вмешательство. В случае нерезектабельных новообразований применяется лучевая терапия с химиотерапией или без неё. При выраженной дисфагии может устанавливаться эндоскопический стент с целью облегчения приёма пищи и улучшения качества жизни пациента
Прогноз
Прогноз при синдроме Хоуэла-Эванса варьирует в зависимости от наличия и стадии рака пищевода. Риск развития плоскоклеточного рака пищевода к 65 годам оценивается в 95 %, однако выраженность кожных проявлений не коррелирует с онкологическим прогнозом. При развитии рака пищевода прогноз остаётся неблагоприятным: заболевание часто диагностируется на поздних стадиях (II—IV), когда уже имеется поражение регионарных лимфатических узлов. Общая 5-летняя выживаемость при таких формах рака составляет менее 5 %[1].
Диспансерное наблюдение
Профилактика
Не разработана.