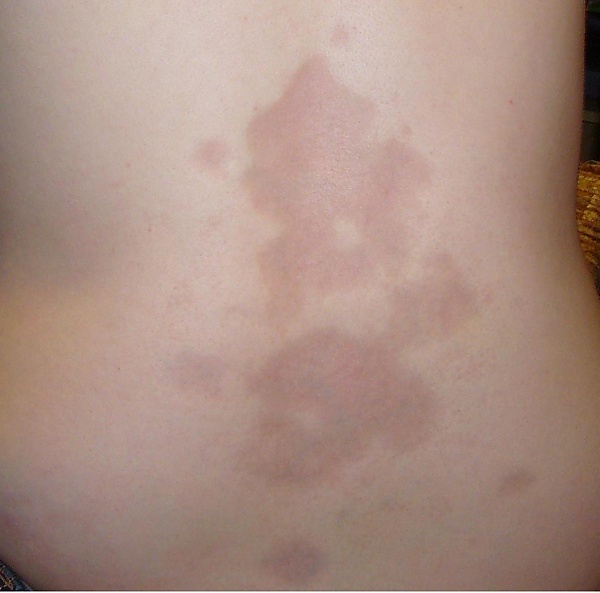
Локализованная склеродермия
Локализо́ванная склеродерми́я (очаго́вая склеродерми́я, ограни́ченная склеродерми́я, морфеа́, морфея́) — хроническое воспалительное иммунно-опосредованное заболевание соединительной ткани, ограниченное кожей и подлежащими тканями, характеризующееся очаговым утолщением, уплотнением и склерозом кожи вследствие избыточного синтеза и отложения коллагена. Заболевание рассматривается как мультифакториальное, при развитии которого важную роль играют сочетание генетических, иммунологических и внешних факторов. Ведущую роль играют аутоиммунные механизмы, сосудистые нарушения и активация фибробластов, приводящие к накоплению компонентов внеклеточного матрикса и формированию очагов склероза[2][3].
Клинические проявления локализованной склеродермии варьируют от единичных очагов поражения кожи до распространённых форм, при которых могут вовлекаться мышцы, фасции и кости. Выделяют несколько клинических вариантов заболевания: ограниченную, линейную, генерализованную, глубокую, пансклеротическую, буллёзную и смешанную формы. Диагноз устанавливается на основании характерной клинической картины, результатов гистологического и других лабораторных методов исследования[4]. Метод лечения зависит от клинического варианта локализованной склеродермии, глубины поражения и активности процесса[2].
Общие сведения
Классификация
Единой общепринятой классификации локализованной склеродермии нет. Чаще всего используют классификацию, основанную на клинических проявлениях[4]:
- Бляшечная.
- Буллёзная.
- Глубокая.
- Генерализованная (многоочаговая).
- Линейная.
В Российской Федерации применяется следующая классификация[4][5]:
- Ограниченная склеродермия (морфеа):
- бляшечная;
- каплевидная;
- узловатая (келоидоподобная);
- идиопатическая атрофодермия Пазини — Пьерини.
- Линейная склеродермия:
- в области головы (по типу «удар саблей»);
- в области конечностей и туловища;
- прогрессирующая гемиатрофия лица Парри — Ромберга.
- Генерализованная склеродермия.
- Буллёзная склеродермия.
- Глубокая склеродермия.
- Пансклеротическая склеродермия.
- Смешанная склеродермия.
Этиология
Причины возникновения локализованной склеродермии окончательно не установлены. Заболевание рассматривается как мультифакториальное, при развитии которого важную роль играют сочетание генетических, иммунологических и внешних факторов.
К числу провоцирующих факторов относят:
- травмы, механическое трение кожи, длительное давление;
- вакцинация;
- укусы насекомых;
- радиационная терапия[2];
- длительное переохлаждение;
- длительное сдавление мягких тканей (например, тугой одеждой);
- нарушения иммунной системы или метаболизма гормонов[4];
- бактериальные и вирусные инфекции, в частности, инфекцию, вызванную Borrelia burgdorferi (возбудитель болезни Лайма);
- инсоляция;
- некоторые лекарственные препараты, включая блеомицин и витамин K;
- ишемические повреждения тканей[5][6].
Описаны семейные случаи заболевания, что свидетельствует о возможной генетической предрасположенности. Наиболее значимые ассоциации выявлены с аллелями системы HLA — DRB1*04:04 и B*37[3].
Патогенез
Патогенез локализованной склеродермии является многофакторным и включает сложное взаимодействие различных механизмов, ведущих к нарушению дифференцировки фибробластов и избыточному образованию внеклеточного матрикса (коллагеновые волокна, фибронектин, эластин)[2].
Ключевую роль в развитии заболевания играют аутоиммунные нарушения. Аутоиммунный характер воспаления подтверждается выявлением аутоантител, а также сочетанием локализованной склеродермии с другими аутоиммунными заболеваниями, включая системную красную волчанку, витилиго, аутоиммунный тиреоидит и сахарный диабет 1-го типа. Ведущими патофизиологическими звеньями являются эндотелиальная дисфункция, воспалительная активация иммунных клеток и нарушение фибробластной регуляции. Повреждение эндотелия мелких сосудов сопровождается гиперплазией перицитов, уменьшением количества капилляров и аномалиями базальной мембраны, что приводит к развитию локальной ишемии. В ответ на эндотелиальное повреждение происходит активация Т-лимфоцитов и моноцитов, сопровождающаяся повышением экспрессии молекул адгезии — молекула адгезии сосудистых клеток-1, молекула внутриклеточной адгезии-1 и E-селектина. Эти молекулы задействованы в привлечении воспалительных Т-хелперных клеток 2-го типа, моноцитов и других иммунных клеток с увеличением секреции профибротических цитокинов — интерлейкинов ИЛ-2, ИЛ-4, ИЛ-6, ИЛ-8, ИЛ-10, ИЛ-13, фактора некроза опухоли-альфа, а также трансформирующего фактора роста бета (TGF-β), тромбоцитарного фактора роста и фактора роста соединительной ткани[2][3][5].
Указанные медиаторы индуцируют активацию фибробластов, стимулируют синтез коллагена, фибронектина и других компонентов внеклеточного матрикса. TGF-β оказывает двойное действие: усиливает синтез коллагена и подавляет активность матриксных металлопротеиназ, ответственных за деградацию коллагена, что способствует накоплению волокон в дерме и развитию фиброза[2][5].
Дополнительным механизмом фиброгенеза считается активация толл-подобных сигнальных путей под действием эндогенных лигандов, включая митохондриальную ДНК, фибронектин экстрадомен-A и тенаскин-C, которые также индуцируют TGF-β-зависимый фиброз. После активации TGF-β значимую роль приобретает фактор роста соединительной ткани, усиливающий фиброзные процессы[2].
На молекулярном уровне при локализованной склеродермии выявлены изменения экспрессии микроРНК: повышенная экспрессия miRNA-let-7a и сниженная экспрессия miRNA-196a ассоциируются с увеличением экспрессии коллагена I типа[2]. Отмечено также участие инсулиноподобного фактора роста, стимулирующего фибробластную активность[2].
Совокупность этих процессов приводит к хроническому воспалению и постепенному формированию фиброза кожи и подкожной клетчатки, сопровождающемуся утолщением, уплотнением и последующей атрофией тканей[2]. Морфологически процесс проходит три последовательные стадии: воспаление, индурация (уплотнение) и атрофия[4].
Патогенез локализованной склеродермии во многом схож с системным склерозом, поскольку обе формы характеризуются сходными патоморфологическими изменениями кожи. Однако при локализованной склеродермии поражение ограничивается кожей и подлежащими тканями, в то время как при системной форме фиброз затрагивает также внутренние органы (лёгкие, сердце, ЖКТ и др.)[2].
Морфологические изменения зависят от стадии и глубины поражения[7]:
- ранняя (воспалительная) стадия: обнаруживаются плотный, гомогенизированный коллаген, скопления эозинофилов (особенно вокруг сосудов и придатков кожи), могут визуализироваться лимфогистиоцитарный воспалительный инфильтрат с включениями фибробластов в периаднексальном и периваскулярном пространствах, вакуолизация эндотелия сосудов дермы и сужение их просвета;
- фиброзная (поздняя) стадия: характерен интенсивный фиброз в дерме, который постепенно замещает жировую ткань, дермальный коллаген эозинофилен, гомогенизирован, уплотнён. По мере прогрессирования наблюдается тенденция к замещению придатков кожи соединительной тканью, сосуды подкожной клетчатки имеют утолщённую стенку и суженный просвет.
Эпидемиология
Локализованная склеродермия является редким заболеванием кожи, встречающимся у представителей всех рас, но наиболее часто — у лиц европеоидного происхождения. Распространённость заболевания составляет от 0,3 до 3 случаев на 100 000 человек[6].
Женщины болеют значительно чаще мужчин, соотношение составляет 2,6—6:1[6]. Заболевание может развиться как в детском, так и во взрослом возрасте, демонстрируя бимодальное распределение по возрасту: первый пик приходится на детский возраст (7—11 лет), второй — на взрослый период (около 40—50 лет)[2][6].
У детей преобладает линейная форма локализованной склеродермии, составляющая до 90 % случаев в возрасте 2—14 лет, тогда как у взрослых наиболее часто встречается бляшечная форма (43,9 %), обычно встречается в возрасте от 40 до 50 лет[5][6]. Смешанные формы выявляются примерно у 15 % пациентов[5].
Распространённость локализованной склеродермии в Российской Федерации в 2018 году составила 15,9 случая на 100 000 населения, а заболеваемость — 4,1 случая на 100 000 населения[5].
Диагностика
Диагноз устанавливается на основании физикального обследования кожи с визуальным осмотром и пальпацией очагов поражения. При затруднении физикальной диагностики подтверждается результатами лабораторных методов исследования[5].
Клиническая картина локализованной склеродермии отличается значительным полиморфизмом и определяется глубиной поражения, стадией развития патологического процесса и клиническим подтипом заболевания.
В типичных случаях заболевание начинается с появления на коже пятен розовой, розовато-сиреневой или гиперпигментированной окраски округлой либо линейной (полосовидной) формы, нередко с явлениями отёка. Очаги поражения проходят три последовательные стадии: эритемы/отёка, склероза (индурации) и атрофии кожи. В стадии склероза формируются плотные участки уплотнения цвета слоновой кости с гладкой поверхностью и характерным восковидным блеском; по периферии нередко определяется розовато-сиреневый или лиловый воспалительный венчик («сиреневое кольцо»), указывающий на активную стадию процесса. Кожа в очагах плохо собирается в складку, потоотделение уменьшено или отсутствует, нарушается функция сальных желёз и рост волос. На стадии атрофии наблюдаются истончение кожи, телеангиэктазии, гипопигментация или гиперпигментация, атрофия дермы и подкожно-жировой клетчатки. Стадийность заболевания наблюдается не у всех пациентов[2][5].
Заболевание может сопровождаться субъективными ощущениями зуда, покалывания, болезненности, чувства стянутости кожи, ограничением подвижности в суставах и деформацией поражённых участков тела. В отдельных случаях отмечается спонтанная ремиссия с частичным или полным разрешением очагов, однако нередко остаются атрофические и пигментные изменения[5].
У ряда пациентов в очагах могут образовываться пузыри (буллы) с прозрачным или геморрагическим содержимым. При глубоком распространении процесса в патологический очаг вовлекаются подкожная клетчатка, фасции, мышцы и даже костная ткань[5].
Наиболее частый вариант заболевания у взрослых. Характеризуется появлением на коже туловища или конечностей округлых либо овальных эритематозных пятен, которые в дальнейшем трансформируются в плотные бляшки желтовато-белого или цвета слоновой кости с лиловым краем. По мере прогрессирования в центре формируется плотный участок индурации, а по периферии сохраняется активная воспалительная зона. Со временем бляшки подвергаются обратному развитию с формированием атрофии, телеангиэктазий и диспигментации[2].
Признаками активности считаются появление новых очагов, увеличение размеров существующих и усиление уплотнения кожи. Признаками угасания бляшек при длительном их существовании являются диспигментации (гипопигментация или гиперпигментации), атрофия эпидермиса с блестящей кожей и видимыми кровеносными сосудами, атрофия дермы и подкожно-жировой клетчатки, выпадение волос, потеря потовых желёз[2].
Встречается примерно у 5 % пациентов, у взрослых и детей. Процесс затрагивает глубокие слои соединительной ткани с вовлечением подкожно-жировой клетчатки, фасций и иногда мышц. Очаги представлены плотными, чётко очерченными участками с глубокой индурацией, чаще симметрично расположенными на нижних конечностях. При прогрессировании возможно развитие контрактур, артралгий, артритов, миалгий и атрофии подлежащих тканей[2].
Диагностируется при наличии четырёх и более индуративных очагов диаметром более 3 см, поражающих не менее двух анатомических областей из семи возможных (голова/шея, правая и левая верхняя конечности, правая и левая нижние конечности, передняя и задняя поверхность туловища). Очаги часто симметричны, склонны к слиянию, поражают туловище и конечности, не затрагивая лицо, кисти и стопы[2].
Наиболее тяжёлая и инвалидизирующая форма заболевания, при которой поражаются все слои кожи и подлежащие ткани вплоть до костей. Часто развивается в детском возрасте, быстро прогрессирует и резистентна к терапии. Характерны обширные участки индурации, язвообразование, кальцификация, контрактуры суставов и деформация конечностей. Несмотря на глубокое поражение тканей, внутренние органы обычно не вовлекаются в процесс[2][5].
Наиболее распространённая форма у детей (до 65—70 % случаев). Представлена линейными очагами уплотнения кожи, расположенными вдоль сосудисто-нервных пучков или по линиям натяжения кожи Блашко. Очаги поражения чаще всего возникают на голове или конечностях. При локализации на конечностях могут вызвать серьёзную задержку роста, атрофию мышц, сгибательные контрактуры, миозит, истончение поражённой конечности. На лице и волосистой части головы линейная склеродермия обычно выглядит в виде плотного тяжа склерозированной кожи, в которой отсутствует рост волос. Обычно располагается на лобно-теменной области, начиная от бровей до волосистой части головы. Может сопровождаться рубцовой алопецией, неврологическими нарушениями, поражением глаз[2][5].
Характеризуется линейным уплотнением кожи в парамедиальной области лба, нередко распространяющимся на волосистую часть головы и приводящим к рубцовой алопеции. Возможны офтальмологические, неврологические и одонтостоматологические нарушения (увеит, эписклерит, головные боли, судороги, невралгии, когнитивные расстройства)[2].
Редкий вариант, проявляющийся односторонней атрофией кожи, подкожной клетчатки, мышц и костей лица. Может сочетаться с линейной формой по типу «удар саблей». Заболевание развивается преимущественно в первые два десятилетия жизни. Часто сопровождается внекожными проявлениями — судорогами, мигренями, невралгией тройничного нерва, когнитивными нарушениями и офтальмологической патологией (энофтальм, офтальмоплегия, гетерохромия радужки, увеит)[2].
Характеризуется множественными мелкими (до 1 см) плотными папулами желтовато-белого цвета с блестящей поверхностью и лиловым венчиком, преимущественно на коже туловища. Иногда очаги возникают на фоне эритемы[5].
Проявляется образованием единичных или множественных узелков, напоминающих келоидные рубцы, но развивающихся без предшествующей травмы. Локализуется преимущественно на шее, туловище и верхних конечностях.
Рассматривается как поверхностный вариант локализованной склеродермии. Проявляется плоскими пятнистыми очагами розовато-красного или коричневого цвета с сиреневым оттенком без выраженного уплотнения кожи. Очаги чаще располагаются на туловище и конечностях, прогрессируют медленно, не сопровождаются воспалением[5].
Отличается образованием в очагах склеродермии пузырей (булл) с прозрачным или геморрагическим содержимым, которые могут вскрываться с образованием эрозий и корок[5].
Представляет собой сочетание признаков двух и более клинических вариантов (например, линейной и бляшечной, или генерализованной и линейной)[2]. Чаще встречается у детей[5].
Термин используется для обозначения локализованной склеродермии, развившейся в детском или подростковом возрасте. Клинически проявляется теми же формами, что и у взрослых, но чаще сопровождается внекожными симптомами — артралгиями, контрактурами, нарушением роста, сколиозом, асимметрией грудной клетки, а также неврологическими и офтальмологическими расстройствами (эпилептические припадки, мигрени, увеит, эписклерит)[2][5].
У взрослых внекожные симптомы чаще встречаются при линейной форме, особенно по типу «удар саблей» и при синдроме Парри — Ромберга. К ним относятся артралгии, артриты, миалгии, ограничение подвижности суставов, неврологические расстройства (головные боли, судороги, невралгии, когнитивные нарушения) и поражения органов зрения (увеит, эписклерит, косоглазие). У детей аналогичные проявления встречаются чаще, включая нарушения роста, сколиоз, контрактуры и офтальмоневрологические осложнения[2][5].
Для клинической оценки активности и выраженности кожных проявлений используется валидизированный индекс LoSCAT (Localized Scleroderma Cutaneous Assessment Tool), включающий два индекса[2]:
- mLoSSI (modified Localized Scleroderma Severity Index) — отражает признаки активности (распространённость, наличие эритемы, уплотнение кожи);
- LoSDI (Localized Scleroderma Damage Index) — оценивает степень повреждения с учётом признаков атрофии и нарушений пигментации.
Оценка проводится в 18 анатомических областях тела. Баллы для каждой анатомической области соответствуют наиболее высокому по каждому параметру[2].
- Общий анализ крови — может выявляться эозинофилия, особенно при генерализованной и линейной форме склеродермии; скорость оседания эритроцитов в норме или может быть повышена при активном процессе[2].
- Иммунологические исследования: антинуклеарные антитела выявляются у 23—68 % пациентов, чаще у детей; при этом специфические аутоантитела, характерные для системного склероза, как правило, отсутствуют или обнаруживаются лишь у 5—15 % больных. Ревматоидный фактор может быть положительным у 15—60 % пациентов, преимущественно при линейной форме. Возможно выявление антител к одноцепочечной ДНК, антигистоновых и антифосфолипидных антител, чаще при генерализованных и линейных формах[2][6].
- Биохимический анализ крови — при подозрении на миозит или поражение мышц показано определение концентрации креатинкиназы, лактатдегидрогеназы, С-реактивного белка. При линейной форме склеродермии наблюдается гипергаммаглобулинемия[5].
- При наличии в анамнезе укусов клещей рекомендуется серологическое обследование на Borrelia burgdorferi, поскольку боррелиоз может имитировать склеродермические поражения[5].
- Гистологическое исследование поражённых участков кожи[7].
- Ультразвуковое исследование кожи — позволяет оценить толщину и структуру дермы и подкожной клетчатки; в активной фазе определяется утолщение дермы с пониженной эхогенностью и повышенной эхогенностью в подкожной клетчатке. Применяется также для динамической оценки эффективности терапии[2].
- Инфракрасная термография демонстрирует связь между температурой кожных элементов и их клинической активностью[2].
- Дурометрия используется для количественной оценки плотности очагов, хотя менее информативна при поражении участков над костной тканью[2].
- Магнитно-резонансная томография показана при глубоких, линейных и пансклеротических формах для выявления поражения мышц, фасций и костей, а также при наличии неврологических или офтальмологических симптомов[2].
- Компьютерная томография применяется при линейных формах, локализованных на голове, для исключения поражения костей лицевого скелета, а также при тяжёлых генерализованных формах — для оценки вовлечения суставов и мышц[5].
- Электромиография используется для выявления мышечной дисфункции при линейной склеродермии[2].
- Дерматоскопия служит дополнительным методом для определения стадии активности очага (эритема, телеангиэктазии, степень атрофии)[5].
Дифференциальная диагностика
Состояния, от которых необходимо дифференцировать:
- системная склеродермия;
- липодерматосклероз;
- претибиальная микседема;
- соединительнотканный невус;
- склероатрофический лишай;
- склеродермоподобная форма базальноклеточной карциномы;
- Лайм-боррелиоз (атрофический акродерматит);
- склеромикседему;
- дерматофибросаркому выбухающую;
- гранулёматозный интерстициальный дерматит;
- поствоспалительная гиперпигментация;
- анетодермия[2];
- липоидный некробиоз;
- витилиго;
- панникулит;
- рубцовая алопеция[6];
- грибовидный микоз;
- лучевой дерматит;
- амилоидоз;
- липодистрофия;
- саркоидоз;
- нефрогенный системный фиброз[3];
- кольцевидная гранулёма;
- мигрирующая эритема;
- лекарственный дерматит[8];
- эозинофильный фасциит[9].
Осложнения
Лечение
Терапия локализованной склеродермии направлена на подавление воспалительной активности, замедление фиброзных изменений кожи и подлежащих тканей, а также на восстановление их эластичности и предотвращение функциональных нарушений. Выбор лечебной тактики определяется формой, глубиной и распространённостью процесса, возрастом пациента и наличием внекожных проявлений.
Основным методом лечения ограниченных поверхностных форм заболевания является местная терапия. Применяются местные глюкокортикоиды средней и высокой активности (флутиказон, мометазон, клобетазол, бетаметазон, метилпреднизолона ацепонат), которые наносят на очаги поражения ежедневно курсом от нескольких недель до трёх месяцев. В ряде случаев используется окклюзионная повязка для усиления действия препарата. Возможно также применение ингибиторов кальциневрина (такролимус). В терапию могут включаться препараты кальципотриола, а также средства, улучшающие микроциркуляцию и трофику тканей (мазь с депротеинизированным гемодериватом из крови телят)[5][8].
Системная терапия показана при генерализованных, линейных, глубоких и пансклеротических формах заболевания, а также при быстром прогрессировании или вовлечении глубоких тканей. Препаратом выбора является метотрексат, который применяется в индивидуально подобранной дозировке в течение шести и более месяцев. При выраженном воспалении и быстром прогрессировании болезни метотрексат комбинируется с системными глюкокортикостероидами (преднизолоном или метилпреднизолоном), которые используются в виде коротких курсов или пульс-терапии, с обязательным назначением фолиевой кислоты. В случаях недостаточной эффективности может применяться микофенолата мофетил. Дополнительно используются препараты, улучшающие микроциркуляцию и обменные процессы в соединительной ткани — пентоксифиллин, никотиновая кислота, ферментные препараты (гиалуронидаза)[4][5][8].
Рассматривается применение препаратов, воздействующих на сигнальные пути цитокинов (иматиниб, тоцилизумаб, абатацепт), а также ингибиторов JAK/STAT-пути (тофацитиниб, барицитиниб) и моноклональных антител к фактору роста соединительной ткани (памревлумаб)[2][8].
Также назначается фототерапия. Наиболее эффективной считается узковолновая УФА-1 терапия, она способствует снижению воспаления и позволяет уменьшить выраженность склероза. Применяется также ПУВА-терапия, преимущественно при поверхностных формах заболевания[5][8].
После купирования активности заболевания показаны физиотерапевтические методы, направленные на уменьшение плотности очагов и восстановление подвижности тканей: ультразвуковая терапия, электрофорез и фонофорез с гиалуронидазой, лазеротерапия, массаж и лечебная физкультура. Эти процедуры способствуют уменьшению фиброза, улучшению микроциркуляции и профилактике контрактур. В активной стадии заболевания их проведение противопоказано из-за риска усиления воспаления[5][8].
Хирургические методы применяются при стойких анатомических деформациях, выраженных косметических дефектах и функциональных ограничениях, развившихся вследствие хронического течения заболевания. Основное условие проведения оперативного вмешательства — стабильная клиническая ремиссия, поскольку активный воспалительный процесс значительно повышает риск рецидива и усугубления склероза[8].
Пластическая и реконструктивная хирургия показана при поражении лица и подкожных структур, особенно при линейной форме локализованной склеродермии типа «удар саблей» и синдроме Парри — Ромберга. В этих случаях применяются различные методы коррекции, включая краниопластику, установку имплантатов и аутотрансплантацию жировой ткани. Последний метод является предпочтительным, поскольку собственный жир не только восполняет объём, но и содержит мезенхимальные стволовые клетки, способные оказывать противофибротическое и восстанавливающее действие. При вовлечении конечностей возможно проведение ортопедических операций[8].
Прогноз
Прогноз обычно благоприятный: в течение 5 лет заболевание у большинства пациентов стабилизируется или переходит в ремиссию. В отдельных случаях процесс может приобретать хроническое течение и рецидивировать, особенно при линейных и генерализованных формах[9]. У детей заболевание протекает дольше и чаще сопровождается повторными обострениями[10].
Диспансерное наблюдение
Регулярное наблюдение врача с целью раннего выявления прогрессирования заболевания и своевременного назначения терапии[5].
Профилактика
Специфических мер профилактики не разработано. Пациентам рекомендуется избегать травматизации кожи, активной инсоляции, психоэмоционального перенапряжения, самостоятельного приёма лекарственных средств[5].