Лактатдегидрогеназа
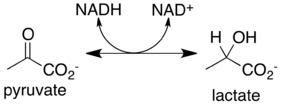
Лактатдегидрогеназа (L-лактат: NAD-оксидоредуктаза (LDH) 1.1.1.27) — фермент, принимающий участие в реакциях гликолиза[1]. Лактатдегидрогеназа катализирует превращение лактата в пируват, при этом образуется NADH.
Впервые лактатдегидрогеназа получена из отмытой мышцы Маергофом в 1909 году, а в 1940 году Штрауб получил её в кристаллическом виде.
Лактатдегидрогеназа устойчива к химическим воздействиям, например к действию реактивов, окисляющих или блокирующих сульфгидрильные группы, например йодоацетат и йодобензоат. Активность лактатдегидрогеназы снижается при повышении концентрации пирувата выше 10−4 М. Значительное инактивирование, обратимое при добавлении цистеина, происходит при инкубировании с парахлормеркурибензоатом.
Коферментом лактатдегидрогеназы является никотинамидадениндинуклеотид, сокращенно NAD. NAD — кофермент динуклеотидного типа, в котором два нуклеозид-5'-монофосфата соединены фосфоангидридной связью.
Анализ на ЛДГ входит в биохимический анализ крови. Нормы:
- новорожденные — до 2000 Ед/л
- дети до 2 лет — 430 Ед/л
- дети от 2 до 12 — 295 Ед/л
- дети старше 12 лет и взрослые — 250 Ед/л
Общие сведения
| Лактатдегидрогеназа | |
|---|---|
| Идентификаторы | |
| Шифр КФ | 1.1.1.27 |
| Номер CAS | 9001-60-9 |
| Базы ферментов | |
| IntEnz | IntEnz view |
| BRENDA | BRENDA entry |
| ExPASy | NiceZyme view |
| MetaCyc | metabolic pathway |
| KEGG | KEGG entry |
| PRIAM | profile |
| PDB structures | RCSB PDB PDBe PDBj PDBsum |
| Gene Ontology | AmiGO • EGO |
| Поиск | |
| PMC | статьи |
| PubMed | статьи |
| NCBI | NCBI proteins |
| CAS | 9001-60-9 |
| Лактатдегидрогеназа A (субъединица M) | |
|---|---|
| Обозначения | |
| Символы | LDHA; LDHM |
| CAS | 9001-60-9 |
| Entrez Gene | 3939 |
| HGNC | 6535 |
| OMIM | 150000 |
| RefSeq | NM_005566 |
| UniProt | P00338 |
| Другие данные | |
| Шифр КФ | 1.1.1.27 |
| Локус | 11-я хр., 11p15.4 |
Реакция
Лактатдегидрогеназа катализирует взаимопревращение пирувата и лактата с сопутствующим взаимопревращением NADH и NAD+. Он превращает пируват, конечный продукт гликолиза, в лактат, когда кислород отсутствует или его не хватает, и он выполняет обратную реакцию во время цикла Кори в печени. При высоких концентрациях лактата фермент проявляет ингибирование с обратной связью, и скорость превращения пирувата в лактат снижается. Она также катализирует дегидрирование 2-гидроксибутирата, но это гораздо более бедный субстрат, чем лактат.
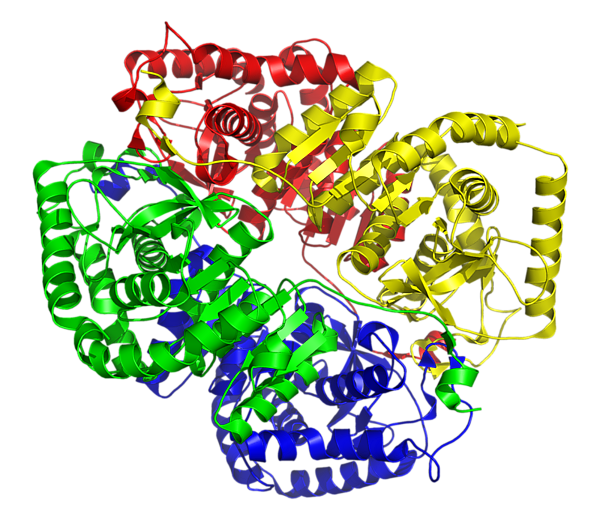
Активный центр
ЛДГ у людей использует His(193) в качестве акцептора протонов и работает в унисон с коферментом (Arg 99 и Asn 138) и остатками, связывающими субстрат (Arg106; Arg169;Thr 248)[2][3]. Активный сайт His (193) обнаружен не только в человеческой форме ЛДГ, но и у многих разных животных, что свидетельствует о конвергентной эволюции ЛДГ. Две разные субъединицы ЛДГ (ЛДГ-A, также известная как М-субъединица ЛДГ, и ЛДГ-B, также известная как Н-субъединица ЛДГ) сохраняют один и тот же активный сайт и одни и те же аминокислоты, участвующие в реакции. Заметным различием между двумя субъединицами, составляющими третичную структуру ЛДГ, является замена аланина (в М-цепи) на глютамин (в Н-цепи). Считается, что это крошечное, но заметное изменение является причиной того, что Н-субъединица может быстрее связывать NAD, а каталитическая активность М-субъединицы не снижается в присутствии ацетилпиридиндениндинуклеотида, тогда как активность Н-субъединицы снижается в пять раз[4].
Изоферменты лактатдегидрогеназы
Имеют разный состав субъединиц М (muscle) и Н (heart). Нумерация идет в зависимости от подвижности в геле при электрофорезе[5].
ЛДГ 1 — (НННН) — обладающий наибольшей подвижностью, содержится преимущественно в миокарде;
ЛДГ 2 — (НННМ) — преимущественно локализован в эритроцитах и почках.
ЛДГ 3 — (ННММ) — преимущественно содержится в легких;
ЛДГ 4 — (НМММ) — преимущественно локализован в скелетных мышцах и отчасти в гепатоцитах. Это причина того, что при болезни Боткина, в сыворотке крови больного одновременно повышается активность и содержание ЛДГ-5 и ЛДГ-4;
ЛДГ 5 — (ММММ) — обладающий наименьшей подвижностью, преимущественно локализован в гепатоцитах;
Изоферменты используются при диагностике инфарктов, ишемий, повреждения почек и т. д. Уровень лактатдегидрогеназы коррелирует со степенью тяжести заболевания, спровоцировавшего выброс фермента в кровь[6].