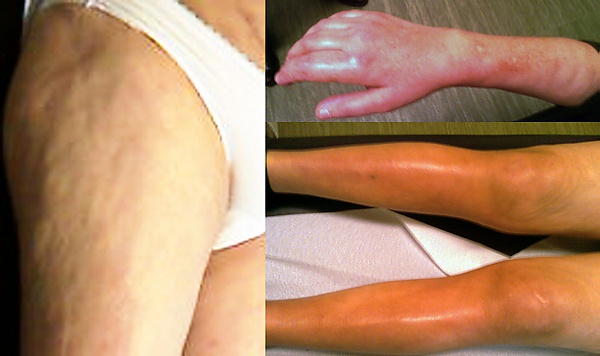
Эозинофильный фасциит
Эозинофи́льный фасции́т (ЭФ, синдро́м Шу́льмана) — редкое заболевание из группы склеродермических заболеваний, сопровождающееся локальным или генерализованным фиброзом. Его точная причина неизвестна. Болезнь чаще развивается у людей в возрасте от 20 до 60 лет, причём женщины страдают в два раза чаще мужчин. Изредка случаи заболевания встречаются и у детей. Среди возможных провоцирующих факторов выделяют сопутствующие аутоиммунные нарушения, такие как синдром Шегрена, системная красная волчанка и первичный билиарный цирроз[2].
Общие сведения
История
В 1974 году Шульман предложил новую концепцию заболевания под названием «диффузный фасциит с эозинофилией», основанную на двух клинических случаях. Оба пациента демонстрировали двустороннее, симметричное, диффузное, склеродермоподобное уплотнение кожи на конечностях, контрактуры суставов, отсутствие признаков синдрома Рейно или поражения внутренних органов, а также хороший ответ на терапию пероральными глюкокортикоидами[3].
В 1975 году Роднан предложил термин «эозинофильный фасциит», который стал общепринятым названием, несмотря на то, что на определённых стадиях болезни характерные признаки, такие как периферическая эозинофилия и эозинофильная инфильтрация в утолщённой фасции, могут отсутствовать[3].
Классификация
Классификация тяжести ЭФ:
- контрактура суставов (верхние конечности) — 1 балл;
- контрактура суставов (нижние конечности) — 1 балл;
- ограничение движений (верхние конечности) — 1 балл;
- ограничение движений (нижние конечности) — 1 балл;
- распространение и ухудшение кожной сыпи (прогрессирование симптомов) — 1 балл.
2 и более балла классифицируется как тяжёлая форма[4].
Этиология
Большинство случаев ЭФ считаются идиопатическими. Однако выделяют несколько возможных триггеров и связанных факторов[3]:
- интенсивные физические нагрузки;
- аутоиммунные заболевания (системная красная волчанка, синдром Шегрена, первичный билиарный цирроз, патология щитовидной железы);
- приём некоторых лекарственных препаратов (статины, рамиприл, гепарин, пембролизумаб);
- гематологические заболевания (аутоиммунная анемия, тромбоцитопения, панцитопения, апластическая анемия, парциальная красноклеточная аплазия, лимфомы, лейкозы, миеломная болезнь, миелопролиферативные заболевания);
- злокачественные новообразования (меланома, рак лёгких);
- необходимость проведения гемодиализа;
- инфекция Borrelia burgdorferi (болезнь Лайма);
- лучевая терапия;
- реакция трансплантата против хозяина.
Патогенез
В основе ЭФ предполагается аутоиммунный механизм. У пациентов с ЭФ отмечается повышенная экспрессия фибронектина и коллагена I типа в дермальных фибробластах, а также развитие фиброза вследствие избыточной выработки тканевого ингибитора металлопротеиназы-1, который блокирует расщепление внеклеточного матрикса. Важную роль в патогенезе играет эозинофилия, проявляющаяся повышенным уровнем катионного протеина эозинофилов и интерлейкина-5 в сыворотке, а также усиленной миграционной способностью эозинофилов. Одновременно наблюдается повышение уровня гистамина, свидетельствующее о вовлечении тучных клеток в патологический процесс. Дополнительными факторами являются увеличенная продукция интерлейкина-2, интерферона гамма и лейкемического ингибирующего фактора мононуклеарными клетками крови, гиперэкспрессия лигандов CD40 и повышенный уровень супероксиддисмутазы. Исследования также выявили повышенную экспрессию мРНК трансформирующего фактора роста-β1 и увеличение экспрессии генов фактора роста соединительной ткани в фибробластах фасции поражённых участков, что подтверждает участие этих провоспалительных цитокинов в развитии фиброзных изменений при данном заболевании[3].
Для гистологической картины характерно: в глубоких слоях фасции и нижних отделах подкожной клетчатки обнаруживаются отёк и воспалительный инфильтрат, состоящий из лимфоцитов, плазмоцитов, гистиоцитов и, в большинстве случаев, эозинофилов. На более поздних стадиях заболевания фасция утолщается и склерозируется, при этом воспалительный инфильтрат постепенно исчезает. Одновременно в поражённых тканях и на системном уровне отмечается повышенное содержание гистамина — продукта дегрануляции тучных клеток. Аналогичные гистологические изменения наблюдаются и в прилегающих мышечных структурах, затрагивая эпимизий, перимизий, эндомизий, а также сами мышечные волокна[3].
Эпидемиология
ЭФ остаётся редким заболеванием с ограниченным количеством зарегистрированных случаев. На момент разработки диагностических критериев в 2019 году в Японии было выявлено приблизительно 100 пациентов с этим диагнозом. В российской медицинской практике описаны лишь единичные случаи данной патологии. Наиболее часто заболевание поражает взрослых людей в возрастном диапазоне 20—60 лет, хотя в клинической практике встречаются случаи заболевания детей. Болезнь встречается с сопоставимой частотой у представителей обоих полов. Для ЭФ характерно спорадическое возникновение, эпидемические вспышки не типичны[5].
Диагностика
ЭФ характеризуется внезапным появлением болезненного покраснения и отёка поражённых конечностей. Хотя заболевание преимущественно симметричное, встречаются и односторонние случаи. Поражение конечностей является типичным проявлением, однако могут вовлекаться и другие участки кожи. Вовлечение туловища считается признанным фактором риска развития рефрактерного фиброза[6].
Постепенно отёк сменяется утолщением кожи, которая становится плотно спаянной с подлежащими тканями. Характерными диагностическими признаками являются симптом «апельсиновой корки» и симптом «борозды». При наиболее распространённых формах заболевания могут наблюдаться рестриктивные нарушения дыхания вследствие выраженного фиброза кожи туловища, миалгии, а также слабость проксимальных мышц, вызванная распространением воспалительного процесса с фасции на перимизий[6].
Уплотнение кожи может приводить к развитию суставных контрактур и ретракции сухожилий, что проявляется «симптомом молитвы», отражающим выраженность фиброза фасции. Воспалительный полиартрит с поражением как мелких, так и крупных суставов наблюдается у 40 % пациентов. Среди других распространённых проявлений отмечаются потеря веса, астения, утренняя скованность и синдром запястного канала[6].
Висцеральные поражения встречаются редко и требуют исключения других заболеваний, однако в литературе описаны случаи ассоциации ЭФ с поражением лёгких, плевральным выпотом, перикардитом и поражением почек[6].
Магнитно-резонансная томография служит основным методом диагностики ЭФ, позволяя выявлять характерные изменения в виде гиперинтенсивного сигнала от фасций на Т2-взвешенных изображениях, их выраженного утолщения и усиленного накопления контрастного вещества на Т1-взвешенных срезах, а также отёка перифасциальных тканей. Обнаружение этих патогномоничных признаков даёт возможность в типичных случаях отказаться от инвазивной процедуры и сразу начать специфическую терапию. Высокая информативность делает этот метод незаменимым в диагностическом алгоритме при подозрении на ЭФ, обеспечивая точную визуализацию патологических изменений фасциальных структур и окружающих тканей[2].
При ультразвуковом исследовании выявляется комплекс характерных изменений: утолщение кожного покрова и подкожно-жировой клетчатки, патологическое изменение структуры фасций и сухожилий, а также выраженное снижение эластичности и компрессионной податливости мягких тканей[2].
Позитронно-эмиссионная томография в сочетании с компьютерной томографией с 18F-фтордезоксиглюкозой представляет собой высокоинформативный метод диагностики, способный выявлять активные воспалительные процессы при ЭФ даже при отсутствии структурных изменений в тканях[2].
Гистологическое исследование биоптата тканей позволяет выявить характерные гистологические изменения[7].
Клинический анализ крови: может наблюдаться эозинофилия, тромбоцитопения, анемия и повышение скорости оседания эритроцитов[7].
Иммуноферментный анализ крови: гипергаммаглобулинемия является характерным, хотя и непостоянным признаком, в большинстве случаев обусловлена поликлональным повышением иммуноглобулина G. Ревматоидный фактор и антинуклеарные антитела могут быть положительными[7].
Полимеразная цепная реакция: может выявлять инфекцию бактериями рода Borrelia[7].
В 2019 году Японской дерматологической ассоциацией были разработаны и опубликованы диагностические критерии ЭФ. К малым критериями относятся[5]:
- гистологически подтверждённый фиброз подкожной клетчатки и соединительной ткани с утолщением фасции, сопровождающийся инфильтрацией эозинофилами и моноцитами;
- характерное утолщение фасций, выявляемое при магнитно-резонансной томографии.
Большой критерий представляет собой симметричное склеротическое поражение всех четырёх конечностей при отсутствии проявлений синдрома Рейно и признаков системной склеродермии. Для постановки диагноза необходимо наличие большого критерия в сочетании хотя бы с одним малым критерием[5].
Дифференциальная диагностика
Дифференциальная диагностика ЭФ проводится со следующими состояниями[3]:
- системная склеродермия;
- нефрогенный системный фиброз;
- склеромикседема;
- склередема;
- кожный вариант внутрисосудистой В-крупноклеточной лимфомы.
Осложнения
К возможным осложнениям ЭФ относятся контрактуры суставов, периферическая полинейропатия и развитие компартмент-синдрома. В редких случаях заболевание может выступать как паранеопластический синдром при злокачественных новообразованиях, чаще всего проявляясь до выявления основного онкологического заболевания. Особенно часто описывается связь ЭФ с злокачественными заболеваниями кроветворной и лимфатической систем[8].
Лечение
На 2025 год стандартизированный подход к лечению ЭФ отсутствует ввиду недостатка рандомизированных клинических исследований. Основу терапии составляет системное применение глюкокортикоидов. Длительная терапия высокими дозами глюкокортикоидов сопряжена с риском развития остеопороза и оппортунистических инфекций, что требует профилактического назначения бисфосфонатов и антиибиотиков[3].
При отсутствии ответа на монотерапию глюкокортикоидами в течение 3 месяцев или необходимости снижения их дозы применяют иммуносупрессивные препараты. После достижения ремиссии лечение продолжают в течение 4—6 месяцев. В случаях рефрактерного течения заболевания рассматривается назначение моноклональных антител (тоцилизумаб, барицитиниб, ритуксимаб), внутривенных иммуноглобулинов или фототерапии[3].
Важным компонентом комплексного лечения является физиотерапия, направленная на сохранение объёма движений в суставах и профилактику контрактур. В тяжёлых случаях при формировании стойких контрактур или развитии синдрома запястного канала показано хирургическое вмешательство[3].
Прогноз
Прогноз при ЭФ варьируется, но заболевание часто имеет самоограничивающийся характер после проведённого лечения. Однако у многих больных сохраняются остаточные явления перенесённого заболевания. Наиболее выраженные остаточные повреждения ассоциированы с пожилым возрастом пациентов, наличием тяжёлых проявлений при первичной диагностике (вовлечение туловища, повышение маркеров воспаления), а также сопутствующими заболеваниями[9].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 3 4 Тулин П. Е., Оджарова А. А., Белякова М. А., Крылов А. С. ПЭТ/КТ с 18F-ФДГ при эозинофильном фасциите. Клиническое наблюдение (рус.) // Онкологический журнал: лучевая диагностика, лучевая терапия : статья. — 2022. — Т. 5, № 2. — С. 76—80. — ISSN 2587-7593. — doi:10.37174/2587-7593-2022-5-2-76-80.
- ↑ 1 2 3 4 5 6 7 8 9 Diana Mazilu, Laura Alina Boltașiu (Tătaru), Denise-Ani Mardale, Maria Silviana Bijă, Sermina Ismail, Violeta Zanfir, Florentina Negoi, Andra Rodica Balanescu. Eosinophilic Fasciitis: Current and Remaining Challenges // International Journal of Molecular Sciences. — 2023-01-19. — Т. 24, вып. 3. — С. 1982. — ISSN 1422-0067. — doi:10.3390/ijms24031982.
- ↑ Masatoshi Jinnin, Toshiyuki Yamamoto, Yoshihide Asano, Osamu Ishikawa, Shinichi Sato, Kazuhiko Takehara, Minoru Hasegawa, Manabu Fujimoto, Hironobu Ihn. Diagnostic criteria, severity classification and guidelines of eosinophilic fasciitis // The Journal of Dermatology. — 2017-12-13. — Т. 45, вып. 8. — С. 881–890. — ISSN 1346-8138 0385-2407, 1346-8138. — doi:10.1111/1346-8138.14160.
- ↑ 1 2 3 Акимова А. А., Травин М. А., Летягина Е. А., Королев М. А. Эозинофильный фасциит: современный взгляд на диагностику и лечение (рус.) // РМЖ. Медицинское обозрение : статья. — 2022. — Т. 6, № 3. — С. 153—158. — ISSN 2587-6821. — doi:10.32364/2587-6821-2022-6-3-153-158.
- ↑ 1 2 3 4 I. Pinal-Fernandez, A. Selva-O' Callaghan, J.M. Grau. Diagnosis and classification of eosinophilic fasciitis // Autoimmunity Reviews. — 2014-04. — Т. 13, вып. 4—5. — С. 379–382. — ISSN 1568-9972. — doi:10.1016/j.autrev.2014.01.019.
- ↑ 1 2 3 4 Peter M Henning. Eosinophilic Fasciitis (англ.). Medscape (12 декабря 2024).
- ↑ Ka Lai Tsoi, Martijn Custers, Liesbeth Bij de Vaate, Johannes W G Jacobs. Eosinophilic fasciitis (англ.) // BMJ Case Reports. — 2012-10-03. — Vol. 2012. — P. bcr20126158. — ISSN 1757-790X. — doi:10.1136/bcr.2012.6158.
- ↑ Jorre S. Mertens, Rogier M. Thurlings, Wietske Kievit, Marieke M.B. Seyger, Timothy R.D. Radstake, Elke M.G.J. de Jong. Long-term outcome of eosinophilic fasciitis: A cross-sectional evaluation of 35 patients // Journal of the American Academy of Dermatology. — 2017-09. — Т. 77, вып. 3. — С. 512–517.e5. — ISSN 0190-9622. — doi:10.1016/j.jaad.2017.05.018.
Литература
- Енисеева Елена Сергеевна, Орлова Галина Михайловна, Сараева Наталья Орестовна, Смолькова Людмила Геннадьевна. Ассоциированные с эозинофилией заболевания и расстройства // Байкальский медицинский журнал. — 2006. — № 6.
- Фомина Л. Л. Паранеопластические синдромы в ревматологии // Научно-практическая ревматология. — 2002. — № 2.
- Козлова Л., Багирова Г., Кучма Г., Стеценко Е., Шатилов А. Склеродермоподобные заболевания в практике врача-ревматолога // Врач. — 2018. — № 5.