Гранулоцитарный анаплазмоз человека
Гранулоцита́рный анаплазмо́з челове́ка (ГАЧ) — инфекционное заболевание, вызываемое грамотрицательной бактерией Anaplasma phagocytophilum[2]. Возбудитель обычно передаётся человеку через укусы иксодовых клещей, включая виды Ixodes scapularis, Ixodes pacificus. Ixodes ricinus и Ixodes persulcatus[3]. Заболевание проявляется лихорадкой, ознобом, головной болью, миалгиями, артралгиями, слабостью и другими неспецифическими симптомами интоксикации. У некоторых пациентов наблюдаются поражения печени, селезёнки, сердечно-сосудистой и нервной систем[2]. Диагноз устанавливается на основании клинико-эпидемиологических и лабораторных данных[4]. Препаратом выбора при лечении ГАЧ является доксициклин[5].
Общие сведения
История
Первая известная вспышка ГАЧ была зарегистрирована в США в начале 1990 года. Заболевание началось с пациента из штата Висконсин, госпитализированного в Миннесоте, который скончался, не получив точного диагноза. В последующие годы в Висконсине и Миннесоте были выявлены новые случаи с аналогичными симптомами[6].
В 1991 году заболевание было подробно описано клиницистом Д. Бэккеном в Миннесоте как клинический синдром с лихорадкой и цитоплазматическими включениями в нейтрофилах, предположительно имеющий эрлихиозную природу[4]. В 1994 году было установлено, что заболевание представляет собой ГАЧ[7].
Этиология
Возбудителем ГАЧ является Anaplasma phagocytophilum — облигатный внутриклеточный грамотрицательный микроорганизм из рода Anaplasma, семейства Anaplasmataceae[2].
Основными переносчиками инфекции являются иксодовые клещи рода Ixodes. В США основными видами-переносчиками являются I. scapularis и I. pacificus, в Европе — I. ricinus, а в Азии — I. persulcatus[6][8]. Резервуарами возбудителя, кроме клещей, в природе служат дикие и домашние животные — грызуны, олени, собаки, а также птицы, способствующие распространению инфицированных клещей на большие расстояния[2].
Инфицированный клещ передаёт возбудителя при укусе человеку вместе со слюной. Возможна передача инфекции при переливании крови от заражённого донора (анаплазмоз, передающийся при переливании крови)[9].
Для ГАЧ характерна весенне-летняя сезонность, связанная с активностью клещей[2].
Факторы риска тяжёлого течения болезни[10]:
- возраст старше 65 лет;
- ослабленная иммунная система.
Патогенез
После присасывания клеща возбудитель со слюной проникает в кожу и подкожную клетчатку, затем гематогенным путём распространяется по всему организму. Anaplasma phagocytophilum характеризуется узкоспецифическим тропизмом к гранулоцитам, преимущественно к зрелым нейтрофилам[2][4].
Первичное связывание возбудителя с клеткой-мишенью происходит посредством лиганда PSGL-1 — рецептора, используемого нейтрофилами для адгезии на эндотелиальных клетках при развитии воспалительной реакции. После связывания бактерия интернализируется путём рецепторного эндоцитоза и формирует внутри цитоплазмы мембранную вакуоль, где размножается, образуя морулы — колонии зрелых бактерий, способных избегать действия лизосом клетки[2][4].
После завершения размножения возбудитель выходит из клетки, вызывая её разрушение. В инфекционный процесс вовлекаются также макрофаги селезёнки, печени, лимфатических узлов, костного мозга и других органов, что приводит к развитию воспалительных изменений[2].
Инфицирование нейтрофилов сопровождается угнетением фагоцитарной активности, снижением продукции активных форм кислорода и, как следствие, ослаблением защитных функций организма. В ответ на инфекцию развивается выраженная цитокиновая реакция с повышением концентрации интерлейкинов 1, 6, 8 и фактора некроза опухоли α. Активация синтеза цитокинов происходит через сигнальный путь Toll-like рецепторов, преимущественно TLR-2. Цитокины образуются раньше появления антител и определяют клинические проявления заболевания — лихорадку, миалгии и артралгии. В развитии воспаления основная роль принадлежит интерлейкину-8. Повышение концентрации интерлейкина-8 угнетает продукцию гематопоэза. В период реконвалесценции повышается концентрация противовоспалительного интерлейкина-10[4].
Также важное значение в патогенезе имеет поверхностный белок Msp2, обеспечивающий прикрепление анаплазмы к клеточной мембране и антигенную изменчивость возбудителя. Другой белок, AnkA, обладает способностью проникать через мембраны вакуоли и ядра, что позволяет ему располагаться около хроматина в ядре заражённого гранулоцита. Предполагают, что с ним связаны различия в тяжести течения болезни[11].
Эпидемиология
К 1997 году было выявлено более 450 случаев ГАЧ в США, а также в Европе. В период с 2003 по 2010 год в США было зарегистрировано более более 4500 случаев ГАЧ[4]. По данным Центров по контролю и профилактике заболеваний США к 2023 году число зарегистрированных случаев анаплазмоза достигло рекордного уровня — 7280 случаев[12]. Заболеваемость наиболее высока на северо-востоке и Среднем Западе США, а также в северной Калифорнии. Средние показатели в эндемичных штатах составляют 3—16 случаев на 100 тысяч населения, однако в очагах в Коннектикуте и и северо-западном Висконсине этот показатель достигает 51—58 на 100 тысяч населения[4].
В Европе наибольшее количество заболеваний отмечается в северо-западных и восточных регионах[4]. В Европе ежегодно регистрируется менее 300 случаев заболевания[13].
В России первые случаи ГАЧ были зарегистрированы в 2002 году. ГАЧ выявляют практически повсеместно: Горном Алтае, Иркутской области, на Дальнем Востоке, Тюменской области, Омской и Томской, Воронежской, Тульской областях, в Красноярском крае и многих других территориях . В России в 2016 году было зарегистрировано 53 случая ГАЧ[11]. Инфицированность клещей I. ricinus в различных регионах России составляет 6—19 %, в Республике Беларусь — до 27 %, в Польше — до 25 %[2].
Заболеваемость имеет выраженную сезонность, соответствующую периоду активности клещей (весна — лето, с пиком в июне-июле). Средний возраст больных выше, чем при других клещевых инфекциях, и составляет в среднем от 44 до 60 лет. Соотношение мужчин и женщин среди заболевших составляет 3:1. Наибольшему риску подвергаются жители сельских районов, а также люди, содержащие собак[4].
Диагностика
Диагноз устанавливается на основании клинико-эпидемиологических и лабораторных данных[4].
Большое значение имеет тщательный сбор эпидемиологического анамнеза. При сборе анамнеза обращают внимание на факт присасывания клеща, проживание или пребывание в эндемичных по клещевым инфекциям районах, а также посещение лесных и лесопарковых зон[2].
Инкубационный период ГАЧ составляет от 3 дней до 3 недель (в среднем около 14 дней). Заболевание может протекать от бессимптомных и субклинических форм до тяжёлых случаев, угрожающих жизни пациента[2].
Лёгкие формы заболеваний проявляются в виде недомоганий, напоминающих респираторную инфекцию. У таких пациентов отмечаются лихорадка, слабость, головная боль, миалгии, артралгии и другие неспецифические симптомы интоксикации[2].
Манифестные формы начинаются остро, с повышения температуры тела до 39—40 °C, озноба, выраженной слабости и головной боли[2][4]. Также отмечаются потливость, мышечные и суставные боли, снижение аппетита, боли в животе, тошнота, рвота, диарея, чувство тяжести в правом подреберье. У части пациентов наблюдаются боль в горле, фарингит, кашель и першение[2][11]. При физикальном осмотре может отмечаться гиперемия лица и инъецированность склер[4].
У 25 % пациентов выявляется генерализованная лимфаденопатия. Также может наблюдаться желтушный синдром, гепатомегалия[11]. Со стороны сердечно-сосудистой системы возможны брадикардия и понижение артериального давления. Поражение почек проявляется в виде нефропатии[2]. Может быть увеличена селезёнка[4].
Высыпания на коже встречаются редко (примерно у 20 % пациентов) и могут быть в виде пятнистой, пятнистно-папулёзной или петехиальной сыпи. Они появляются в течение первой недели заболевания, локализуется по всему телу, кроме ладоней и подошв[2][4]. Их появление часто свидетельствуют о микст-инфекции (с клещевым боррелиозом, клещевыми эндемическими риккетсиозами или менингококковой инфекцией)[2][11].
В более тяжёлых случаях заболевание сопровождается общемозговыми симптомами, неврологическими нарушения: менингизмом, менингитом, менингоэнцефалитом или полинейропатией. У иммунокомпрометированных пациентов и лиц без селезёнки течение заболевания значительно тяжелее, что может приводить к развитию инфекционно-токсического шока, острого респираторного дистресс-синдрома, панкардита, рабдомиолиза, почечной недостаточности, кровотечений и инвазивных оппортунистических инфекций вирусной или грибковой природы[2][11].
Продолжительность лихорадочного периода варьирует от нескольких дней[2] до 3—11 недель[4].
- Клинический анализ крови — в первые дни болезни отмечаются лейкопения с палочкоядерным сдвигом влево на фоне нейтропении, лимфопения, тромбоцитопения, повышение скорости оседания эритроцитов. Также может отмечаться анемия и панцитопения[2]. Затем лимфопения сменяется лимфоцитозом, появляются атипичные лимфоциты[11].
- Клинический анализ мочи — гипоизостенурия, протеинурия, гематурия[2], лейкоцитурия[4].
- Биохимический анализ крови — повышением активности аспартатаминотрансферазы, аланинаминотрансферазы, лактатдегидрогеназы, повышение концентрации креатинина, мочевины, С реактивного белка[2].
- Биохимический анализ мочи — повышение концентрации мочевины и креатинина[2].
- Выявление ДНК Anaplasma phagocytophilum методом полимеразной цепной реакции[11]. Материалом для исследования служат плазма крови, лейкоцитарная фракция, ликвор, могут исследоваться клещи[2].
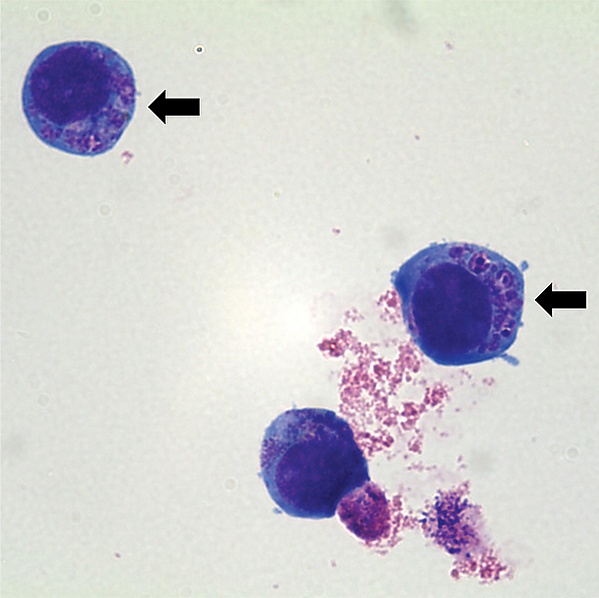
- Микроскопия мазков крови или лейкоцитарной фракции, окрашенных по Райту или Романовскому — Гимзе — на первой неделе заболевания у пациентов в периферической крови могут обнаруживаться морулы — скопления возбудителя в цитоплазме нейтрофилов[11].
- Бактериологический метод — культивирование возбудителя на культурах из промиелоцитарных клеток, взятых у больных лейкемией (HL-60)[11].
- Реакция непрямой иммунофлюоресценции — позволяет выявить антитела классов IgM и IgG к A. phagocytophilum. Диагноз подтверждается четырёхкратным увеличением титра антител в парных сыворотках, взятых с интервалом 2—4 недели. Антитела IgM появляются на 9—11-й день болезни, достигают максимума на 12—24-й день и затем снижаются. Антитела IgG достигают пика к 4—5-й неделе и могут длительно сохраняться после выздоровления[11].
- Иммуноферментный анализ — используется для качественного определения антител классов IgM и IgG к A. phagocytophilum[11].
- Электрокардиография — выявляются признаки нарушения проводимости миокарда[2].
- Рентгенография органов грудной клетки — могут выявляться признаки бронхита или пневмонии, увеличение лимфатических узлов[2].
Дифференциальная диагностика
Состояния, от которых необходимо дифференцировать:
- энтеровирусная инфекция;
- инфекционный мононуклеоз;
- инфекция, вызванная вирусом герпеса человека 6-го типа;
- инфекция, вызванная парвовирусом B19;
- вирусный гепатит;
- лихорадка Западного Нила;
- лихорадка Чикунгунья;
- болезнь Лайма;
- боррелиоз, вызванный Borrelia miyamotoi;
- бабезиоз;
- моноцитарный эрлихиоз человека;
- вирусные инфекции Повассана;
- возвратный тиф, вызванный Borrelia hermsii;
- диссеминированная гонококковая инфекция;
- эндокардит;
- менингококцемия;
- микоплазменная пневмония;
- вторичный сифилис;
- септический шок;
- брюшной тиф;
- аллергическая реакция на лекарственные препараты;
- идиопатическая тромбоцитопеническая пурпура;
- синдром Кавасаки;
- тромботическая тромбоцитопеническая пурпура;
- гемафагоцитарный синдром;
- синдрома активации макрофагов[14];
- цитомегаловирусная инфекция;
- менингоэнцефалит;
- лептоспироз[2];
- стрептококковая инфекция группы А;
- колорадская клещевая лихорадка;
- крысиный сыпной тиф;
- Ку-лихорадка;
- содоку;
- пятнистая лихорадка Скалистых гор;
- туляремия;
- лихорадка Денге;
- малярия;
- клещевой энцефалит;
- лейкемия;
- лимфома[11].
Осложнения
Включают:
- инфекционно-токсический шок;
- атипичную пневмонию;
- миокардит;
- острую почечную недостаточность;
- острую дыхательную недостаточность;
- коагулопатии;
- кровотечения;
- оппортунистические инфекции[2];
- острый респираторный дистресс-синдром;
- панкардит;
- перикардит;
- рабдомиолиз;
- полинейропатию;
- менингит;
- менингоэнцефалит;
- сенсоневральную тугоухость[11]
Лечение
Препаратом выбора при лечении ГАЧ является полусинтетический антибиотик широкого спектра действия группы тетрациклинов. Стандартная продолжительность курса терапии составляет 10—14 дней[5].
Патогенетическая терапия включает проведение дезинтоксикационных мероприятий, а при тяжёлом течении возможно назначение глюкокортикоидных гормонов[4].
Симптоматическая терапия включает назначение нестероидных противовоспалительных препаратов, противорвотных средств, спазмолитиков, ферментов и других лекарственных препаратов по показаниям[15].
Прогноз
Диспансерное наблюдение
Индивидуально.
Профилактика
Специфических мер профилактики не разработано. Основным способом защиты от ГАЧ является профилактика присасывания клещей и их немедленное удаление, которая включает в себя[2][16]:
- ношение одежды, максимально закрывающей поверхность тела;
- обработка одежды и снаряжения средствами, содержащими 0,5 % перметрина;
- использование репеллентов;
- избегание контакта с клещами;
- само- и взаимоосмотр на факт нахождения клещей после посещения зон их обитания.