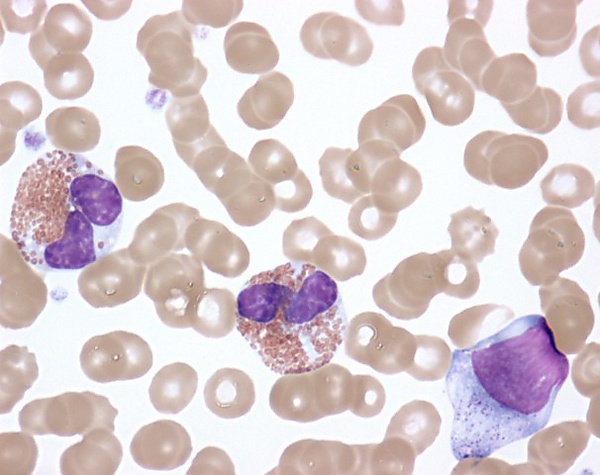
Гиперэозинофильный синдром
Гиперэозинофильный синдром — сложная группа гетерогенных заболеваний, характеризующихся стойким и значительным повышением уровня эозинофилов и их медиаторов, что приводит к инфильтрации и повреждению тканей[1].
Общие сведения
История
Термин «гиперэозинофильный синдром» (ГЭС) был введён в 1968 году для объединения пациентов с рядом схожих заболеваний, характеризующихся хронически повышенным уровнем эозинофилов в периферической крови и поражением органов, связанным с эозинофильной инфильтрацией. Определение идиопатического ГЭС было предложено Чусидом в 1975 году: стойкая эозинофилия периферической крови неизвестного происхождения, превышающая 1,5 × 10⁹/л в течение более чем шести месяцев подряд и приводящая к дисфункции и/или повреждению органов[2].
Классификация
На основании этиологических причин развития ГЭС выделяют[1]:
- Миелопролиферативный ГЭС;
- Вторичный (реактивный) ГЭС;
- Семейный ГЭС;
- Идиопатический ГЭС;
- Орган ограниченный ГЭС.
Этиология
Миелопролиферативный ГЭС:
Классифицируются на несколько подтипов, включая[1][3]:
- FIP1L1-PDGFRA-ассоциированный вариант (F/P+) — возникает из-за интерстициальной делеции хромосомы 4q12;
- мутации в гене PDGFRB, например, транслокация t(5;12)(q31-35;p13);
- точечная мутация в гене JAK2;
- мутация в гене FGFR1;
- хронический эозинофильный лейкоз;
- ГЭС с миелоидными чертами без известных мутаций;
- Т-клеточные лимфоцитарные варианты: обусловлены аномальными IL-5-продуцирующими T-клетками.
Вторичный (реактивный) ГЭС
К заболеваниям, вызывающим развитие реактивного ГЭС относятся:
1. Инфекции[3]:
- паразитозы: описторхоз, трихинеллёз, токсокароз, эхинококкоз, филяриоз, аскаридоз, стронгилоидоз, шистосомоз;
- хронические инфекции вирусной и бактериальной этиологии.
2. Аллергические реакции[3]:
- атопические заболевания: бронхиальная астма, аллергический ринит, атопический дерматит, крапивница;
- пищевая аллергия;
- лекарственная аллергия на фоне приёма антибиотиков, сульфаниламидов.
3. Заболевания лёгких:
- острая и хроническая идиопатическая эозинофильная пневмония (болезнь Леффлера)[3].
4. Заболевания желудочно-кишечного тракта, ассоциированные с эозинофилией[3]:
- первичный или вторичный эозинофильный эзофагит;
- первичный или вторичный гастроэнтерит;
- первичный или вторичный колит.
5. Другие причины аутоиммунного, воспалительного или токсического характера[3]:
- заболевания соединительной ткани (склеродермия, узелковый периартериит, системная красная волчанка);
- синдром Черга — Страусс (эозинофильный васкулит);
- эозинофильный фасциит;
- болезнь Кимура;
- саркоидоз;
- хронический панкреатит.
6. Злокачественные заболевания.
- лимфопролиферативные заболевания, где эозинофилы не являются частью патологического клона (лимфома Ходжкина, неходжкинские лимфомы, особенно Т-клеточные);
- солидные опухоли (особенно с метастазами в костный мозг)[3].
7. Эндокринная недостаточность надпочечников (болезнь Аддисона)[3].
Семейный ГЭС
Диагностируется при наличии семейного анамнеза документированной стойкой гиперэозинофилии неустановленной причины[3].
Идиопатический ГЭС
До его установления должен быть проведён детальный диагностический поиск для того, чтобы отвергнуть все возможные причины реактивного процесса и исключить наличие маркеров клональной гиперэозинофилии[3].
Органоограниченный ГЭС
Характеризуется тканевой гиперэозинофилией с поражением органов, но без соответствия критериям ГЭС по показателям крови[1].
Патогенез
Эозинофилы, являясь многофункциональными лейкоцитами, проявляют мощные провоспалительные, протромботические и профибротические свойства. Их способность инфильтрировать ткани может приводить к серьёзным повреждениям органов и развитию органной дисфункции. Ключевую роль в этом процессе играет активация фибробластов, их пролиферация и секреция трансформирующего фактора роста бета и интерлейкина-1β. Токсичные гранулярные белки эозинофилов, включая катионный протеин эозинофилов, стимулируют выброс трансформирующего фактора роста бета, что инициирует развитие эозинофил-опосредованного фиброза тканей. Многочисленные исследования подтверждают участие эозинофильной инфильтрации в формировании воспалительных фиброзных поражений[1].
Кроме того, заболевания, связанные с активацией эозинофилов, ассоциированы с повышенным риском тромбообразования. Этот эффект объясняется экспрессией тканевого фактора эозинофилами, а также их способностью активировать тромбоциты через действие гранулярных белков, создавая состояние гиперкоагуляции[1].
Диагностика
Клиническая картина
Гиперэозинофилия ассоциирована с дисфункцией различных систем органов. По мере изучения подтипов ГЭС выявилась чёткая связь между клиническими фенотипами и специфическими осложнениями. Наиболее часто при ГЭС поражаются кроветворная система, кожа, сердечно-сосудистая система, лёгкие и нервная система.
Кожные проявления встречаются более чем у 50 % пациентов с ГЭС и часто служат первым признаком заболевания. Для миелопролиферативного ГЭС характерно развитие болезненных слизистых язв, которые могут ошибочно приниматься за проявления болезни Бехчета. Однако язвы при ГЭС обычно крупнее и не сопровождаются другими типичными признаками болезни Бехчета, такими как увеит и синовит. Для ГЭС, опосредованного Т-клетками, более характерны генерализованный зуд, экзема, эритродермия и крапивница. Среди других дерматологических проявлений отмечаются эпизодический ангионевротический отёк, крапивница, зудящие эритематозные высыпания, кольцевидная центробежная эритема и некротизирующий васкулит[4].
Сердечно-сосудистые осложнения развиваются у 40-60 % пациентов с ГЭС и являются важной причиной смертности. Поражение сердца при ГЭС традиционно подразделяют на три стадии: острую некротическую, тромботическую и фиброзную. Острая стадия развивается в течение 1-2 месяцев после появления эозинофилии и характеризуется инфильтрацией миокарда эозинофилами с последующим некрозом клеток. В течение года после некротической стадии часто формируются пристеночные тромбы в желудочках, выводных трактах и подклапанных областях. В среднем через 2 года от начала эозинофилии развивается фиброз эндокарда и хорд, приводящий к дилатационной кардиомиопатии и прогрессирующей клапанной дисфункции. Клинические проявления варьируют от болей в груди и одышки до тяжёлых эмболических осложнений и аритмий[4].
Неврологические проявления при ГЭС отличаются значительным разнообразием. Кардиальные тромбы могут стать источником эмболий, приводящих к транзиторным ишемическим атакам или инсультам. Первичное поражение ЦНС может проявляться энцефалопатией с изменениями поведения, потерей памяти и спутанностью сознания. При обследовании часто выявляются признаки поражения верхних мотонейронов. Реже наблюдаются судороги, внутричерепные кровоизлияния и деменция. Периферические нейропатии могут проявляться изолированными сенсорными или моторными нарушениями, либо их сочетанием[4].
Поражение лёгких встречается примерно у 40 % пациентов с ГЭС и может проявляться одышкой, кашлем или бессимптомными изменениями на рентгенограмме. У 15-30 % пациентов развиваются инфильтративные изменения в лёгких, которые могут быть как очаговыми, так и диффузными. В исходе заболевания может развиться фиброз лёгких[4].
Ревматологические проявления ГЭС могут включать артралгии, неэрозивный полиартрит, выпоты в суставах с эозинофилией синовиальной жидкости и феномен Рейно. Эти осложнения связывают со способностью катионного протеина эозинофилов индуцировать сокращение коллагена и высвобождение фиброгенных цитокинов[4].
Тромбозы при эозинофильном васкулите могут развиваться вследствие активации коагуляционного каскада тканевым фактором, высвобождаемым при дегрануляции эозинофилов[4].
Поражение желудочно-кишечного тракта при ГЭС проявляется болями в животе, рвотой, диареей и дисфагией. Эти симптомы обусловлены цитотоксическим действием эозинофилов на эпителий, индукцией воспалительных цитокинов и повреждением энтеральной нервной системы[4].
Лабораторная диагностика
Общий анализ крови: выявляется эозинофилия, анемия, тромбоцитопения.
Цитологическое исследования мазка крови: характерно наличие незрелых эозинофилов в периферической крови. Эозинофилы могут иметь выраженные структурные аномалии, включая увеличенные размеры клеток, неравномерную грануляцию цитоплазмы и вакуолизацию. Также отмечались ядерные аномалии — как гипосегментация, так и гиперсегментация.
Дифференциальная диагностика
Дифференциальная диагностика ГЭС проводится со следующими состояниями[1]:
- острый эозинофильный лейкоз;
- хронический миелолейкоз;
- системный мастоцитоз с эозинофилией;
- эозинофильный гранулёматоз с полиангиитом.
Осложнения
Наиболее опасные осложнения включают[1]:
- лейкозы;
- сердечную недостаточность
- эндокардит
- тяжёлую рестриктивную кардиомиопатию, приводящую к желудочковым аритмиям из-за поражения проводящей системы сердца.
Лечение
Кортикостероиды
Глюкокортикостероиды остаются наиболее широко используемыми и высокоэффективными препаратами для лечения ГЭС. Ответ на кортикостероидную терапию может варьировать в зависимости от фенотипа ГЭС. Пациенты с лимфоцитарным ГЭС обычно демонстрируют хороший ответ на стероиды. Напротив, пациенты с миелопролиферативным ГЭС обычно менее чувствительны к стероидной терапии[4].
Гидроксимочевина широко применяется как препарат второй линии при ГЭС. Её преимущества включают доступность и относительно низкую стоимость. Высокие дозы часто связаны с гематологической и желудочно-кишечной токсичностью. В отличие от кортикостероидов, гидроксимочевина действует преимущественно на этапе развития эозинофилов в костном мозге, а не на зрелые периферические эозинофилы, что объясняет её более медленное начало действия[4].
Интерферон-α обладает комплексным действием на различные клеточные линии, что делает его потенциально эффективным при разных вариантах ГЭС. Этот препарат не только воздействует непосредственно на эозинофилы, но и подавляет пролиферацию CD4+ T-клеток и продукцию IL-5 аномальными CD3-CD4+ T-клетками. В клинической практике препарат первоначально продемонстрировал эффективность у пациентов, резистентных к терапии гидроксимочевиной и кортикостероидами[4].
Ингибиторы тирозинкиназ
Прорывом в лечении миелопролиферативных ГЭС стало применение ингибиторов тирозинкиназ, в частности иматиниба. В многоцентровом исследовании 17 из 18 пациентов получали иматиниб в средней дозе 400 мг в сутки, причём у 15 из них (88 %) была достигнута полная ремиссия[4].
Иммуномодулирующие препараты
Меполизумаб, моноклональное антитело против IL-5, является одним из перспективных препаратов в лечении ГЭС[4].
Прогноз
Прогноз при ГЭС отличается значительной вариабельностью — от лёгких форм, требующих лишь наблюдения, до тяжёлых жизнеугрожающих случаев с развитием лейкоза или необратимой сердечной недостаточности. Хотя чёткие прогностические маркеры пока не установлены, в последние годы исходы заболевания существенно улучшились благодаря нескольким факторам: более раннему выявлению осложнений, совершенствованию хирургических методов лечения кардиальных поражений и появлению новых целенаправленных терапевтических подходов. Дальнейшее изучение патогенеза различных вариантов ГЭС открывает перспективы для оптимизации лечения и улучшения прогноза у пациентов[1].
Примечания
Литература
- Лопина Е. А., Душина А. Г., Либис Р. А. Идиопатический гиперэозинофильный синдром. Клинический случай // Архивъ внутренней медицины. — 2022. — № 5 (67).
- Михеева О. М., Кирова М. В., Ефремов Л. И., Быстровская Е. В., Лазебник Л. Б. Гиперэозинофильный синдром с поражением пищевода, желудка и тонкой кишки // Экспериментальная и клиническая гастроэнтерология. — 2010. — № 8.
- Яковлев Яков Яковлевич, Рудковская Любовь Валерьевна, Лавринова Ольга Викторовна, Матвеева Наталья Владимировна, Андриянова Ольга Ивановна. Тяжёлый гиперэозинофильный синдром с поражением кожи у детей в практике педиатра // Мать и дитя в Кузбассе. — 2022. — № 3 (90). — doi:10.24412/2686-7338-2022-3-69-77.