Синдром Баннаяна — Райли — Рувалькабы
Синдром Банная́на — Ра́йли — Рувалька́бы (СБРР) — это редкое генетическое заболевание, которое чаще всего диагностируется у детей. Оно характеризуется развитием гамартомных, липоматозных или сосудистых опухолей, врождённой макроцефалией, задержкой развития и пигментированными пятнами на гениталиях. Другие распространённые клинические признаки включают пренатальный избыточный рост и нарушения опорно-двигательного аппарата. СБРР обычно наследуется по аутосомно-доминантному типу, связанному с патогенными вариантами гена PTEN. На данный момент не существует стандартного метода лечения пациентов с СБРР[1].
История
СББР впервые был описан в 1960 году американскими врачами Харрисом Райли и Уильямом Смитом, которые выделили три основных клинических признака: макроцефалию, псевдозастой на глазном дне и множественные гемангиомы. Позже, в 1971 году, патолог Джордж Банаян описал случай сочетания макроцефалии с липомами и гемангиомами, а в 1975 году генетик Джонатан Зонана представил дополнительные данные об этом синдроме. В 1980 году педиатр Рожелио Рувалькаба дополнил клиническую картину, сообщив о пациенте с макроцефалией, кишечным полипозом и пигментными пятнами на половых органах. Благодаря вкладу этих исследователей, синдром получил несколько названий в медицинской литературе. Важным этапом в его изучении стало открытие в 1997 году гена PTEN, мутации в котором приводят к развитию этого заболевания[2].
Классификация
СБРР входит в структуру синдрома PTEN-ассоциированных гамартомных опухолей, в который входят[3]:
- синдром Коудена;
- синдром Баннаяна — Райли — Рувалькабы;
- синдром Протея, ассоциированный с PTEN;
- PTEN-ассоциированный Протея-подобный синдром.
Этиология
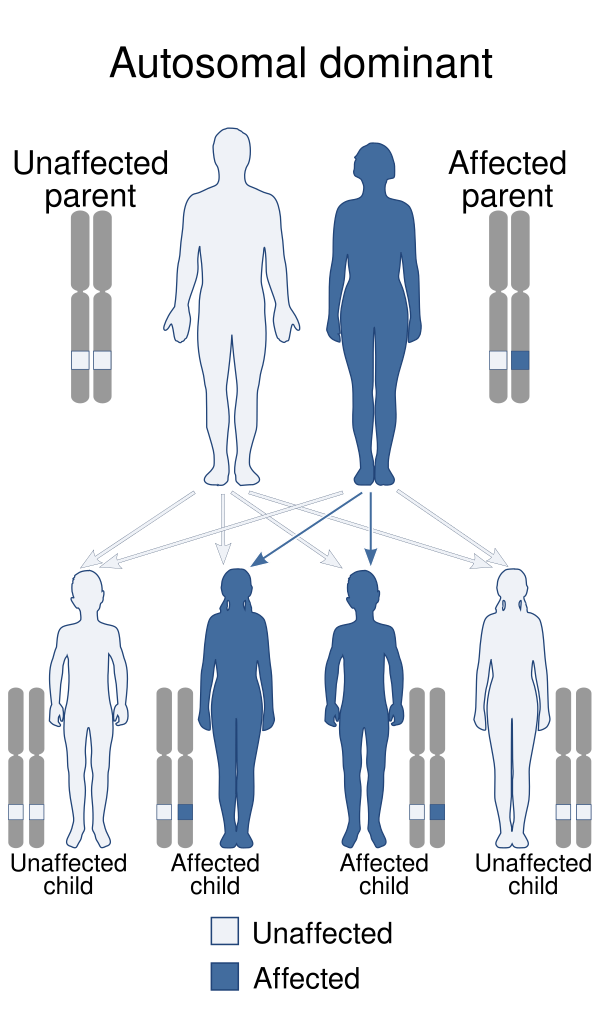
Примерно у 60 % пациентов с СБРР имеется врождённая мутация в гене-супрессоре опухолей PTEN, присутствующая во всех клетках организма. Гены-супрессоры опухолей выполняют важные функции: они замедляют деление клеток, восстанавливают повреждения ДНК и регулируют процесс запрограммированной клеточной гибели (апоптоз). Мутации в таких генах часто приводят к избыточному росту тканей и/или развитию злокачественных новообразований. СБРР наследуется по аутосомно-доминантному типу[4].
Патогенез
Ген PTEN кодирует липидную фосфатазу — белок, выполняющий важную регуляторную функцию. Он ингибирует образование серин/треонинкиназы (участвующей в опухолевом процессе) и предотвращает гиперактивацию фосфоинозитид-3-киназного сигнального пути, который играет ключевую роль в канцерогенезе. В норме PTEN регулирует клеточную пролиферацию и стимулирует апоптоз, тем самым предотвращая неконтролируемое деление клеток. При мутациях в гене PTEN его регуляторная функция нарушается, что приводит к бесконтрольному росту и делению клеток[2].
Диагностика
Клиническая картина
Клинические проявления СБРР отличаются значительной вариабельностью и могут затрагивать различные системы организма. У пациентов наблюдаются кожные изменения, лицевые дисморфии, скелетные аномалии, опухоли щитовидной железы, поражения желудочно-кишечного тракта, центральной нервной системы, глазные нарушения, мышечные патологии и другие особенности. Дети с СБРР обычно рождаются с большими росто-весовыми показателями и часто имеют сосудистые мальформации, проявляющиеся в виде выпуклых красных пятен. Макроцефалия служит ключевым диагностическим критерием СБРР. С возрастом темпы роста замедляются, и к взрослому возрасту параметры тела обычно нормализуются[4].
У 35—45 % пациентов выявляется гамартомный полипоз толстой и прямой кишки, представляющий собой дезорганизованное скопление клеток слизистой оболочки. Кожные проявления включают множественные подкожные или висцеральные липомы, гиперпигментированные пятна на коже полового члена (папулёзные лентигины), потемнение кожных складок (чёрный акантоз) и лицевые папилломатозные папулы[4].
Неврологические нарушения представлены мышечной гипотонией, задержкой психомоторного развития, реже — судорогами, расстройствами аутистического спектра и интеллектуальной недостаточностью. Скелетные аномалии включают воронкообразную деформацию грудной клетки, сколиоз, кифоз или их сочетание (кифосколиоз), а также гипермобильность суставов. Мышечные нарушения характеризуются патологическим включением жировой ткани, фиброзных элементов и аномальных сосудистых структур в толще мышц[4].
Лабораторная диагностика
Молекулярно-генетический анализ: обнаружение мутации гена PTEN методом секвенирования[2].
Эндоскопические исследования позволяют выявить полипоз различных отделов желудочно-кишечного тракта[5].
Для СБРР не существует специфических диагностических критериев, и диагноз обычно устанавливается на основании клинической картины. В педиатрической практике может применяться система балльной оценки, которая в значительной степени основывается на наличии или отсутствии макроцефалии в сочетании с одним из четырёх дополнительных критериев: расстройство аутистического спектра, дерматологические проявления, сосудистые мальформации и/или полипоз желудочно-кишечного тракта. Обнаружение герминальной мутации гена PTEN подтверждает принадлежность пациента с СБРР к группе PTEN-ассоциированных гамартомных опухолей[5].
Дифференциальная диагностика
Дифференциальная диагностика СБРР проводится со следующими состояниями[3]:
- AKT1-ассоциированный синдром Протея;
- синдром ювенильного полипоза;
- синдром Бёрта — Хогг — Дьюбе;
- нейрофиброматоз 1 типа;
- синдром Горлина;
- синдром Пейтца — Егерса;
- синдром Коудена.
Осложнения
СБРР связан с высоким риском возникновения опухолевых образований, лёгочными осложнениями и выраженной предрасположенностью к развитию тромбоза глубоких вен и тромбоэмболии лёгочной артерии[3].
Лечение
Современные подходы к терапии СБРР включают три основных направления: хирургическое лечение, терапию сосудистых аномалий и таргетную терапию ингибиторами mTOR[1].
Хирургические вмешательства остаются основным методом — наиболее часто выполняют удаление липом, полипэктомию гамартомных полипов, в тяжёлых случаях — колэктомию. При поражениях щитовидной железы проводят тиреоидэктомию (описано в 15—20 % случаев)[1].
Для лечения сосудистых мальформаций традиционно применяют склеротерапию, эмболизацию и хирургические методы, однако, несмотря на их эффективность, процедура сопряжена с высоким риском рецидивов и осложнений. В связи с этим перспективным направлением стала таргетная терапия сиролимусом — ингибитором mTOR-пути, гиперактивация которого наблюдается при PTEN-мутациях[1].
Прогноз
Прогноз заболевания остаётся неопределённым и зависит от двух ключевых факторов: первоначальной клинической картины и генотипа пациента (конкретного варианта генетической мутации)[5].
Диспансерное наблюдение
Детям и подросткам с СБРР показаны ежегодные осмотры с оценкой дерматологического статуса, неврологического и психомоторного развития, а также ультразвуковое исследование органов брюшной полости. Ультразвуковое исследование щитовидной железы следует выполнять при первичной диагностике и повторять при выявлении патологических изменений. Особое внимание уделяется симптомам анемии и желудочно-кишечным проявления заболевания (боли в животе, ректальные кровотечения, запоры или диарея)[1].
Примечания
Литература
- Ткачук Елена Анатольевна, Семинский Игорь Жанович. Синдромальный подход в диагностике наследственных заболеваний (лекция) // Байкальский медицинский журнал. — 2023. — № 4. — doi:10.57256/2949-0715-2023-2-4-85-94.
- Цоцонава Жужуна Мурмановна, Белопасов В. В., Ткачёва Н. В. Неопластический потенциал при пороках развития экто- и мезодермальных структур // Неврологический журнал имени Л. О. Бадаляна. — 2020. — № 4.