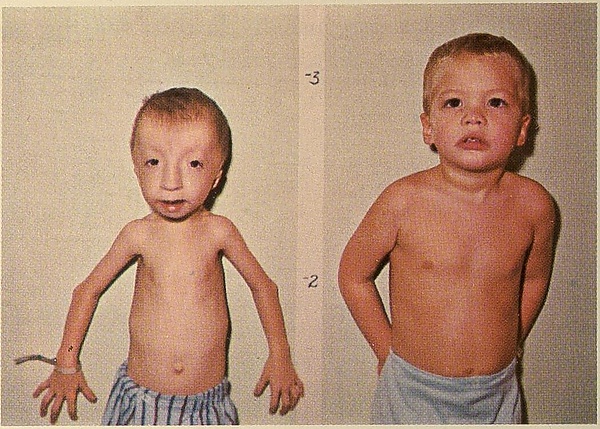
Синдром Секкеля
Синдром Се́ккеля (СС) — это редкое наследственное заболевание, характеризующееся внутриутробной задержкой развития, карликовостью, микроцефалией и умственной отсталостью. Его также называют микроцефалической примордиальной карликовостью или примордиальной карликовостью с микроцефалией из-за характерных особенностей, включающих малый размер головы и черты лица, напоминающие птичьи. Болезнь проявляется ещё до рождения и требует симптоматического и поддерживающего лечения, так как специфической терапии не существует[1].
Общие сведения
История
СС впервые был описан в 1959 году британскими врачами Тревором Манном и Александром Расселом. Более подробное описание заболевания представил в 1960 году Гельмут Секкель, проанализировав два собственных клинических случая и двадцать четыре описанных в медицинской литературе. Во всех наблюдениях отмечались характерные признаки: низкая масса тела при рождении, выраженная микроцефалия, специфические черты лица и нарушения интеллектуального развития. Понятие «птицеголовая карликовость с микроцефалией» было введено ранее немецким патологоанатомом Рудольфом Вирховом, который одним из первых обратил внимание на эту редкую патологию[1].
Классификация
По этиологии СС классифицируется на 8 типов[2]:
- 1 тип — мутация гена ATR;
- 2 тип — мутация гена RBBP8;
- 4 тип — мутация гена CENPJ;
- 5 тип — мутация гена CEP152;
- 6 тип — мутация гена CEP63;
- 7 тип — мутация гена NIN;
- 8 тип — мутация гена DNA2;
- 9 тип — мутация гена TRAIP;
- 10 тип — мутация гена NSMCE2.
Этиология
Патогенез
СС представлен несколькими генетическими формами, каждая из которых обусловлена мутациями в определённых генах[1]:
- 1-й тип заболевания связан с мутациями гена ATR, кодирующего ключевой регуляторный белок, отвечающий за целостность генома, контроль репликации и репарации ДНК;
- 2-й тип вызывается мутациями гена RBBP8, который кодирует белок, участвующий в транскрипции, репарации ДНК и регуляции клеточного цикла;
- 4-й тип ассоциирован с мутациями гена CENPJ, ответственного за синтез центросомного белка, регулирующего формирование микротрубочек;
- 5-й тип обусловлен мутациями гена CEP152, кодирующего белок центросомы, играющего ключевую роль в организации микротрубочек, делении клеток и поддержании их структуры;
- 6-й тип связан с мутациями гена CEP63, также участвующего в функционировании центросом и процессах клеточного деления;
- 7-й тип вызвается мутациями гена NIN, который кодирует центросомный белок, необходимый для правильной организации микротрубочек и восстановления структуры центросом после митоза;
- 8-й тип ассоциирован с мутациями гена DNA2, кодирующего фермент (геликазу/нуклеазу), участвующий в поддержании стабильности ядерной и митохондриальной ДНК;
- 9-й тип связан с мутациями гена TRAIP, белок которого вовлечён в процессы апоптоза;
- 10-й тип обусловлен мутациями гена NSMCE2, кодирующего лигазу, необходимую для репарации ДНК и предотвращения апоптоза при её повреждении.
Ранее предполагалось существование 3-го типа синдрома, связанного с геном на 14-й хромосоме, однако эти данные не подтвердились[1].
Все перечисленные генетические дефекты приводят к внутриутробную нарушению развития организма, что вызывает характерные проявления СС[3].
Эпидемиология
Диагностика
Клиническая картина
СС характеризуется замедленным внутриутробным развитием, что приводит к низкой массе тела при рождении. После рождения также наблюдается отставание в росте, что может вызвать карликовость[3].
У младенцев с СС отмечаются характерные черты лица и черепа (краниофациальные аномалии). У большинства наблюдается микроцефалия. Лоб может быть скошенным назад, нижняя челюсть — маленькой (микрогнатия) и смещённой кзади (ретрогнатия). Нос часто имеет изогнутую треугольную форму, напоминающую клюв, из-за чего средняя часть лица кажется выступающей. У некоторых детей преждевременно закрываются швы черепа (краниосиностоз), что может придавать голове удлинённую или укороченную форму[3].
Дополнительные особенности включают[3]:
- большие глаза с опущенными наружными уголками;
- косоглазие;
- низко расположенные, деформированные уши без мочек;
- высокое арковидное нёбо, иногда с расщелиной;
- асимметрия лица;
- слабая зубная эмаль, аномалии количества и расположения зубов.
Скелетные аномалии могут включать[3]:
- вывих лучевой кости в области запястья;
- подвывихи локтевых или тазобедренных суставов;
- дисплазию тазобедренных суставов;
- ограниченное разгибание коленей;
- костные разрастания конической формы;
- кифосколиоз;
- клинодактилию;
- косолапость, плоскостопие;
- отсутствие одной пары рёбер.
У мальчиков возможен крипторхизм, у девочек — увеличение клитора. Также встречается избыточное оволосение (гирсутизм) и одинарная ладонная складка[3].
У пациентов с СС в редких случаях могут встречаться пороки развития сердечно-сосудистой системы и аноректальные аномалии (недоразвитие прямой кишки и заднего прохода). Некоторые больные имеют эндокринные нарушения, страдают сенсоневральной тугоухостью (снижение слуха из-за поражения внутреннего уха) и различными офтальмологическими патологиями, включая катаракту, глаукому и отслойку сетчатки. Также могут наблюдаться судорожные приступы[1].
У части пациентов выявляются структурные аномалии головного мозга и разнообразные пороки развития центральной нервной системы. В медицинской литературе описаны случаи развития апластической анемии и острого миелоидного лейкоза[1].
Практически у всех больных присутствует умственная отсталость различной степени выраженности — от умеренной до глубокой. Пациенты могут проявлять признаки гиперактивности и сниженной концентрации внимания[1].
У некоторых пациентов встречается аномальное расположение почек (эктопия)[3].
Инструментальная диагностика
При рентгенографии и компьютерной томографии костей выявляются микроцефалия, краниосиностоз, гипоплазия лицевых костей и микрогнатия. Исследование конечностей демонстрирует задержку костного возраста, дисплазию суставов и аномалии костей кистей. При исследовании позвоночника выявляются сколиоз, дисплазию позвонков и возможное отсутствие одной пары рёбер[3][5].
Магнитно-резонансная томография головного мозга позволяет выявить пороки развития центральной нервной системы[1].
Лабораторная диагностика
Диагноз подтверждается при выявлении характерных мутаций методом секвенирования[1].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими состояниями[3]:
- синдром Мейера — Горлина;
- синдром Рассела — Сильвера;
- остеодиспластическая примордиальная карликовость тип I/III;
- остеодиспластическая примордиальная карликовость тип II.
Лечение
Лечение СС носит симптоматический и поддерживающий характер, так как специфической терапии данного заболевания не существует. Основное внимание уделяется комплексной реабилитации, включающей регулярные нейрореабилитационные мероприятия — лечебную физкультуру, массаж и физиотерапевтические процедуры. Важным компонентом терапии является психолого-педагогическая поддержка с ранней коррекцией развития и специальным обучением, адаптированным к интеллектуальным возможностям пациента. В медикаментозной терапии применяются препараты рекомбинантного гормона роста, особенно у детей с выраженной постнатальной задержкой роста, а также ноотропные средства и препараты, улучшающие обменные процессы[1].
Прогноз
Прогноз при СС вариабелен и определяется тяжестью врождённых аномалий, степенью выраженности клинических проявлений и наличием сопутствующих осложнений. В медицинской литературе описан случай пациента с этим заболеванием, достигшего 75-летнего возраста, что свидетельствует о возможности относительно благоприятного течения при адекватном медицинском сопровождении. Однако в большинстве случаев продолжительность жизни снижена ввиду множественных органных нарушений[1].
Примечания
Литература
- Нагаева Е. В. Внутриутробная задержка роста // Педиатрия. Журнал им. Г. Н. Сперанского. — 2009. — № 5.
- Голоунина Ольга Олеговна, Фадеев Валентин Викторович, Белая Жанна Евгеньевна. Наследственные синдромы с признаками преждевременного старения // Остеопороз и остеопатии. — 2019. — № 3.