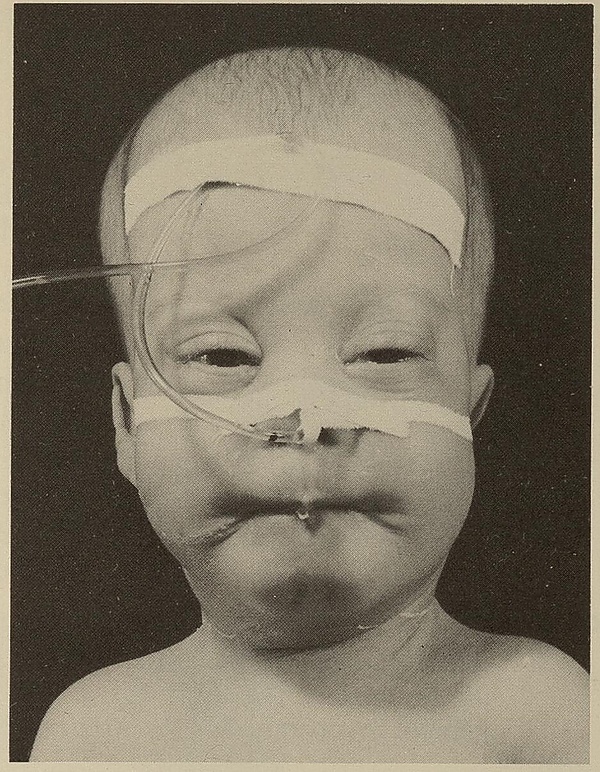
Синдром Цельвегера
Синдро́м Цельве́гера (СЦ, цереброгепаторена́льный синдро́м) — редкое наследственное заболевание, относящееся к группе пероксисомных болезней. Для заболевания характерны челюстно-лицевые аномалии, выраженная мышечная слабость, судорожные приступы, а также поражение печени и других внутренних органов. Патология возникает из-за дефекта белков пероксинов, которые обеспечивают нормальное формирование и работу пероксисом. В результате их недостаточности в тканях и биологических жидкостях накапливаются токсичные вещества, повреждающие органы. Причиной болезни являются мутации в одном из 13 генов PEX[1].
Общие сведения
История
Первые случаи синдрома Цельвегера были описаны в 1964 году американскими врачами Боуэном, Ли и Цельвегером, которые наблюдали множественные врождённые пороки у четырёх детей из двух разных семей. В 1967 году исследователи Пассарж и МакАдамс зафиксировали ряд схожих случаев и предложили термин «цереброгепаторенальный синдром». Однако позже, после анализа всех известных на тот момент данных, Опитц и его коллеги пришли к выводу, что лишь у двух из описанных ранее пациентов действительно имелся этот синдром. Поскольку именно Цельвегер впервые описал эти случаи, заболевание получило название «синдром Цельвегера». Дальнейшие исследования позволили уточнить генетическую природу болезни. К 2011 году были систематизированы данные о мутациях в 12 генах PEX, приводящих к развитию этого заболевания[1].
Классификация
Группа пероксисомных заболеваний спектра синдрома Цельвегера (СЦ) включает в себя[1][2]:
- синдром Цельвегера;
- неонатальную адренолейкодистрофию;
- инфантильную болезнь Рефмуса.
Пациентов с заболеваниями СЦ можно условно разделить на три группы в зависимости от возраста манифестации симптомов[3]:
- Неонатально-младенческая форма.
- Детская форма.
- Подростково-взрослая.
Этиология
СЦ развивается из-за мутаций в различных генах, необходимых для биогенеза пероксисом. Известно, что заболевание связано с мутациями как минимум в 13 различных генах PEX, кодирующих белки пероксины (белки сборки пероксисом). Наиболее распространёнными являются мутации в генах PEX1 и PEX6, которые встречаются примерно у 65 % пациентов. Эти гены кодируют АТФ-азы, необходимые для транспорта белков из цитозоля в пероксисомы[2].
Патогенез
Пероксисомы участвуют в бета-окислении жирных кислот с очень длинной цепью, альфа-окислении разветвлённых жирных кислот, катаболизме аминокислот и этанола, синтезе жёлчных кислот, стероидных гормонов, глюконеогенезе, а также в образовании плазмалогенов — важных компонентов клеточных мембран и миелина. Кроме того, они обезвреживают цитотоксичную перекись водорода[2].
СЦ характеризуется накоплением жирных кислот с очень длинной цепью. Нарушение синтеза стероидов и накопление жирных кислот в клетках надпочечников приводят к снижению уровня адренокортикотропного гормона и других стероидных гормонов. Недостаточное расщепление перекиси водорода и аномальное накопление жирных кислот вызывают повреждение нейрональных мембран и демиелинизацию[2].
Основные патологические изменения наблюдаются в почках (кортикальные кисты), печени (фиброз) и головном мозге (демиелинизация, полимикрогирия центральных извилин), что и дало заболеванию альтернативное название — цереброгепаторенальный синдром[2].
Эпидемиология
Распространённость заболеваний СЦ оценивается как 1 случай на 50 000 новорождённых в США. Предполагается, что СЦ встречается во всем мире, однако частота возникновения может варьировать в зависимости от региона. Например, в франкоканадском регионе Квебек частота СЦ составляет примерно 1 случай на 12 000 новорождённых, тогда как в Японии этот показатель значительно ниже — около 1 случая на 500 000 рождений. Данных о распространённости СЦ в Российской Федерации нет[1][3].
Диагностика
Клиническая картина зависит от возраста манифестации заболевания[3]:
- Неонатально-младенческая форма. У пациентов этой группы симптомы проявляются в неонатальном периоде, включая печёночную недостаточность и выраженную гипотонию, что приводит к затяжной желтухе и трудностям с кормлением. У таких пациентов часто наблюдаются эпилептические приступы. Характерные дизморфические черты, особенно лицевые аномалии, обычно хорошо заметны. Типичными, но не всегда распознаваемыми при первичном осмотре признаками являются нейросенсорная тугоухость и глазные аномалии (ретинопатия, катаракта, глаукома).
- Детская форма. У пациентов с детской формой заболеваний СЦ наблюдается более разнообразная симптоматика по сравнению с неонатально-младенческой формой. Первичное обращение к врачу обычно связано с задержкой развития психомоторных навыков. Характерными офтальмологическими проявлениями являются пигментный ретинит, катаракта и глаукома, которые часто приводят к развитию ранней слепоты и туннельного зрения. Практически у всех пациентов присутствует нейросенсорная тугоухость. Со стороны гепатобилиарной системы типичны гепатомегалия и нарушения функции печени, проявляющиеся коагулопатией. У значительной части пациентов отмечаются эпилептические приступы. В отличие от неонатально-младенческой формы, краниофациальные дизморфические признаки выражены в меньшей степени.
- Подростковая-взрослая форма. У пациентов подростково-взрослой формы заболевания симптомы выражены менее значительно, при этом диагноз может быть установлен как в позднем детском возрасте, так и у взрослых. Наиболее стабильными клиническими проявлениями выступают различные нарушения зрения и нейросенсорная тугоухость. Краниофациальные дизморфические признаки могут наблюдаться, но в ряде случаев полностью отсутствуют. Степень задержки развития существенно варьирует — от выраженных форм до случаев с сохранением нормального интеллекта. Уровень повседневной активности пациентов колеблется от полной самостоятельности до состояния, требующего постоянного круглосуточного ухода. Особое внимание следует обратить на частые случаи первичной надпочечниковой недостаточности, которая нередко остаётся нераспознанной. Характерно наличие периферической нейропатии, мозжечковой атаксии и пирамидных симптомов. Течение заболевания в большинстве случаев медленно прогрессирующее, однако возможны длительные периоды стабилизации продолжительностью в многие годы.
По данным магнитно-резонансной томографии выявляется двусторонняя симметричная демиелинизация в теменно-затылочной области с вовлечением мозолистого тела. В дальнейшем процесс демиелинизации распространяется в переднем и латеральном направлениях. Магнитно-резонансная спектроскопия выявляет снижение уровня N-ацетиласпартата, повышение пиков холина (отражающего активную демиелинизацию) и умеренное увеличение лактатного пика (свидетельствующего о воспалительном процессе). Изменения на спектроскопии появляются раньше, чем видимые структурные изменения на магинтно-резонансной томографии[3].
Биохимический анализ крови: характерно повышение концентрации жирных кислот с очень длинной цепью, фитановой и простановой кислот и жёлчных кислот[1].
Биохимический анализ мочи: характерна повышенная концентрация пипеколиновой и жёлчных кислот[1].
Молекулярно-генетический анализ: выявляется мутация в гене PEX методом полимеразной цепной реакции или секвенирования[3].
При наличии подозрений на СЦ и нормальных показателях анализов крови и мочи рекомендуется проведение дополнительных исследований в фибробластах, культивированных при температуре 40 °C. Культуры фибробластов кожи демонстрируют дисфункцию пероксисомальных матриксных протеинов внутриклеточной локализации, а именно недостаток пероксисомной каталазы и повышение цитозольной каталазы[3][4].
Дифференциальный диагноз
Дифференциальный диагноз проводится со следующими состояниями[2][5]:
- синдром Дауна;
- синдром Прадера — Вилли;
- спинальная мышечная атрофия;
- дефицит ацил-КоА-оксидазы 1-го типа;
- дефицит D-бифункционального белка;
- синдром Ушера 1-го и 2-го типа;
- синдром Коккейна;
- синдром Альпорта;
- синдром Варденбурга;
- классическая болезнь Рефсума;
- синдром Лоу;
- галактоземия;
- врождённые инфекции;
- кровоизлияние в надпочечники;
- Х-сцепленная адренолейкодистрофия;
- инфекционный адреналит.
Осложнения
Осложнения СЦ включают[2]:
- желудочно-кишечные кровотечения;
- печёночная недостаточность;
- пневмония;
- респираторный дистресс-синдром;
- инфекционные осложнения;
- остеопороз.
Лечение
Специфических методов лечения СЦ не существует. Основной подход заключается в симптоматической поддерживающей терапии. При эпилептических приступах назначают противосудорожные препараты. Печёночные нарушения (коагулопатия, холестаз) требуют назначения витамина К и жёлчных кислот, надпочечниковая недостаточность — заместительной терапии кортизоном, при остеопорозе применяют витамин D[1].
Коррекция слуховых нарушений осуществляется с помощью слуховых аппаратов или кохлеарной имплантации. Зрительные расстройства компенсируют подбором очков, а катаракта устраняется хирургическим путём[1].
Прогноз
Прогноз заболевания напрямую зависит от тяжести клинических проявлений. Наиболее неблагоприятный исход характерен для неонатальных форм заболевания. При более позднем начале болезни неврологические нарушения и задержка моторного развития обычно менее выражены, что улучшает прогноз пациентов[1].
Диспансерное наблюдение
Необходимо регулярно проводить комплексный мониторинг состояния пациента с СЦ. Обязательными являются ежегодные обследования: аудиологическое исследование и осмотр офтальмолога, контроль функции печени и показателей свёртывающей системы крови, ультразвуковое исследование и эластометрия печени для оценки её структуры[5].
Требуется регулярный мониторинг судорожной активности и проведение магнитно-резонансной томографии головного мозга для выявления изменений белого вещества, которые могут объяснить когнитивные или двигательные нарушения. Важно ежегодно оценивать динамику развития и когнитивные способности пациента. Начиная с годовалого возраста необходимо ежегодно определять уровень адренокортикотропного гормона и кортизола[5].
Стоматологические осмотры следует проводить каждые полгода[5].
У пациентов старшего возраста (начиная с 4—6 лет) необходимо проводить регулярный мониторинг возможного развития гипероксалурии. Для этого выполняют определение концентрации щавелевой кислоты и креатинина в моче с расчётом их соотношения. Дополнительно рекомендуется проведение ультразвукового исследования почек, которое позволяет выявить как микролиты, так и макролиты в мочевыделительной системе. Такой комплексный подход к диагностике помогает своевременно выявлять и предупреждать развитие осложнений, связанных с нарушением обмена оксалатов[4].
Профилактика
Для всех пациентов с СЦ настоятельно рекомендуется ежегодная вакцинация против сезонного гриппа[4].
Примечания
Литература
- Мамедов И. С., Смолина Юлия Александровна, Сухоруков В. С., Новиков П. В. Диагностика пероксисомных болезней у детей // Клиническая лабораторная диагностика. — 2012. — № 3.
- Гончарь М. А., Муратов Г. Р., Логвинова О. Л., Пушкарь Е. М., Помазуновская Е. П., Омельченко Е. В., Шульга Н. В., Галдина И. М., Зубко А. С., Стребуль Н. В. Пероксисомные биогенные нарушения в спектре синдрома Цельвегера: диагностика, мониторинг и лечение согласно рекомендациям глобальной фундации пероксисомных заболеваний // Здоровье ребёнка. — 2018. — № 2.