Синдром Клиппеля — Треноне — Вебера
Синдром Кли́ппеля — Трено́не — Ве́бера (СКТВ) представляет собой врождённую сосудистую патологию, характеризующуюся аномальным развитием периферических сосудов с образованием патологических артериовенозных соединений. Эти изменения приводят к нарушению венозного кровообращения в поражённой конечности, что вызывает прогрессирующее варикозное расширение поверхностных вен как верхних, так и нижних конечностей с неуклонным нарастанием симптоматики[1].
Общие сведения
История
В 1900 году Морис Клиппель и Поль Треноне описали пациента с асимметричной гипертрофией мягких тканей и костей, сочетающейся с гемангиоматозными поражениями кожи, используя термин "остеогипертрофический варикозный невус". В 1907 году Фредерик Паркс Вебер описал ещё три случая и предложил классическую триаду признаков: кожные невусы, костная и мягкотканная гемигипертрофия, и варикозное расширение вен. В 1918 году Вебер уточнил описание как: гемангиэктатическую гипертрофию конечностей, врождённую флебартериэктазию и врождённые варикозные вены, добавив ещё один компонент - врождённые артериовенозные фистулы. С этого времени стал использоваться тройной эпоним: синдром Клиппеля-Треноне-Вебера[2][3].
Классификация
По тяжести поражения СКТВ классифицируется на[4]:
- лёгкая степень: характерны "гладкие" сосудистые пятна (портвейные пятна), типичные эмбриональные вены (в пределах сегментов конечности);
- средняя степень; дополнительно к симптомам лёгкой степени определяются симметричное увеличение окружности конечности, несимметричная гипертрофия, бугристые сосудистые пятна (невус пламенеющий), локальный ДВС-синдром
- тяжёлая степень: дополнительно к симптомам средней степени определяются гигантизм стоп, макродактилия, слоновость, контрактуры мышц, деформации конечностей, поражение двух и более конечностей, распространение эмбриональных вен на всю конечность, поражение сосудов органов малого таза, распространённый ДВС-синдром;
- крайне тяжёлая степень: дополнительно к симптомам тяжёлой степени уродующая гипертрофия костных и мягких тканей, "венозные соты" на голени, мелена и гематурия, кисты и лимфангиомы брюшной полости и забрюшинного пространства.
Этиология
Этиология синдрома остаётся невыясненной, однако в научной литературе обсуждаются несколько теорий его происхождения. Согласно первой теории, заболевание может развиваться вследствие воздействия повреждающих факторов во внутриутробном периоде. Генетическая теория предполагает связь с хромосомными аномалиями, включая делеции 5q или 11p, а также транслокацию 8q22.3 и 14q13. Другие исследователи рассматривают в качестве возможной причины компрессию симпатических ганглиев микроскопическими артериовенозными анастомозами. Также выдвинута гипотеза о роли повышенной экспрессии инсулиноподобного фактора роста-2[5].
Современные исследования связывают развитие СКТВ соматическими мутациями в гене PIK3CA, кодирующем каталитическую субъединицу фосфатидилинозитол-4,5-бисфосфат-3-киназы. Эти мутации вызывают активацию сигнального пути PI3K/протеинкиназы и чрезмерный рост клеток вследствие нарушения регуляции mTORC2-пути[2].
Патогенез
В патогенезе СКТВ обычно выделяют несколько ключевых причин. К ним относятся аплазия или гипоплазия вен, сдавление венозных сосудов эмбриональными тяжами или артериями, а также врождённая недостаточность клапанного аппарата, сопровождающаяся расширением просвета глубоких вен. Кроме того, врождённые артериовенозные фистулы неизбежно провоцируют варикозное расширение вен[1].
Важную роль в патогенезе играет мутация в гене PIK3CA, ответственном за кодирование белка p110α – каталитической субъединицы фермента фосфатидилинозитол-3-киназы (PI3K). Данный фермент играет ключевую роль в передаче внутриклеточных сигналов, регулируя фундаментальные клеточные процессы, включая пролиферацию, их миграцию и выживаемость. PI3K имеет критическое значение для нормального развития тканей организма. При мутации в гене PIK3CA образуется изменённая субъединица p110α, которая придаёт ферменту аномально высокую активность, что приводит к нарушению регуляции клеточного цикла. В результате клетки приобретают способность к неконтролируемому росту и делению. Такая патологическая пролиферация лежит в основе характерных проявлений синдрома: аномального роста костной ткани, гипертрофии мягких тканей и избыточного разрастания кровеносных сосудов. Эти молекулярные нарушения объясняют основные клинические проявления заболевания, связанные с избыточным ростом различных тканей[4].
Эпидемиология
В медицинской литературе зафиксировано приблизительно 1000 случаев СКТВ. Данное заболевание не имеет чёткой половой или расовой предрасположенности и встречается с одинаковой частотой у мужчин и женщин, а также среди различных этнических групп[5].
Диагностика
Клиническая картина
При рождении СКТВ проявляется в виде неравномерных капиллярных пятен, напоминающих географическую карту. С возрастом на их поверхности образуются мелкие лимфатические пузырьки, которые часто выделяют прозрачную жидкость и темнеют из-за кровоизлияний внутри очага[6].
Лимфатическая мальформация характеризуется локальным или генерализованным увеличением тканей, вызванным микро- и макрокистозными аномалиями, иногда в сочетании с лимфедемой. Нередко наблюдается лимфатический отёк и избыточное отложение жира. Лимфатические аномалии могут также затрагивать органы малого таза, мочевой пузырь и нижние отделы желудочно-кишечного тракта. Кисты лимфатических сосудов в селезёнке встречаются часто [6].
Венозные мальформации присутствуют всегда, но их выраженность варьируется и затрагивает всю поражённую конечность. Характерной особенностью являются аномальные эмбриональные вены, так называемая "маргинальная система". Расширение поверхностных вен может быть незаметным в младенчестве, но становится более выраженным с возрастом. Лимфатические и венозные аномалии могут также поражать органы малого таза и брюшной полости, приводя к кровотечениям из прямой кишки, влагалища или мочевого пузыря. Избыточное отложение жира сопровождает венозные и лимфатические нарушения[6].
У многих пациентов с обширными венозными аномалиями развивается гематологическое нарушение – локальная внутрисосудистая коагулопатия. Застой крови в расширенных венах может приводить к образованию тромбов и провоцировать генерализованное нарушение свёртываемости – диссеминированное внутрисосудистое свёртывание[6].
Увеличение конечности может варьироваться от незначительного до резко выраженного. Часто наблюдается удлинение поражённой конечности, но в некоторых случаях она, наоборот, короче здоровой. Нередко отмечается увеличение противоположной стопы. У детей с тяжёлыми формами заболевания хромота появляется практически сразу после начала ходьбы. К полутора годам жизни у них также возникают жалобы на повышенную утомляемость поражённой конечности. У пациентов с наиболее тяжёлыми формами заболевания наблюдаются выраженные ограничения подвижности конечности – затруднения при сгибании, разгибании, супинации и пронации. Эти нарушения связаны с потерей эластичности мягких тканей из-за интенсивного фиброза в подкожной клетчатке и мышечных структурах[4][6].
Инструментальная диагностика
Ультразвуковые исследования являются первоочередными методами диагностики. Ультразвуковая допплерография – позволяет определить тип кровотока (высоко- или низкоскоростной), а также выявить возможное отсутствие кровотока в зоне поражения[4].
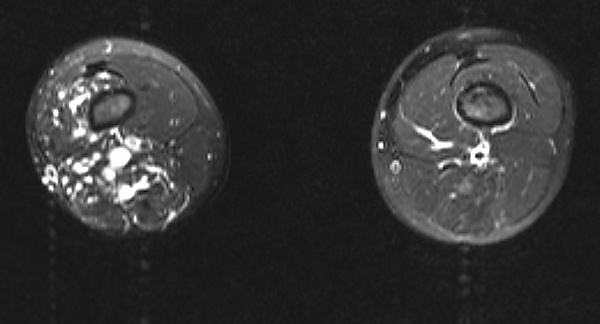
Магнитно-резонансная томография предоставляет основную информацию о распространённости патологического процесса и его анатомическом взаимодействии с окружающими тканями, структурами и органами. Магнитно-резонансная томография с динамическим контрастным усилением позволяет детально оценить характеристики кровотока, степень поражения мягких тканей и их соотношение с неизменёнными структурами. Эта методика имеет важное значение не только для подтверждения сосудистой патологии, но и для дифференциальной диагностики между низко- и высокоскоростными мальформациями[4].
Флебография остаётся одним из наиболее точных методов исследования при дисплазиях магистральных вен. Различные методики контрастирования венозного русла позволяют точно определить локализацию и характер патологических изменений[4].
Ангиография включает несколько высокоточных методик[4]:
- селективная и суперселективная артериография – позволяет детально оценить состояние артериального русла;
- чрескожная прямая пункционная артериография – используется для прицельного исследования артерий;
- чрескожная прямая пункционная флебография – применяется для контрастирования венозной системы.
Лабораторная диагностика
Молекулярно-генетический анализ с выявлением возможных мутаций методом секвенирования[2].
Дифференциальная диагностика
Дифференциальная диагностика СКТВ проводится со следующими состояниями[2][4]:
- синдром Паркса-Вебера;
- синдром Стерджа-Вебера;
- синдром Протея;
- врождённая лимфатическая атрезия;
- синдром Маффуччи;
- синдром Боккенхеймера;
- капошиформная гемангиоэндотелиома;
- синдром CLOVES;
- мегалэнцефалия-капиллярная мальформация;
- диффузная капиллярная мальформация с гипертрофией;
- фиброзно-жировая гипертрофия;
- синдром Беквита — Видемана;
- плексиформная нейрофиброма.
Осложнения
У пациентов с СКТВ может развиваться целлюлит поражённой конечности, вызванный лимфатическим стазом и пропотеванием лимфы, что при недостаточном уходе способно привести к сепсису. Выраженный венозный и лимфатический застой повышает риск развития локальной коагулопатии[2].
Хронические кровотечения из сосудистых мальформаций желудочно-кишечного тракта могут протекать скрыто, требуя многократных переливаний крови и приёма препаратов железа. В некоторых случаях кровотечения становятся жизнеугрожающими, особенно при развитии диссеминированного внутрисосудистого свёртывания[2].
Повторные тромбоэмболии лёгочной артерии, возникающие на фоне тромбоза глубоких вен, способны вызывать хронические изменения в мелких сосудах лёгких, приводя к лёгочной гипертензии[2].
Лечение
На сегодняшний день лечение сосудистых мальформаций проводится в соответствии с общими принципами флебологии, однако единого подхода к терапии дисплазий магистральных вен не существует. Мнения специалистов по этому вопросу существенно расходятся[4].
В современной практике применяется широкий спектр лечебных методик[3][4]:
- консервативные методы: включают медикаментозную (алпелисиб) и немедикаментозную (компрессионная терапия, использование ортопедических приспособлений) терапию.
- хирургические методы: эндоваскулярная эмболизация, лазерная терапия, радиочастотная абляция поражённых вен, склеротерапия, открытые хирургические вмешательства.
Прогноз
СКТВ характеризуется широким спектром клинических проявлений, а его прогноз напрямую зависит от тяжести сосудистых мальформаций. С течением времени патологические изменения прогрессируют: усиливается гипертрофия тканей и нарастает венозная недостаточность. Особую опасность представляют острые кровотечения из сосудистых мальформаций желудочно-кишечного тракта, которые без экстренного медицинского вмешательства могут привести к массивной кровопотере с риском летального исхода. Кроме того, повторные эпизоды тромбоза глубоких вен существенно повышают вероятность развития тромбоэмболии лёгочной артерии, которая в тяжёлых случаях может стать фатальной[2].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
- ↑ 1 2 Скорняков С. Н.; Сабадаш Е. В.; Медвинский И. Д. и другие. Хронический абсцесс легкого у пациента с синдромом Клиппеля – Треноне – Вебера – Рубашова. — 2018. — № 3(I). — С. 36-39.
- ↑ 1 2 3 4 5 6 7 8 Naganathan S., Tadi P. Klippel-Trenaunay-Weber Syndrome (англ.) // StatPearls [Internet]. — Treasure Island (FL): StatPearls Publishing, 2025.
- ↑ 1 2 Camila K Janniger. Klippel-Trenaunay-Weber Syndrome (англ.). Medscape (16 сентября 2022).
- ↑ 1 2 3 4 5 6 7 8 9 10 Азаров Михаил Валерьевич, Купатадзе Димитрий Димитриевич, Набоков Виктор Владиславович. Синдром Клиппеля - Треноне. Этиология, патогенез, диагностика и лечение // Педиатр. — 2018. — № 2.
- ↑ 1 2 Комарова И. Б.; Зыков В. П.; Тамбиев И. Е.; Владимирова С. А.; Степанищев И. Л.; Мамедова Л. С.; Козлова О. В. Вариант синдрома Клиппеля-Треноне-Вебера. — 2014. — Т. 114, № 1-2. — С. 40-44.
- ↑ 1 2 3 4 5 Klippel-Trenaunay Syndrome (англ.). National Organization for Rare Disorders (6 июня 2023).
Литература
- Чеканов А.М., Чеканов М.Н., Осипенко М.Ф., Штофин С.Г., Шамрай А.Б., Благитко Е.М. Абдоминальный вариант синдрома Клиппеля-Треноне (рус.) // Экспериментальная и клиническая гастроэнтерология : журнальная статья. — 2018. — № 7. — С. 155-157.
- Багдасарьян А.С., Сирунянц А.А., Андреева М.Б., Ремизова А.И., Пухняк Д.В., Камалян Ж.А. Синдром Клиппеля-Треноне в практике врача скорой медицинской помощи (рус.) // Кубанский научный медицинский вестник : журнальная статья. — 2018. — Т. 25, № 2. — С. 183-186. — doi:10.25207/1608-6228-2018-25-2-183-186.