Синдром Циммермана — Лабанда
Синдром Ци́ммермана — Лаба́нда (СЦЛ) — аутосомно-доминантное заболевание, обусловленное мутациями в различных генах. Клиническая картина включает множество признаков: грубые черты лица, выступающую нижнюю челюсть, длинные уши, потерю слуха, густые и сросшиеся брови, катаракту, утолщённые губы, гиперплазию дёсен, кардиомиопатию, дилатацию корня аорты, гепатомегалию, внепечёночную билиарную атрезию, сколиоз, гипоплазию ногтей, гипертрихоз, мышечную гипотонию и судороги. Прогноз зависит от фенотипических проявлений, но в целом синдром не является жизнеугрожающим[2].
Общие сведения
История
Это заболевание было впервые описано в 1928 году немецким анатомом и гистологом Карлом Циммерманом. Лабанд и соавторы в 1964 году описали две семьи, у которых наблюдался фиброматоз дёсен в сочетании с «истощением» концевых фаланг и отсутствием или дисплазией ногтевых пластин. Позднее, в 1971 году, описание болезни пересмотрел и дополнил Карл Якоб Виткоп[3][4].
Классификация
Этиология
СЦЛ является генетически гетерогенным заболеванием. Описаны гетерозиготные миссенс-мутации в генах KCNH1 и KCNN3 , а также более редкие миссенс-мутации в гене ATP6V1B2[6].
Патогенез
Патогенез СЦЛ до конца не определён[7].
Патогенез СЦЛ 1-го типа связан с мутациями в гене KCNH1, кодирующем потенциал-зависимый калиевый канал Eag1 (Kv10.1). Эти мутации вызывают структурные изменения в ключевых доменах канала: сенсоре напряжения S4, линкере S4—S5 и гидрофобных кластерах сегментов S5—S6. Особое значение имеет замена Gly469 в S6 сегменте, которая приводит к электростатическому отталкиванию положительно заряженных остатков аргинина в закрытом состоянии канала, стабилизации его открытого состояния с пониженной проводимостью и нарушению процесса тетрамеризации субъединиц. Дополнительно мутации в гидрофобных остатках Ile467, Leu352 и Val356 изменяют конформационные переходы между открытым и закрытым состояниями канала, что проявляется аномальной активацией или инактивацией, нарушением реполяризации мембраны и патологическим усилением функции. Эти молекулярные нарушения лежат в основе характерных неврологических и соматических проявлений синдрома[8][9].
СЦЛ 2-го типа связан с мутацией в гене ATP6V1B2. Ген ATP6V1B2 кодирует одну из субъединиц вакуолярной протонной АТФазы — сложного ферментного комплекса, ответственного за регуляцию кислотности внутриклеточных органелл в эукариотических клетках. Нормальное функционирование АТФазы крайне важно для осуществления внутриклеточного транспорта белков, активации ферментных предшественников, поглощения веществ путём эндоцитоза и создания протонного градиента в синаптических пузырьках. На 2025 год механизмы развития СЦЛ-2 остаются не полностью изученными. Однако известно, что нарушения в работе V-типа протонной АТФазы, вызванные генетическими дефектами, приводят к нарушению кислотно-щелочного баланса в различных клеточных структурах. Это, в свою очередь, вызывает каскад патологических изменений, затрагивающих процессы клеточного роста и дифференцировки, что клинически проявляется разнообразными симптомами, характерными для СЦЛ[10][11].
Ген KCNN3 отвечает за кодирование кальций-зависимого калиевого канала SK3, который относится к семейству малопроводящих SK-каналов. Данные каналы функционируют в составе белкового комплекса, включающего, помимо самих поровых субъединиц, постоянно связанный с ними кальмодулин (выполняющий роль кальциевого сенсора), а также ферменты протеинкиназу CK2 и протеинфосфатазу 2A. Важную роль в регуляции каналов играет процесс фосфорилирования кальмодулина протеинкиназой CK2, что изменяет их чувствительность к ионам кальция. Мутации в гене KCNN3, ассоциированные с развитием заболевания, приводят к усилению функции соответствующих ионных каналов. Это проявляется в виде аномально высокой чувствительности к кальцию, что вызывает ускоренную и более выраженную активацию мутантных каналов по сравнению с их нормальными аналогами[12].
Эпидемиология
Всего в мире зарегистрировано около 50 случаев СЦЛ[6].
Диагностика
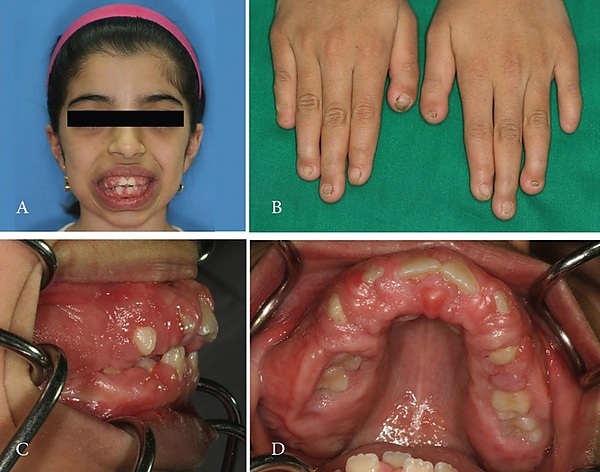
СЦЛ характеризуется прогрессирующей диффузной гипертрофией дёсен, часто сопровождающейся множеством непрорезавшихся зубов и деформациями костей верхней челюсти. У пациентов наблюдается грубоватый внешний вид лица, включая мясистый мягкий нос, утолщённые губы, большую выступающую верхнюю губу, толстые и обвисшие уши, а также увеличенные лицевые кости и нижнюю челюсть. Дополнительными признаками являются отсутствие или недоразвитие концевых фаланг и ногтей на пальцах рук и ног, а также увеличенные размеры пальцев рук и ног[6][7].
К более вариабельным симптомам относятся гиперподвижность суставов, гепатоспленомегалия, лёгкий гирсутизм , потеря слуха и косоглазие. Умственная отсталость встречается не у всех пациентов и обычно имеет лёгкую или умеренную степень выраженности. Разросшиеся десневые ткани могут затруднять речь, что в сочетании с другими проявлениями заболевания существенно влияет на качество жизни пациентов[6].
Молекулярно-генетический анализ: выявление мутаций в генах KCNH1, ATP6V1B2 и KCNN3 методом секвенирования[6].
Дифференциальная диагностика
Дифференциальная диагностика СЦЛ проводится со следующими состояниями[6]:
- синдром лицевого дисморфизма-гипертрихоза-эпилепсии-умственной отсталости и задержки развития-гипертрофии дёсен;
- синдром Канту;
- синдром глухоты-ониходистрофии-остеодистрофии-умственной отсталости-судорог;
- синдром DDOD;
- синдром Амбраса;
- синдром Барбера — Сэя;
- изолированный фиброматоз дёсен.
Лечение
На 2025 год не существует известного способа излечения СЦЛ. Проводится симптоматическая и патогенетическая терапия: физиотерапия, эрготерапия и занятия с логопедом. При наличии эпилепсии применяются противосудорожные препараты. Детям, не способным самостоятельно питаться, может потребоваться нутритивная поддержка[13].
Прогноз
Прогноз зависит от фенотипических проявлений. Синдром не представляет угрозы для жизни[6].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- М. Х. Исаева, В. А. Белова, Д. О. Коростин, А. В. Дегтярёва. Генетические аспекты этиологии билиарной атрезии // Вестник Российского государственного медицинского университета. — 2020. — № 6. — doi:10.24075/vrgmu.2020.069.
- Волынец Г. В., Хавкин А. И., Никитин А. В. Современный взгляд на билиарную атрезию у детей. // Экспериментальная и клиническая гастроэнтерология. — 2020. — № 1 (173).