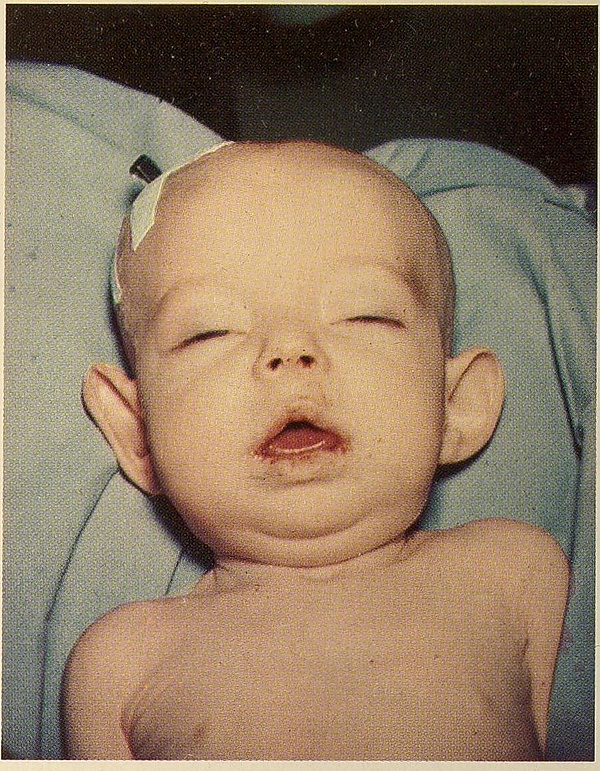
Синдром Донохью
Синдром До́нохью (СД) представляет собой наиболее тяжёлую форму врождённой инсулинорезистентности, вызванную мутациями в обеих копиях гена рецептора инсулина, и характеризуется выраженной задержкой внутриутробного развития, специфическими дизморфическими чертами («эльфоподобное» лицо, липоатрофия, чёрный акантоз, гипертрихоз), а также метаболическими нарушениями, включая постпрандиальную гипергликемию и гипогликемию натощак, гепатомегалию и гипертрофию миокарда. Прогноз заболевания крайне неблагоприятный — большинство детей не доживают до двух лет вследствие интеркуррентных инфекций верхних дыхательных путей, эпизодов тяжёлых гипогликемий или кардиомиопатии, при этом эффективных методов лечения в настоящее время не существует[1].
История
В 1948 году Донохью впервые описал состояние, которое назвал дисэндокринизмом, у белой девочки-младенца, рождённой от близкородственного брака. Ребёнок появился на свет с задержкой внутриутробного развития, весом всего 1,75 кг, и к 28-му дню жизни у неё наблюдалась дальнейшая потеря веса. Также отмечались значительное вздутие живота и множественные подкожные абсцессы на волосистой части головы, спине и лбу. Состояние быстро ухудшалось, и ребёнок умер в возрасте 8 недель. В 1954 году Донохью и Учида обнаружили те же клинические особенности и фенотип у второго ребёнка в этой семье. Для описания синдрома был предложен термин «лепречаунизм», поскольку внешний вид пациентов напоминал карикатурных персонажей — лепреконов. Однако, чтобы избежать стигматизирующего названия, в настоящее время это состояние чаще называют синдромом Донохью[2].
Классификация
Классификация мутаций гена INSR по типу нарушения функции рецептора[1]:
- мутации, вызывающие уменьшение биосинтеза инсулина;
- мутации, нарушающие внутриклеточный транспорт и посттрансляционный процессинг рецептора;
- мутации, приводящие к дефектам связывания инсулина с рецептором;
- мутации, сопровождающиеся снижением тирозинкиназной активности рецептора;
- мутации, ускоряющие деградацию инсулинового рецептора.
Этиология
СД связан с мутацией в гене INSR. INSR - это ген, отвечающий за производство инсулинового рецептора. Этот рецептор является частью большого класса белков, пронизывающих клеточную мембрану и обладающих тирозинкиназной активностью, то есть способностью передавать сигналы внутрь клетки путём фосфорилирования тирозиновых остатков. В гене INSR идентифицировано порядка 130 патогенных мутаций, ассоциированных с развитием СД. Преобладающим типом являются миссенс-мутации, тогда как нонсенс-мутации, нарушения сплайсинга, а также делеции и инсерции встречаются значительно реже. СД наследуется по аутосомно-рецессивному типу наследования[2][3][4].
Патогенез
Патогенные варианты INSR нарушают синтез инсулиновых рецепторов, их транспорт к мембране, сродство к инсулину, тирозинкиназную активность или ускоряют деградацию рецептора. Это приводит к снижению внутриклеточной передачи инсулинового сигнала, что вызывает гипергликемию из-за нарушения регуляции поглощения и высвобождения глюкозы, а также синтеза углеводов, липидов и белков. Гипогликемия, наблюдаемая при этом синдроме связана с отсроченным действием инсулиноподобного фактора роста 1. Кроме того, инсулинорезистентность приводит к изменению экспрессии генов, контролирующих факторы роста и апоптоз, что усугубляет метаболические нарушения[3].
Эпидемиология
СД крайне редкое заболевание с предполагаемой распространенностью 1 случай на 4 миллиона детей, хотя реальная распространённость может быть выше[2].
Диагностика
Клиническая картина
Дети с СД демонстрируют выраженную задержку внутриутробного и постнатального роста. Внутриутробная задержка развития обычно становится очевидной начиная с 7-го месяца гестации. После рождения наблюдается тяжёлая гипотрофия с признаками истощения, несмотря на адекватное питание[2].
У пациентов также отмечается спленомегалия и гепатомегалия. В печени обнаруживается избыточное накопление гликогена и железа, а также явления холестаза. Часто наблюдаются увеличенные почки с признаками нефрокальциноза и атрофия надпочечников. Характерны гипоплазия лимфоидной ткани и кистозные изменения гонад[2].
Поражение сердца при СД обычно проявляется на 1-2 месяце жизни в виде выраженной гипертрофической кардиомиопатии. Развитие кардиомиопатии связывают с чрезмерной гиперинсулинемией[2].
При исследовании костной системы выявляется значительное отставание костного возраста, а патологическое исследование обнаруживает аномалии метафизов и эпифизов[2].
Лабораторная диагностика
Биохимический анализ крови: характерна резкая гиперинсулинемия с аномально повышенными концентрациями инсулина и С-пептида в крови, сопровождающаяся лабильным уровнем гликемии — типичны эпизоды гипогликемии при голодании и гипергликемии после еды[3].
Молекулярно-генетический анализ: выявляется мутация гена INSR методом секвенирования[3].
Инструментальная диагностика
По данным ультразвукового исследования определяется гипертрофическая кардиомиопатия, увеличенные почки, гепато- и спленомегалия, нефрокальциноз, увеличенные поликистозные яичники у девочек[3].
Дифференциальная диагностика
Дифференциальная диагностика СД проводится со следующими состояниями[3][4]:
- липоатрофический сахарный диабет;
- синдром Берардинелли — Сейпа;
- синдром Сильвера — Рассела;
- семейный гиперинсулинизм;
- резистентность к инсулиноподобному фактору роста 1.
Осложнения
К возможным осложнениям относятся[3]:
- кетоацидоз;
- ретинопатию;
- нефропатию;
- нейропатию.
Лечение
Единственным доступным методом лечения СД в настоящее время является терапия инсулиноподобным фактором роста-1. Основная цель лечения — предотвращение компенсаторной гиперинсулинемии, которая вызывает многие проявления синдрома, включая кардиомиопатию[2].
Прогноз
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Таранушенко Татьяна Евгеньевна, Киселёва Н. Г., Карпова Л. Н., Лазарева О. В., Калюжная И. И., Голубенко Н. К. Гипогликемии у новорождённых детей // Педиатрия. Журнал им. Г. Н. Сперанского. — 2018. — № 1.