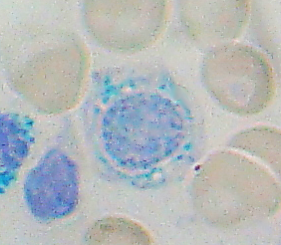
Сидеробластная анемия
Сидеробла́стная анеми́я (СА; сидероахрести́ческая анеми́я) — гетерогенная группа заболеваний, отличительной особенностью которых является нарушение утилизации железа эритрокариоцитами и его патологическое накопление в митохондриях с образованием кольцевых сидеробластов. Последние представляют собой эритрокариоциты с характерным кольцевым расположением гранул негемоглобинового железа вокруг ядра. Выделяют врождённые и приобретённые формы сидеробластных анемий. Прогноз для пациентов варьирует в зависимости от этиологии заболевания. При вторичных приобретённых формах прогноз в целом благоприятный после устранения причинного фактора. При X-сцепленной СА адекватная терапия пиридоксином и контроль перегрузки железом могут значительно улучшить прогноз. Однако при отсутствии своевременного и адекватного лечения прогноз может быть неблагоприятным[1][2].
Общие сведения
| Сидеробластная анемия | |
|---|---|
| МКБ-11 | 3A72.0 |
| МКБ-10 | D64.0 и D64.1 |
| МКБ-10-КМ | D64.0 и D64.1 |
| МКБ-9-КМ | 285.0 |
| OMIM | 301310 |
| DiseasesDB | 12110 |
| MeSH | D000756 |
История
В 1942 году Ханс Грюнеберг продемонстрировал наличие свободного железа в цитоплазме некоторых эритробластов (сидеробластов) и в зрелых эритроцитах (сидероцитах). В 1945 году Кули описал пациента с анемией, которая, вероятно, соответствовала несиндромальной форме X-сцепленной СА, поскольку позднее Коттер и коллеги идентифицировали мутации в гене ALAS2 и кольцевые сидеробласты. В 1956 году Бьёркман описал серию из четырёх пациентов с хронической рефрактерной к терапии анемией с многочисленными аномальными сидеробластами в костном мозге, у одного из которых впоследствии развился лейкоз. Как отдельный подтип анемии СА была признана в 1960-х годах. В течение последующих 30 лет, благодаря значительным достижениями в области молекулярной биологии, была установлена генетическая природа более двух третей случаев врождённых СА и значительной части случаев приобретённых клональных форм[3].
Классификация
СА подразделяются на врождённые и приобретённые формы. Приобретённые сидеробластные анемии охватывают широкий спектр этиологий — от клональных расстройств (таких как миелодиспластический синдром с кольцевыми сидеробластами и миелодиспластическое/миелопролиферативное новообразование с кольцевыми сидеробластами и тромбоцитозом) до токсических или метаболических форм заболевания[3].
Врождённые СА подразделяются на несиндромные и синдромные формы:
- к несиндромным расстройствам относятся X-сцепленная СА (4-го типа);
- синдромные заболевания включают X-сцепленную СА с атаксией, синдром Пирсона, тиамин-зависимую мегалобластную анемию, миопатию, лактатацидоз и СА, СА с иммунодефицитом, лихорадкой и задержкой развития, а также дефицит НАД-дегидрогеназы 1 бета субкомплекса (NDUFB11)[2].
Этиология
Этиология СА зависит от формы заболевания[1][2]:
- наследственные СА обусловлены мутациями в генах, участвующих в синтезе гема, биогенезе железосерных кластеров или митохондриальном метаболизме. Наиболее распространённой причиной является форма, вызываемая мутацией в гене ALAS2, кодирующем ключевой фермент синтеза гема. Для данной мутации характерна X-сцепленная доминантная форма наследования. Другие наследственные формы связаны с дефектами генов митохондриального транспортёра (SLC25A38), переносчика тиамина (SLC19A2), а также генов, кодирующих псевдоуридинсинтазу (PUS1), тирозил-тРНК синтетазу (YARS2) и компоненты митохондриальной ДНК. Для них характерен аутосомно-рецессивный тип наследования;
- приобретённые СА классифицируют на клональные и неклональные (вторичные) формы%
- неклональные СА возникают вследствие избыточного поступления железа в эритрокариоциты (при хроническом гемолизе или многократных гемотрансфузиях) либо нарушения синтеза гема, вызванного токсическими воздействиями (интоксикация свинцом, хронический алкоголизм), приёмом лекарственных препаратов (изониазид, пиразинамид, линезолид, азатиоприн, хлорамфеникол), алиментарными дефицитами (недостаток пиридоксина или меди, избыток цинка). Данная форма анемии также может сопровождать аутоиммунные и онкологические заболевания. Важной характеристикой неклональных СА является их потенциальная обратимость при устранении причинного фактора;
- клональные СА развиваются как проявление клональных нарушений кроветворения при миелодиспластических синдромах, миелодиспластических или миелопролиферативных новообразованиях, острых миелоидных лейкозах и апластической анемии. Клональные формы обычно возникают у лиц пожилого возраста, могут развиваться самостоятельно или как следствие предшествующей лучевой терапии или химиотерапии.
Патогенез
Патогенез синдромальных и несиндромальных форм первичной СА имеет свои особенности[2]:
- Несиндромные формы наследственных СА:
- СА 1-го типа: вызывается различными мутациями в гене ALAS2 (промоторные, миссенс- и нонсенс-мутации), наследуется по X-сцепленному типу. Мутация приводит к нарушению синтеза аминолевулиновой кислоты — ключевого предшественника гема. У женщин может проявляться из-за неравной инактивации X-хромосомы;
- СА 2-го типа: обусловлена мутациями в гене SLC25A38 (миссенс- и нонсенс-мутации). Этот ген кодирует митохондриальный переносчик глицина. Дефект белка нарушает транспорт глицина в митохондрии, что ограничивает образование аминолевулиновой кислоты и последующий синтез гема;
- СА 3-го типа: вызывается гомозиготной мутацией в гене GLRX5, нарушающей сплайсинг мРНК. Продукт экспрессии гена GLRX5 участвует в образовании железосерных кластеров в митохондриях. Снижение его функции приводит к дефициту гема;
- СА 4-го типа: обусловлена мутациями в гене HSPA9, кодирующем митохондриальный шаперонный белок. Отсутствие функционального белка ингибирует дифференцировку эритроидных клеток.
- Синдромные формы наследственных СА:
- X-сцепленная сидеробластная анемия с атаксией: вызывается миссенс-мутацией в гене ABCB7, участвующем в биогенезе железосерных кластеров и транспорте железа в цитозоль. Проявляется сочетанием анемии и мозжечковой атаксии;
- синдром Пирсона: обусловлен делециями митохондриальной ДНК, вызывающими дефекты дыхательной цепи митохондрий. Проявляется рефрактерной СА и экзокринной недостаточностью поджелудочной железы;
- тиамин-зависимая мегалобластная анемия: вызывается мутацией гена SLC19A2, нарушающей транспорт тиамина. Тиамин необходим для образования сукцинил-КоА. Характеризуется триадой: мегалобластная анемия, сахарный диабет и нейросенсорная тугоухость;
- миопатия, лактат-ацидоз и сидеробластная анемия: вызывается мутациями в генах PUS1 или YARS2. PUS1 участвует в модификации рибосомальной РНК, YARS2 кодирует митохондриальную тирозил-тРНК-синтетазу. Точный механизм развития анемии неизвестен;
- СА с иммунодефицитом: обусловлена мутацией гена TRNT1, кодирующего нуклеотидилтрансферазу. Мутации в гене, кодирующем этот фермент, приводят к нарушению созревания тРНК и митохондриальной дисфункции;
- дефицит NDUFB11: вызывается делецией трёх нуклеотидов в гене NDUFB11, приводящей к делеции фенилаланина в одноимённом белке. Проявляется нормоцитарной СА и лактат-ацидозом.
Патогенез клональной формы СА в основном связан с соматическими мутациями в гене SF3B1, который кодирует ключевой компонент сплайсосомы. Основным механизмом развития заболевания является нарушение сплайсинга генов, критически важных для метаболизма железа и синтеза гема. К ним относятся: ABCB7 (продукт экспрессии обеспечивает транспорт железа из митохондрий), ALAS2 (продукт экспрессии кодирует первый фермент синтеза гема), TMEM14C и SLC25A37 (продукты экспрессии участвуют в митохондриальном импорте железа). Снижение экспрессии ABCB7 нарушает выведение железа из митохондрий, а дисрегуляция аминолевулинатсинтазы и других генов приводит к дефекту синтеза гема. Это вызывает накопление железа в митохондриях и формирование кольцевых сидеробластов. Комбинированное воздействие на множество белков объясняет тяжесть нарушения эритропоэза. Реже патогенез может быть связан с мутациями в других генах сплайсинга (PRPF8, SRSF2, ZRSR2) или хромосомными аберрациями[3].
Во всех случаях патогенез вторичных приобретённых форма СА происходит прямое или опосредованное нарушение функции митохондрий и ключевых ферментов синтеза гема, что приводит к неиспользованию железа и его патологическому накоплению в митохондриях эритрокариоцитов[3]:
- алкогольная интоксикация: этанол и его метаболит ацетальдегид оказывают прямое токсическое действие на фермент аминолевулинатсинтазу, ключевой для синтеза гема. Это вызывает дисбаланс между импортом железа в митохондрии и недостаточным производством протопорфирина IX, что приводит к накоплению железа в митохондриях;
- лекарственно-индуцированные формы:
- изониазид, пиразинамид: нарушают метаболизм витамина B6, приводя к дефициту синтеза гема;
- хлорамфеникол: подавляет активность аминолевулинатсинтазы и феррохелатазы, что нарушает синтез митохондриальных белков и окислительный метаболизм;
- линезолид: связывается с митохондриальными рибосомами, ингибируя синтез белков и вызывая прямую митохондриальную токсичность;
- дефицит меди: медь является кофактором церулоплазмина и цитохром-с-оксидазы. Дефицит нарушает восстановление трёхвалентного железа и его включение в гем, а также транспорт железа трансферрином;
- дефицит пиридоксина (витамина B6): пиридоксаль-5-фосфат является кофактором аминолевулинатсинтазы. Его недостаток блокирует первую реакцию синтеза гема — образование аминолевулиновой кислоты;
- отравление свинцом: свинец ингибирует множество ферментов синтеза гема: аминолевулинатдегидратазу, копропорфириногеноксидазу и феррохелатазу, что приводит к нарушению образования гема и накоплению промежуточных продуктов порфиринового обмена;
- гипотермия: низкая температура нарушает митохондриальный метаболизм и окислительное фосфорилирование, что вторично вызывает дисфункцию синтеза гема и накопление железа в митохондриях.
Эпидемиология
СА относится к категории орфанных заболеваний, поражающих менее 200 000 человек. Из-за низкой распространённости точные статистические эпидемиологические данные отсутствуют. Заболевание может развиваться в любом возрасте — от младенцев с врождёнными формами до лиц среднего и пожилого возраста[4].
Диагностика
Клиническая картина СА включает общие симптомы анемии: слабость, недомогание, одышку, сердцебиение и головную боль. При осмотре могут выявляться бледность кожных покровов и конъюнктив, тахикардия. У некоторых пациентов наблюдается бронзовый оттенок кожи из-за перегрузки железом. В тяжёлых хронических случаях или при ассоциации с миелодиспластическим синдромом может присутствовать умеренная гепатоспленомегалия из-за экстрамедуллярного кроветворения[2].
Пациенты с синдромальными наследственными формами могут иметь сопутствующие проявления, такие как декомпенсированный сахарный диабет и нейросенсорная тугоухость. Наследственные формы обычно выявляются у молодых пациентов с отягощённым семейным анамнезом, в то время как приобретённые формы чаще встречаются у пожилых пациентов и могут быть ассоциированы с миелодиспластическим синдромом[2].
- Клинический анализ крови: характерно выявление микроцитарной анемии при врождённых формах и нормо- и макроцитарной анемии при приобретённых форма СА[2].
- Микроскопическое исследование мазка периферической крови: сидероциты считаются характерным признаком СА. Эти гипохромные эритроциты содержат выраженные грубые базофильные гранулы, видимые при окраске по Райту — Гимзе. Гранулы представляют собой остатки митохондрий, перегруженных железом, и известны как тельца Паппенгеймера. Сидероциты являются зрелыми эритроцитарными аналогами кольцевых сидеробластов, наблюдаемых в костном мозге[2].
- Цитологическое исследование мазка костного мозга: окрашивание костного мозга берлинской лазурью (реакция Перлса) выявляет характерные кольцевые сидеробласты, которые должны иметь не менее пяти гранул, окружающих как минимум треть ядерной мембраны. Гранулопоэз часто характеризуется сдвигом влево, но при этом сохраняется полное созревание клеток. Костный мозг обычно демонстрирует многочисленные макрофаги, нагруженные железом, которые плохо визуализируются в мазке. Дизэритропоэтические изменения, включая сдвиг влево эритроидных предшественников, мегалобластоидные изменения и двуядерность, часто наблюдаются при миелодиспластических вариантах, но менее характерно для других типов СА. Вакуолизация эритроидных и миелоидных предшественников обычно встречается при дефиците меди, где также может отмечаться гиперплазия лимфоидных клеток-предшественников[1][2].
- Цитохимическое исследование мазка костного мозга: отложения негемоглобинового железа в эритрокариоцитах представлены в виде гранул синего цвета. Аналогичные гранулы выявляются также в эритроцитах и макрофагах[1].
- Молекулярно-генетический анализ: при клональном характере СА характерно выявление мутации в гене SF3B1 методом полимеразной цепной реакции[2].
Дифференциальная диагностика
Дифференциальный диагноз СА включает следующие заболевания[2]:
- железодефицитная анемия;
- талассемия;
- анемия хронического заболевания;
- отравление свинцом;
- постгеморрагическая анемия.
Осложнения
Наследственные формы СА, обусловленные мутациями в генах XLSA, GLRX5 и SLC25A38, вызывают системную перегрузку железом. Железо накапливается преимущественно в печени, что со временем может приводить к развитию фиброза и цирроза, аналогично наследственному гемохроматозу. В редких случаях при длительном и выраженном накоплении железа у пациентов могут развиваться гепатомегалия, кардиомиопатия и эндокринные нарушения[2].
Приобретённые формы СА, ассоциированные с миелопролиферативными заболеваниями, характеризуются тяжёлой анемией, вызывающей слабость, утомляемость и снижение толерантности к физической нагрузке. Лейкопения предрасполагает к частым инфекционным осложнениям, а тромбоцитопения проявляется повышенной кровоточивостью и образованием гематом. Наиболее серьёзным осложнением является повышенный риск трансформации в острый миелоидный лейкоз. Для этой группы заболеваний также характерны высокая частота тромбоэмболических осложнений[2].
Лечение
Лечение СА зависит от её типа и тяжести. При X-сцепленной форме назначают пиридоксин, что может частично или полностью корригировать анемию. При тиамин-зависимой форме применяют тиамин. Для коррекции неэффективного эритропоэза при врождённых формах может использоваться активатор созревания клеток-предшественников эритроцитов[2].
При тяжёлой анемии, рефрактерной к терапии, показана гемотрансфузия. Для профилактики и лечения перегрузки железом назначают хелаторную терапию при значительном повышении концентрации ферритина. Пациентам с нормализованной концентрацией гемоглобина после терапии пиридоксином может проводиться кровопускание для устранения избытка железа. Адекватный контроль перегрузки железом улучшает ответ на пиридоксин и общие результаты лечения[2].
Лечение миелодиспластического синдрома с СА включает поддерживающую и патогенетическую терапию. К методам поддерживающего лечения относятся гемотрансфузии эритроцитов и тромбоцитов, применение стимуляторов эритропоэза, иммуномодулирующих препаратов (леналидомид), регуляторов суперсемейства трансформирующего фактора роста бета (сотатерцепт, луспатерцепт) и хелаторной терапии при перегрузке железом[3].
Патогенетическая терапия предусматривает использование гипометилирующих агентов (азацитидин, децитабин) ингибиторов теломеразы (иметелстат), а также препаратов, нацеленных на модуляцию сплайсинга, которые проходят клинические испытания[3].
Единственным потенциально радикальным методом лечения остаётся аллогенная трансплантация гемопоэтических стволовых клеток, однако процедура сопряжена с высоким риском летальности в зависимости от индивидуальных факторов риска[3].
Прогноз
Прогноз при СА вариабелен и зависит от этиологии заболевания. При вторичных приобретённых формах прогноз в целом благоприятный после устранения причинного фактора — отмены лекарственных препаратов или прекращения воздействия токсинов. При X-сцепленной СА адекватная терапия пиридоксином и контроль перегрузки железом могут значительно улучшить прогноз. Однако при отсутствии своевременного и адекватного лечения прогноз может быть неблагоприятным[2].
Прогноз при приобретённых формах, ассоциированных с миелодиспластическими/миелопролиферативными заболеваниями, зависит от подлежащих генетических и клинических характеристик. Эта форма СА обычно встречается у пожилых пациентов и часто ассоциирована с мутацией гена SF3B1, что связано с относительно благоприятным прогнозом. Однако на исход заболевания влияют наличие сопутствующих мутаций и риск трансформации в острый миелоидный лейкоз. Общая выживаемость пациентов определяется уровнем бластов в костном мозге и ответом на проводимую терапию[2].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Двирнык В. Н., Кохно А. В., Чулкова А. А., Наумова И. Н., Лазарева О. В., Паровичникова Е. Н. Цитологическая и цитохимическая диагностика сидеробластных анемий // Гематология и трансфузиология : Journal Article. — 2024. — Т. 69, № 1. — С. 80—88. — ISSN 0234-5730. — doi:10.35754/0234-5730-2024-69-1-80-88.
- Rodriguez-Sevilla J.J., Calvo X., Arenillas L. Causes and Pathophysiology of Acquired Sideroblastic Anemia (англ.) // Genes : Journal Article; Review. — 2022. — 30 August (vol. 13, no. 9). — P. 1562. — ISSN 2073-4425. — doi:10.3390/genes13091562.
- D. Ashorobi, A. Kaur, A.Chhabra. Sideroblastic Anemia (англ.). Statpearls (11 декабря 2024). Дата обращения: 21 сентября 2025.