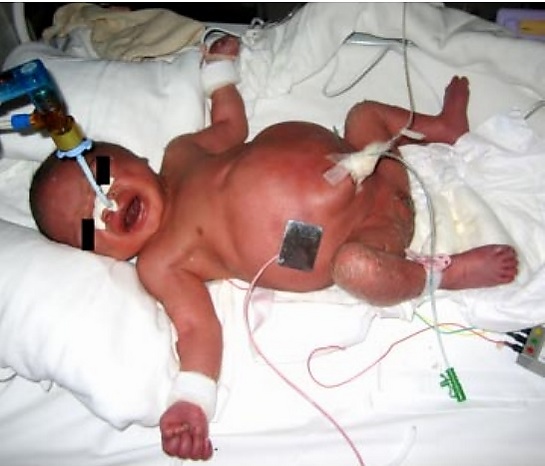
Синдром Перлмана
Синдро́м Пе́рлмана (СП) — это редкое аутосомно-рецессивное заболевание, вызванное герминальными мутациями в гене DIS3L2. Для этого синдрома характерна врождённая гипертрофия, мышечная гипотония, увеличение внутренних органов и специфические лицевые аномалии: V-образная верхняя губа, выступающий лоб, глубоко посаженные глаза, широкая и плоская переносица, а также низко расположенные уши. Кроме того, у пациентов могут встречаться почечные аномалии, такие как нефромегалия и гидронефроз, а также задержка психомоторного развития[1].
История
Первые шесть пациентов с этим СП родились в близкородственном браке в йеменской еврейской семье. Морфологические особенности почек у этих больных были описаны ещё в 1970 году, а клиническая характеристика синдрома была представлена Перлманом и его коллегами в 1973 и 1975 годах. Позже, в 1984 году, Нери и соавторы более детально описали проявления синдрома у двух поражённых сиблингов и предложили название «синдром Перлмана». В последующие годы дополнительные случаи заболевания были зарегистрированы различными исследователями[2].
Этиология
СП вызывается биаллельными (гомозиготными или компаунд-гетерозиготными) мутациями в гене DIS3L2, расположенном в хромосомной области 2q37. Ген DIS3L2 кодирует ключевой компонент экзосомного комплекса, который участвует в процессинге и деградации РНК, что играет важную роль в регуляции клеточных процессов.
Патогенез
Продукт экспрессии гена DIS3L2 кодирует ключевой компонент экзосомного комплекса, участвующий в процессинге и деградации РНК. Он обладает экзорибонуклеазной активностью, регулируя стабильность и метаболизм РНК. Мутации в гене DIS3L2 приводят к потере этой активности, что нарушает контроль над клеточным циклом и пролиферацией. В частности, дисфункция DIS3L2 вызывает[3]:
- аномалии митоза — нарушение расхождения хроматид, что связано с накоплением аномальных транскриптов;
- нарушение обмена РНК — дисрегуляция деградации мРНК, включая те, что участвуют в контроле роста и клеточного деления;
- опухолевую предрасположенность — особенно к нефробластоме, что согласуется с данными о соматических делециях 2q37.1 в спорадических опухолях Вильмса.
Эпидемиология
Всего по данным литературы описано около 30 случаев СП.
Диагностика
Клиническая картина
При СП дети обычно рождаются с большой массой тела, значительной длиной тела и макроцефалией. Характерные черты лица включают выступающий лоб, широкую уплощённую переносицу, глубоко посаженные глаза, V-образную вывернутую верхнюю губу и низко расположенные уши. Более чем у 75 % больных отмечаются мышечная гипотония, увеличение почек и печени, приводящее к выпячиванию живота, а у мальчиков — крипторхизм. У части пациентов встречаются колоколообразная грудная клетка (из-за вторичной лёгочной гипоплазии), гиперинсулинизм, судороги, аномалии развития мозга (гипоплазия мозолистого тела, церебральная атрофия, гетеротопии серого вещества), пороки сердца (перерыв дуги аорты, аномальное отхождение левой коронарной артерии) и желудочно-кишечные аномалии (заворот кишок, атрезия подвздошной кишки).
Почти у всех пациентов наблюдается задержка развития разной степени выраженности, включая моторные и речевые нарушения, интеллектуальную недостаточность и поведенческие расстройства — описан лишь один случай девочки 9 лет с сохранными когнитивными функциями.
Среди выживших младенцев примерно у двух третей развивается опухоль Вильмса в среднем возрасте 19 месяцев, причём в 55 % случаев она бывает двусторонней. Частыми гистологическими особенностями при синдроме Перлмана являются нефробластоматоз (предшественник опухоли Вильмса) и гиперплазия островковых клеток поджелудочной железы, приводящая к гиперинсулинизму.
Лабораторная диагностика
Молекулярно-генетический анализ: выявление мутации в гене DIS3L2 методом секвенирования.
Пренатальная диагностика
Пренатальная диагностика СП: более чем у половины поражённых плодов во время беременности по данным ультразвукового исследования выявляются многоводие, макросомия, нефромегалия с гидронефрозом и асцит.
Дифференциальная диагностика
Дифференциальная диагностика СП проводится со следующими состояниями[1]:
- синдром Беквита — Видемана;
- синдром Симпсона — Голаби — Бемель;
- изолированная гемигипертрофия.
Лечение
Лечение СП требует мультидисциплинарного подхода и включает симптоматическую терапию проявлений заболевания. После рождения необходимо незамедлительно корректировать гипогликемию, респираторный дистресс -синдром и почечную недостаточность. Пороки развития органов следует лечить в соответствии со стандартными рекомендациями.
Прогноз
Прогноз при СП неблагоприятный и характеризуется высокой неонатальной смертностью. Большинство поражённых младенцев развивают респираторный дистресс с рефрактерной гипоксемией и почечную недостаточность, умирая в первые часы или дни жизни. Лишь немногим пациентам удаётся пережить неонатальный период. Большая часть из них погибает в течение первого года жизни от сепсиса или прогрессирующей дыхательной недостаточности. Описано всего пять пациентов, переживших первый год жизни, у всех отмечалась задержка развития различной степени выраженности[2].
Диспансерное наблюдение
Хотя специальный протокол скрининга опухолей для данного заболевания не разработан, целесообразно проводить ультразвуковое исследование органов брюшной полости каждые три месяца от рождения до 7-летнего возраста для раннего выявления опухоли Вильмса. На основании индивидуальных потребностей пациента необходимо обеспечить регулярную оценку нервно-психического развития и раннюю коррекционную поддержку.
Примечания
Литература
- Казакова Лилия Леонидовна. Билатеральная нефробластома у детей. Описание клинического случая // Российский журнал детской гематологии и онкологии. — 2018. — № 2.
- Soma, N.; Higashimoto, K.; Imamura, M.; Saitoh, A.; Soejima, H.; Nagasaki, K. Long term survival of a patient with Perlman syndrome due to novel compound heterozygous missense mutations in RNB domain of DIS3L2 (англ.) // American Journal of Medical Genetics Part A : Journal article. — 2017. — April (vol. 173, no. 4). — P. 1077–1081. — ISSN 1552-4825. — doi:10.1002/ajmg.a.38111.