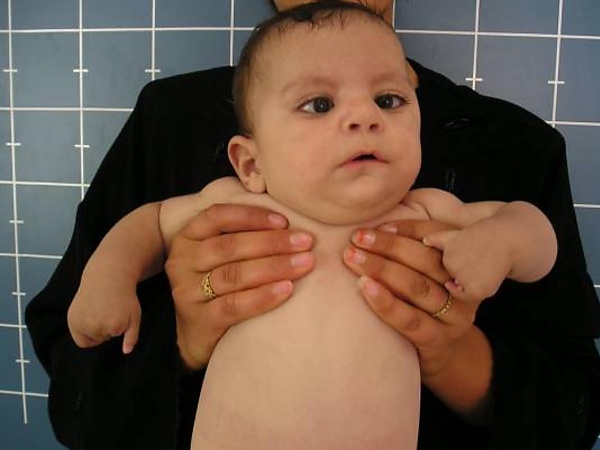
Синдром Мёбиуса
Синдро́м Мёбиуса (врождённая лицевая диплегия) — редкая врождённая аномалия, для которой характерно отсутствие мимики лица. Патология характеризуется параличом лицевого нерва, имеет аутосомно-доминантное, аутосомно-рецессивное и X-сцепленное наследованиепри этом большинство случаев возникает спорадически без семейного анамнеза[2][3]. Основными клиническими проявлениями являются ограничение подвижности глазных яблок, косоглазие, а также разнообразные неврологические и ортопедические нарушения, включая аномалии развития конечностей и опорно-двигательного аппарата, трудности с глотанием и речью, и поражения мимической мускулатуры[4].
Синдром назван в честь Пауля Юлия Мёбиуса — немецкого невролога, который впервые описал синдром в 1888 году[5].
Диагностика синдрома Мёбиуса основывается на клиническом обследовании с оценкой движения лицевых мышц и глаз, а также на инструментальных исследованиях: магнитно-резонансной томографии и компьютерной томографии головного мозга для выявления гипоплазии ствола мозга и ядер лицевых и отводящих нервов. Электромиография может использоваться для дифференциации врождённого паралича лицевого нерва и повреждений, вызванных родовой травмой[4]. Лечение носит симптоматический и поддерживающий характер и включает хирургические методы коррекции лицевого паралича, глазных и ортопедических аномалий, физиотерапию, логопедическую и психомоторную реабилитацию. Психологическая поддержка играет важную роль для адаптации пациентов и их семей, учитывая ограничения мимической активности и социальные трудности[4].
Прогноз зависит от степени поражения ствола головного мозга и тяжести осложнений. Заболевание не прогрессирует, при лёгких формах продолжительность жизни обычно нормальная[4].
Общие сведения
История
Синдром Мёбиуса впервые был описан немецким офтальмологом Альфредом фон Грефе в 1880 году. Позднее, в 1888 году, немецкий невропатолог Пауль Юлиус Мёбиус подробно охарактеризовал клинические особенности данного состояния, вследствие чего синдром получил его имя[5].
В 1994 году был создан Фонд синдрома Мёбиуса, направленный на изучение, поддержку пациентов и повышение осведомлённости о заболевании. В том же году в Лос-Анджелес состоялась первая конференция, посвящённая синдрому Мёбиуса[6].
Классификация
В 1979 году Тоуфиги и соавторы предложили патоморфологическую классификацию синдрома Мёбиуса, основанную на выявляемых при обследовании пациентов структурных изменениях. Было выделено четыре группы[4]:
- I группа — простая гипоплазия или атрофия ядер черепных нервов;
- II группа — первичные поражения периферических нервов;
- III группа — очаговый некроз в ядрах ствола головного мозга;
- IV группа — первичная миопатия без поражения центральной нервной системы или периферических нервов.
Этиология
Этиология синдрома Мёбиуса остаётся до конца не установленной. Заболевание как мультифакторное, возникающее в результате сочетанного влияния генетических и экзогенных факторов[2][3].
В подавляющем большинстве случаев синдром Мёбиуса носит спорадический характер и развивается у пациентов без семейного анамнеза. Однако описаны семейные случаи, предполагающие возможность различных типов наследования (аутосомно-доминантного, аутосомно-рецессивного и Х-сцепленного), что указывает на генетическую гетерогенность заболевания[2][3]. При этом единый ген, ответственный за развитие синдрома, не установлен. В отдельных исследованиях выявлялись мутации de novo в генах PLXND1 (3q21.3) и REV3L (6q22), а также хромосомные перестройки (в частности, с участием 1-й, 3-й, 10-й и 13-й хромосом), однако их роль остаётся окончательно не доказанной[4][7].
Среди экзогенных факторов значительное внимание уделяется воздействию тератогенов. Описана связь синдрома Мёбиуса с пренатальным воздействием лекарственных препаратов, обладающих сосудосуживающим или эмбриотоксическим эффектом, включая мизопростол и талидомид, а также с употреблением матерью наркотических веществ (например, кокаина). Предполагается, что такие воздействия могут нарушать нормальное кровоснабжение развивающегося эмбриона[4][7].
Одной из наиболее обоснованных гипотез считается сосудистая теория, согласно которой ключевую роль играет транзиторное нарушение кровотока в системе артерий, кровоснабжающих ствол головного мозга плода (в частности, в бассейне базилярной или подключичной артерий). Такое нарушение может быть обусловлено как внешними воздействиями, так и врождёнными ромбенцефальным. аномалиями развития[4][2].
Также рассматриваются гипоксически-ишемические повреждения центральной нервной системы плода в критические периоды эмбриогенеза (примерно на 4—7-й неделе гестации), токсическое воздействие на плод и нарушения раннего морфогенеза ствола головного мозга[4][7].
Патогенез
Патогенез синдрома Мёбиуса связан с нарушением развития структур ствола головного мозга и черепных нервов, преимущественно отводящего (VI) и лицевого (VII), что определяет основные клинические проявления заболевания. Ключевым морфологическим субстратом считается аплазия или гипоплазия ядер черепных нервов в области моста и продолговатого мозга. Наиболее часто поражаются отводящий и лицевой нервы, однако патологический процесс может распространяться и на другие черепные нервы (преддверно-улитковый, языкоглоточный, блуждающий, подъязычный), реже — глазодвигательный и блоковый нервы. При этом лицевой нерв вовлекается практически во всех случаях, а отводящий — в большинстве наблюдений[3][8].
Выделяют несколько возможных механизмов поражения[4]:
- аплазия или гипоплазия ядер черепных нервов;
- дегенерация или некроз нейронов ствола головного мозга;
- поражение периферических отделов черепных нервов;
- первичное поражение мышечной ткани (миопатический вариант).
Наиболее распространённой считается теория, согласно которой первичным является ишемическое или гипоксическое повреждение ствола головного мозга плода на ранних этапах развития. Нарушение кровоснабжения приводит к гибели или недоразвитию нейронов двигательных ядер, что в дальнейшем вызывает стойкий дефицит иннервации соответствующих мышц[4].
Альтернативные теории включают[4]:
- врождённую гипоплазию или агенезию ядер черепных нервов генетической природы;
- мезодермальную дисплазию с первичным поражением мышц, происходящих из первой и второй жаберных дуг, при вторичном вовлечении нервной системы;
- комбинированные механизмы с одновременным поражением нервной и мышечной тканей.
С эмбриологической точки зрения важную роль играет тесная связь развития ядер отводящего и лицевого пар черепных нервов, что объясняет их одновременное поражение. Нарушение морфогенеза в критический период формирования этих структур приводит к формированию типичной клинической картины[4].
Наряду с поражением черепных нервов, у части пациентов наблюдаются аномалии конечностей (например, гиподактилия, синдактилия), что указывает на более широкий дефект эмбрионального развития. Это подтверждает гипотезу о нарушении развития в определённый временной промежуток эмбриогенеза, затрагивающем как краниальные, так и соматические структуры[3].
Клинически итогом данных патологических процессов является формирование стойкой недостаточности нервно-мышечной передачи в поражённых областях, что проявляется врождённым параличом мимической мускулатуры, нарушением движений глаз, а также расстройствами речи, жевания и глотания различной степени выраженности[3].
При гистологическом исследовании наиболее выраженные патологические изменения обнаруживаются в области двигательных ядер черепных нервов центральной нервной системы, преимущественно ядер отводящего, лицевого и подъязычного нервов, в меньшей степени — глазодвигательного и добавочного нервов. Наиболее значительные изменения отмечаются в ядре отводящего нерва, где описывается почти полная утрата нейронов. В поражённых участках могут выявляться очаги некроза, которые имеют округлую форму, чёткие границы и базофильную окраску. Вокруг некротических зон определяются реактивные изменения, включая глиоз, а также разрастание клеточных отростков. По периферии очагов могут обнаруживаться аксональные сфероиды, свидетельствующие о дегенеративных процессах в нервной ткани. В некоторых случаях отмечается недоразвитие проводящих путей, в частности пирамид. Изменения затрагивают и периферические ткани: в лицевых мышцах выявляется атрофия с замещением мышечной ткани жировой и фиброзной тканью, что связано с нарушением иннервации[4].
Эпидемиология
Распространённость синдрома Мёбиуса составляет примерно от 2 до 20 случаев на 1 миллион новорождённых. Синдром Мёбиуса встречается одинаково во всех популяциях. Заболевание встречается у представителей всех этнических групп. Нет гендерных предубеждений; мужчины и женщины страдают в равной степени[5].
Диагностика
Диагноз устанавливается на основании данных анамнеза, клинического осмотра, применения инструментальных методов обследования[9].
Клиническая картина синдрома Мёбиуса характеризуется выраженной полиморфностью, однако ведущими проявлениями являются врождённый паралич лицевого нерва и нарушение отведения глаз, обусловленные поражением лицевого и отводящего черепных нервов[5]. Заболевание носит непрогрессирующий характер и проявляется с рождения[7].
Ведущим проявлением является так называемое «маскообразное» лицо. У пациентов отсутствует мимическая активность: они не могут улыбаться, хмуриться, поднимать брови, выражать эмоции при помощи лицевых мышц. Лицо выглядит амимичным, сглажены носогубные складки, углы рта опущены, рот часто остаётся полуоткрытым[3][9]. Паралич может быть двусторонним, что наблюдается чаще всего, либо односторонним или асимметричным. В ряде случаев сохраняется частичная подвижность отдельных групп мышц, однако полноценная мимика отсутствует[7].
Поражение отводящего нерва приводит к ограничению или полному отсутствию горизонтальных движений глазных яблок. Вследствие этого пациенты не могут отводить глаза кнаружи и вынуждены компенсаторно поворачивать голову для фиксации взгляда и слежения за движущимися объектами[3][8]. Часто развивается косоглазие, преимущественно сходящееся, хотя возможны и другие варианты нарушения положения глаз, возможно псевдокосоглазие. Зрительный контакт затруднён, что имеет важное значение для социальной коммуникации. Дополнительное поражение глазодвигательного и блокового нервов может приводить к более сложным нарушениям движений глаз, включая офтальмоплегию и птоз. Также могут наблюдаться эктропион, эпифора[7][9].
Вследствие пареза круговой мышцы глаза формируется лагофтальм — неполное смыкание век. Это состояние сопровождается повышенной сухостью роговицы, её раздражением, риском развития экспозиционной кератопатии, а также слезотечением, обусловленным нарушением прилегания нижнего века к глазному яблоку. У ряда пациентов наблюдается повышенная чувствительность глаз к внешним раздражителям[7][9].
Помимо лицевого и отводящего нервов, в патологический процесс могут вовлекаться и другие черепные нервы. Поражение тройничного нерва может сопровождаться нарушением чувствительности лица и снижением жевательной функции. Вовлечение преддверно-улиткового нерва приводит к снижению слуха или глухоте. Поражение языкоглоточного и блуждающего нервов обусловливает выраженные нарушения глотания и фонации, а вовлечение подъязычного нерва — ограничение подвижности языка и его гипоплазию[4][9].
Уже в раннем неонатальном периоде у детей выявляются трудности с кормлением. Нарушение сосания, жевания и глотания связано с недостаточностью иннервации соответствующих мышц, что приводит к поперхиванию, повышенному слюноотделению и риску аспирации пищи[9]. В тяжёлых случаях возможны эпизоды дыхательных нарушений[2]. По мере роста ребёнка проблемы с питанием могут частично компенсироваться, однако сохраняются нарушения глотания различной степени выраженности[9].
Речевые нарушения являются частым и значимым компонентом клинической картины. Они обусловлены сочетанием факторов: параличом мимической мускулатуры, гипоплазией и ограниченной подвижностью языка, а также аномалиями нёба и челюстей. Речь у таких пациентов может быть нечленораздельной, смазанной, труднопонимаемой, нередко отмечается задержка речевого развития[3][9]. При проведении логопедической коррекции многие пациенты способны значительно у. учшить разборчивость речи[10].
Черепно-лицевые аномалии встречаются у значительной части пациентов. Наиболее типичны микрогнатия (уменьшение размеров нижней челюсти), микростомия (малый размер ротовой щели), гипоплазия языка и различные его аномалии. Нёбо может быть высоким, готическим или расщеплённым, что дополнительно усугубляет нарушения питания и речи. Часто выявляются стоматологические аномалии, включая отсутствие отдельных зубов и неправильный прикус. Также могут наблюдаться эпикантус, низко расположенные или деформированные ушные раковины[3][9].
Помимо черепно-лицевых изменений, для синдрома Мёбиуса характерны аномалии опорно-двигательного аппарата. У пациентов часто выявляются врождённые деформации конечностей, например, косолапость, синдактилия, брахидактилия или редукция пальцев[3][7]. Возможны также сколиоз, дисплазия тазобедренных суставов и артрогрипоз. В ряде случаев синдром Мёбиуса сочетается с синдромом Поланда, для которого характерны гипоплазия большой грудной мышцы и аномалии верхней конечности, что отражает более широкий дефект эмбрионального развития[2][9].
Неврологические проявления включают мышечную гипотонию и задержку моторного развития. Дети могут позже осваивать навыки сидения, ползания и ходьбы, однако в большинстве случаев со временем догоняют сверстников[5][3]. Возможны также сопутствующие соматические нарушения, включая врождённые пороки сердца и расстройства сна[5].
Когнитивное развитие у большинства пациентов остаётся в пределах нормы. Тем не менее у части больных отмечается задержка психического развития различной степени выраженности, которая, по данным различных авторов, может встречаться в 10—40 % случаев, особенно при наличии сопутствующих аномалий[8].
Особое значение имеют поведенческие и социальные аспекты заболевания. Из-за отсутствия мимики и ограниченной подвижности глаз пациенты испытывают трудности в установлении зрительного контакта и выражении эмоций, что может приводить к ошибочной интерпретации их поведения окружающими[11]. Несмотря на это, многие пациенты успешно адаптируются, компенсируя недостаток мимической экспрессии использованием. жестов, позы и интонации[12].
Некоторые исследования показали, что у детей с синдромом Мёбиуса чаще, чем у здоровых детей, наблюдаются признаки расстройств аутистического спектра — группы состояний, характеризующихся нарушениями коммуникации и социального взаимодействия. Однако недавние исследования поставили эту связь под сомнение. Поскольку людям с синдромом Мёбиуса из-за их физических особенностей сложно поддерживать зрительный контакт и говорить, у них бывает трудно диагностировать расстройства аутистического спектра[3].
К. Белл и соавторы провели систематический обзор литературы, в результате которого была собрана серия сложных случаев из 449 человек с синдромом Мёбиуса, где они представили доказательства для двух групп синдрома Мёбиуса[2]:
- Тип 1: проявляются микрогнатия, аномалии конечностей и трудности при кормлении/глотании, которые, как правило, возникают вместе.
- Тип 2: фенотипически разнообразен, но больше связан с рентгенологически выявляемыми неврологическими аномалиями и задержкой развития.
Специфические лабораторные методы диагностики синдрома Мёбиуса отсутствуют. Может проводиться молекулярно-генетическое исследование с целью выявления возможных мутаций в генах PLXND1 и REV3L, однако они выявляются лишь у небольшой доли пациентов и не являются специфическими для синдрома Мёбиуса. Также может применяться гистологическое исследование[4].
Инструментальная диагностика играет ключевую роль в выявлении морфологических изменений центральной нервной системы и сопутствующих аномалий развития. Основными методами являются нейровизуализация и лучевые методы исследования.
Магнитно-резонансная томография головного мозга является наиболее информативным методом и позволяет выявить характерные изменения ствола мозга. При магнитно-резонансной томографии могут определяться гипоплазия моста и продолговатого мозга, уплощение дна четвёртого желудочка, недоразвитие лицевых холмиков и подъязычного выступа, а также гипоплазия мозжечка. В ряде случаев визуализируется отсутствие или выраженная гипоплазия лицевого и отводящего нервов. Также описаны кальцинаты в области ядер отводящего нерва и базальных ганглиев, однако эти изменения не являются специфичными[4][2].
Компьютерная томография может использоваться для выявления кальцинатов и грубых структурных аномалий головного мозга, однако уступает магнитно-резонансной томографии по информативности в оценке мягкотканных структур. Рентгенография применяется преимущественно для диагностики сопутствующих аномалий костной системы, включая деформации конечностей, грудной клетки и позвоночника[4].
Пренатальная и постнатальная ультразвуковая диагностика может выявлять косвенные признаки заболевания, включая кальцинаты в области ствола головного мозга и базальных ганглиев, однако чувствительность и специфичность ограничены[4].
Важное значение в дифференциальной диагностике имеет электромиография, позволяющая оценить состояние нервно-мышечной передачи и отличить врождённое поражение при синдроме Мёбиуса от приобретённых или травматических повреждений лицевого нерва. При врождённой аплазии или гипоплазии нервов признаки активной денервации, как правило, отсутствуют, что позволяет отличить заболевание от перинатальной травмы[4].
Дифференциальная диагностика
Дифференциальная диагностика синдрома Мёбиуса проводится со следующими заболеваниями:
- паралич отводящего нерва;
- синдром Дуэйна;
- синдром Каллмана;
- метаболическая невропатия;
- синдром Клиппеля — Фейля;
- тромбоз базилярной артерии;
- глиома ствола головного мозга;
- врождённые мышечные дистрофии;
- врождённые миопатии;
- метаболические миопатии;
- спинальная мышечная атрофия;
- токсическая полинейропатия;
- травматические поражения периферической нервной системы;
- синдром Поланда[4];
- детский церебральный паралич;
- паралич Белла;
- велокардиофациальный синдром;
- синдром Ди Джорджи;
- синдром Ханхарта[13];
- синдром Кэри — Файнмана — Зитера;
- оро-мандибулярно-конечностной синдром гипогенезии;
- глоссопалатинный анкилоз[7].
Осложнения
Могут наблюдаться следующие осложнения: нарушения мимической активности и речи, патология опорно-двигательного аппарата и ортопедические деформации, трудности при глотании и приёме пищи, расстройства зрительного восприятия, хронический конъюнктивит, аспирационная пневмония, изъязвления и эрозии роговицы, дисфункция дыхательных путей, осложнения среднего отита при аномалиях уха, а также повышенный риск инфекций и психологических трудностей, связанных с социальной адаптацией[4].
Лечение
Специфического лечения синдрома Мёбиуса не существует, так как заболевание является врождённым. Терапия носит поддерживающий и симптоматический характер[9].
Основное внимание уделяется коррекции функциональных нарушений и улучшению качества жизни пациентов. Офтальмологические осложнения, связанные с неполным смыканием век, включая кератит и конъюнктивит, требуют своевременного лечения для предотвращения повреждения роговицы. В ряде случаев применяются хирургические методы, например имплантация утяжеляющих конструкций в верхнее веко для улучшения его закрытия[4].
Нарушения глотания и кормления, особенно в раннем возрасте, могут требовать специализированной нутритивной поддержки, включая использование гастростомии при выраженной дисфагии. При риске аспирации необходим контроль питания и участие диетолога. У пациентов с выраженными нарушениями дыхательных путей в отдельных случаях может потребоваться трахеостомия[4].
Хирургическое лечение носит преимущественно симптоматический и реконструктивный характер и направлено на коррекцию аномалий и улучшение функций. Одним из наиболее современных методов является микронейрососудистая трансплантация свободной мышечной ткани, применяемая для восстановления мимической активности при параличе лицевого нерва. Также используются различные методы реиннервации лица с применением донорских нервов, включая добавочный нерв или ветви тройничного нерва. Перенос тонкой мышцы с иннервацией жевательного нерва рассматривается как один из эффективных подходов при двустороннем поражении. Лучшие результаты хирургического восстановления достигаются при выполнении вмешательства в раннем детском возрасте[4][7].
Коррекция сопутствующих ортопедических и краниофациальных аномалий, включая косолапость, синдактилию, деформации конечностей и челюстно-лицевые нарушения, осуществляется с использованием ортопедических и хирургических методов[9]. При необходимости применяются протезирование и вспомогательные ортопедические устройства[4].
Психологическая и социальная поддержка также имеет важное значение, поскольку особенности внешнего вида и мимики могут затруднять коммуникацию и социальную адаптацию. У детей могут наблюдаться трудности во взаимодействии с окружающими, а у их родителей — повышенный уровень стресса. В связи с этим рекомендуется психологическое сопровождение и, при необходимости, семейное консультирование[4].
Реабилитация играет ключевую роль и должна начинаться как можно раньше. Она включает физиотерапию, направленную на коррекцию двигательных нарушений, трудотерапию для формирования навыков самообслуживания, а также логопедическую помощь при нарушениях речи и глотания[4].
Прогноз
Прогноз при синдроме Мёбиуса во многом определяется степенью поражения ствола головного мозга и выраженностью функциональных нарушений. Заболевание является непрогрессирующим[7].
В лёгких и умеренных случаях продолжительность жизни пациентов, как правило, не отличается от популяционной. При этом качество жизни во многом зависит от своевременности реабилитации и коррекции сопутствующих нарушений. В более тяжёлых случаях, особенно при выраженном поражении ствола головного мозга, прогноз может быть неблагоприятным. Нарушения глотания, аспирация и невозможность адекватной защиты дыхательных путей повышают риск развития аспирационной пневмонии и дыхательной недостаточности, что может приводить к летальному исходу в раннем возрасте. Наиболее высокий риск смерти отмечается в неонатальном и раннем детском периоде, часто вследствие дыхательных нарушений или бульбарного паралича. Дополнительное влияние на прогноз оказывают сопутствующие осложнения[4].
Диспансерное наблюдение
Пациенты с синдромом Мёбиуса и их семьи нуждаются в наблюдении и консультациях специалистов различного профиля, что позволяет своевременно выявлять и корректировать сопутствующие нарушения. К таким специалистам относятся педиатр, хирург, детский стоматолог, ортопед, офтальмолог, оториноларинголог, психолог, физиотерапевт, специалист по трудотерапии, аудиолог и логопед[4].
Профилактика
Специфические меры профилактики синдрома Мёбиуса не разработаны. Общие профилактические рекомендации направлены на рациональное ведение беременности и минимизацию воздействия неблагоприятных факторов на плод. К ним относятся соблюдение здорового образа жизни, включая отказ от употребления алкоголя и курения, адекватное питание, оптимальный уровень физической активности, а также исключение воздействия потенциальных тератогенных факторов и бесконтрольного приёма лекарственных препаратов во время беременности[9].
Генетическое тестирование может быть применено только в редких случаях, когда в семье выявлены патогенные мутации, ассоциированные с развитием синдрома Мёбиуса. При этом специфических пренатальных маркеров заболевания не существует. Некоторые аномалии, например косолапость, могут быть выявлены при ультразвуковом исследовании плода, однако они не являются специфичными для данного синдрома[7].
Важную роль играет медико-генетическое консультирование семей, особенно при наличии в анамнезе врождённых аномалий развития. Несмотря на то, что семейные случаи встречаются редко (около 2 %), проведение консультации позволяет оценить потенциальные риски и информировать родителей о вероятности повторного возникновения заболевания[7].