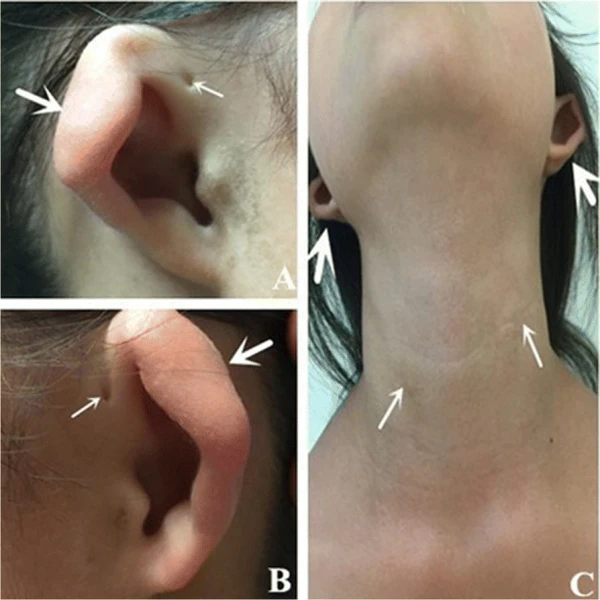
Бранхио-ото-ренальный синдром
Бранхи́о-о́то-рена́льный синдро́м (БОР, синдром Ме́льника — Фре́йзера) — врождённое заболевание, характеризующееся сочетанием патологии почек и слуха, которое проявляется в раннем возрасте. Основные клинические признаки включают аномалии развития ушных раковин, тугоухость или глухоту, наличие преаурикулярных свищей, а также пороки развития мочевыделительной системы, которые встречаются примерно у двух третей пациентов. Заболевание передаётся по аутосомно-доминантному типу наследования и с одинаковой частотой встречается у детей обоих полов[2].
Общие сведения
История
Впервые детальное описание признаков БОР-синдрома было представлено в 1975 году американским генетиком Мельником, а позднее, в 1978 году, канадский генетик Фрейзер дополнил характеристику этого заболевания[2].
Классификация и этиология
БОР-синдром является генетически гетерогенным заболеванием, для которого известны три типа[3]:
- тип 1 — связан с мутациями в гене EYA1 (в рамках этого типа выделяют бранхио-отический синдром — аллельный вариант БОР-синдрома, характеризующийся аналогичными клиническими проявлениями, но без поражения почек);
- тип 2 — связан с мутациями в гене SIX5;
- тип 3 — связан с мутациями в гене SIX1.
БОР-синдром передаётся по аутосомно-доминантному типу наследования[3].
Патогенез
Наиболее распространённый тип 1, составляющий около 40 % случаев, обусловлен мутациями в гене EYA1. Этот ген кодирует многофункциональный белок семейства Eyes Absent, который входит в консервативную регуляторную сеть Pax-Six-Eya-Dach, играющую ключевую роль в эмбриональном развитии глаз, внутреннего уха, почек и жаберных дуг. C-концевой домен белка EYA1 проявляет тирозинфосфатазную активность и участвует в репарации ДНК, а N-концевой домен функционирует как коактиватор транскрипционных факторов семейства Six (SIX1-6), регулируя экспрессию генов-мишеней. У 2 % пациентов с БОР-синдромом обнаруживаются патогенные мутации в гене SIX5, а у 2,5 % — в гене SIX1. Экспрессия гена EYA1 наблюдается на ранних стадиях эмбриогенеза в пресомитной мезодерме, мезенхиме головы, отических пузырьках и развивающихся почках, что объясняет множественные аномалии развития при БОР-синдроме. Нарушение функций белка EYA1 приводит к комбинированному поражению слуховой системы, жаберных дуг и почек, формируя характерную клиническую картину заболевания[3].
Эпидемиология
Распространённость БОР-синдрома составляет 1 случай на 40 000 детей и встречается с одинаковой частотой у обоих полов[4].
Диагностика
Аномалии второй жаберной дуги включают свищевой ход жаберной щели, проявляющийся точечным отверстием кпереди от грудино-ключично-сосцевидной мышцы, а также кисту жаберной щели в виде пальпируемого образования под этой мышцей. Эти симптомы наблюдаются примерно у половины пациентов с БОР-синдромом[5].
Нарушение слуха является наиболее частым симптомом БОР-синдрома, встречаясь более чем у 90 % пациентов. Наблюдаются различные типы тугоухости, наиболее распространённой из которых является смешанная форма. Среди других отологических аномалий наиболее часто встречаются преаурикулярные свищи, реже — жаберные свищи, деформации ушных раковин, стеноз наружного слухового прохода и преаурикулярные привески[5].
Почечные аномалии, включающие гипоплазию почки, агенезию и гидронефроз вследствие пузырно-мочеточникового рефлюкса или обструкции лоханочно-мочеточникового сегмента, наблюдаются примерно у 67 % пациентов с БОР-синдромом, при этом почечная гипоплазия является наиболее частым проявлением. У части пациентов отмечаются разные типы аномалий в каждой почке[5].
Сердечная патология редко встречается при БОР-синдроме, хотя описаны случаи пролапса митрального клапана и брадикардии во время анестезии[5].
Задержка психомоторного развития не характерна для типичного БОР-синдрома[5].
Аудиологические исследования пациентов с БОР-синдромом выявляют нарушения слуха в 90 % случаев. Характер слуховых расстройств у таких больных отличается значительным разнообразием — от минимальной степени тугоухости до полной глухоты. Наблюдаются как стабильные, так и прогрессирующие формы снижения слуха, которые могут дебютировать как в раннем детском возрасте, так и в подростковый период[2].
При компьютерной томографии височных костей у пациентов с БОР-синдромом выявляются характерные изменения, включая так называемую «развёрнутую улитку», при которой средний и апикальный завитки смещены кпереди и медиально, отдаляясь от базального завитка, а также изменённый ход лицевого нерва, проходящего медиальнее улитки. Дополнительными частыми находками являются гипоплазия апикального завитка улитки, недоразвитие модиолуса, воронкообразное расширение внутреннего слухового прохода и патологически расширенная (зияющая) евстахиева труба[6].
Для клинической диагностики БОР-синдрома применяются критерии, разделённые на большие и малые[2]:
- к большим критериям относятся наиболее характерные проявления: тугоухость, преаурикулярные свищи, аномалия почек (гипоплазия или агенезия, поликистоз, нарушение ротации, дефекты чашечно-лоханочной системы), свищи шеи и стеноз наружного слухового прохода;
- малые критерии включают менее специфичные признаки: атрезию слёзного протока, расщелину неба, ретрогнатию, врождённую дисплазию тазобедренных суставов, парез лицевого нерва и кистозные изменения поджелудочной железы.
Диагноз считается подтверждённым при наличии[2]:
- либо трёх больших критериев;
- либо двух больших и двух малых критериев;
- либо двух больших критериев у пациента плюс одного большого критерия у ближайшего родственника.
Дифференциальная диагностика
Дифференциальная диагностика БОР-синдрома проводится со следующими состояниями[5]:
- синдром Таунса — Брокса;
- бранхио-окуло-фациальный синдром;
- ото-фацио-цервикальный синдром;
- синдром CHARGE;
- HDR-синдром (Hypoparathyroidism, Deafness, Renal dysplasia).
Лечение
Этиологического лечения БОР-синдрома нет. Лечение носит симптоматический и патогенетический характер . Детям с нарушением слуха необходимо своевременное лечение отитов. Применение слуховых аппаратов может быть эффективным, а при структурных аномалиях уха рассматривается возможность хирургической коррекции[7].
Жаберные аномалии (кисты, свищи) требуют хирургического удаления из-за высокого риска инфицирования; при наличии инфекции назначается антибактериальная терапия[7].
При тяжёлой почечной недостаточности рассматривается вопрос о диализе или трансплантации почки[7].
Прогноз
Большинство пациентов с БОР-синдромом при получении адекватного лечения могут вести нормальную активную жизнь. Прогноз для таких пациентов в первую очередь определяется степенью поражения почек. В тяжёлых случаях почечная недостаточность может прогрессировать до терминальной стадии, требующей заместительной терапии[8].
Диспансерное наблюдение
Пациентам с БОР-синдромом показано диспансерное наблюдение[9]:
Примечания
Литература
- Гарманова Т. Н. Генетические причины врождённых заболеваний почек и верхних мочевыводящих путей. Обзор литературы // Экспериментальная и клиническая урология. — 2016. — № 2.