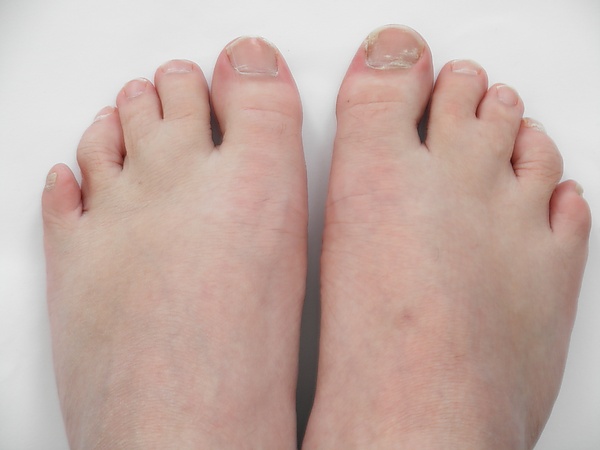
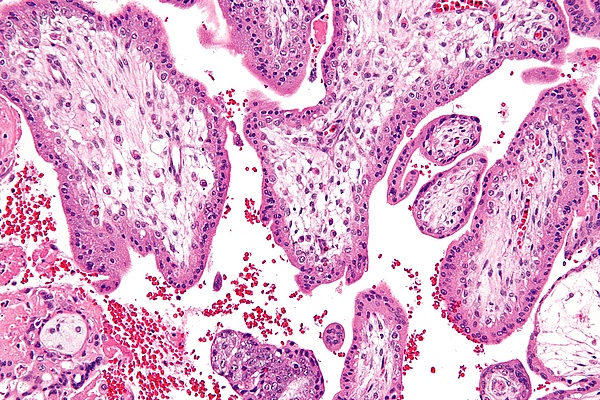
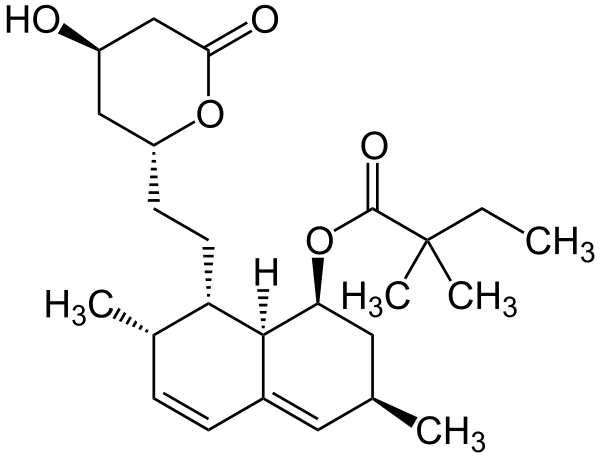
Синдром Смита — Лемли — Опица
Синдром Смита — Лемли — Опица — это аутосомно-рецессивное заболевание, возникающее из-за неспособности организма синтезировать холестерин[2]. Синдром встречается редко, но проявляется тяжело, его частота составляет 1 на 10 000-70 000 новорождённых. Ошибки в эмбриогенезе возникают из-за отсутствия продукции холестерина, что приводит к дисфункции клеточной мембраны и отсутствию активации белков hedgehog, отвечающих за координацию транслокации и дифференциации. Дальнейшие осложнения возникают из-за постоянной неспособности вырабатывать холестерин и накопления предшественников холестерина[3].
Общие сведения
История
Синдром назван в честь Дэвида Вейхе Смита (1926—1981), американского педиатра; Люка Лемли (1935-), бельгийского врача; и Джона Мариуса Опица (1935—2023), немецко-американского врача. Это исследователи, которые первыми описали симптомы синдрома Смита — Лемли — Опица[4].
Наиболее распространённым животным, используемым для изучения синдрома Смита — Лемли — Опица, является мышь. По данным BioCyc, биосинтез холестерина у мышей очень похож на биосинтез холестерина у людей. Самое главное, что у мышей есть как DHCR7 (фермент, ответственный за синдром Смита — Лемли — Опица), так и ГМГ-КоА-редуктаза (важна для стадии, ограничивающей скорость синтеза холестерина)[5]. Крысы похожи на мышей и также использовались. Существует два популярных способа создания животных моделей синдрома Смита — Лемли — Опица. Первый — это использование тератогенов, второй — генетические манипуляции для создания мутаций в гене DHCR7[6].
Ген, кодирующий DHCR7 (обозначенный как DHCR7), был клонирован в 1998 году. Тогда же установили его расположение на хромосоме 11q12-13. Длина этого гена составляет 14100 пар оснований и содержит девять экзонов. Длина соответствующей мРНК составляет 2786 пар оснований (оставшаяся последовательность ДНК является интронной). Структура крысиного гена DHCR7 очень похожа на структуру человеческого гена[2].
Тератогенные модели индуцируются путём скармливания беременным крысам или мышам ингибиторов DCHR7. Двумя распространёнными ингибиторами являются BM15766 (4-(2-[1-(4- хлорциннамил)пиперазин-4-ил]этил)-бензойной кислоты) и AY9944 (транс-l,4-бис(2-хлорбензиламиномети1)дигидрохлорид циклогексана). Эти соединения обладают различными химическими и физическими свойствами, но вызывают сходные эффекты. Было показано, что AY9944 вызывает голопроэнцефалию и пороки полового развития, подобные тем, которые наблюдаются у людей с синдромом Смита — Лемли — Опица. Известно также, что он вызывает нарушения в работе серотониновых рецепторов — ещё один дефект, часто наблюдаемый у пациентов с синдромом Смита — Лемли — Опица[7]. BM15766 приводит к отсутствию синтеза холестерина и жёлчных кислот, что наблюдается у пациентов с синдромом Смита — Лемли — Опица с гомозиготными мутациями. Все тератогенные модели могут быть эффективно использованы для изучения синдрома Смита — Лемли — Опица; однако они демонстрируют более низкие уровни 7-DHC и 8-DHC, чем у людей. Это может быть объяснено тем фактом, что у людей наблюдается постоянный блок активности DHCR7, в то время как у мышей и крыс, получавших ингибиторы, наблюдались только временные блоки. Кроме того, различные виды мышей и крыс более устойчивы к тератогенам и могут быть менее эффективными в качестве моделей синдрома Смита — Лемли — Опица[8]. Тератогенные модели чаще всего используются для изучения более долгосрочных последствий синдрома Смита — Лемли — Опица, поскольку они сохраняются дольше, чем генетические модели. Например, в одном исследовании изучалась дегенерация сетчатки при синдроме Смита — Лемли — Опица, которая у крыс наступает по крайней мере через месяц после рождения[7].
Генетические модели синдрома Смита — Лемли — Опица создаются путём нокаутирования гена DHCR7. В одном исследовании для разрушения DCHR7 в эмбриональных стволовых клетках мыши использовалась гомологичная рекомбинация. Подобно тому, что наблюдается у людей, гетерозиготные мыши (имеющие только один мутированный аллель) были фенотипически нормальными, и их скрещивали для получения детёнышей, гомозиготных по мутированному аллелю. Хотя эти детёныши умерли в течение первого дня жизни из-за своей неспособности питаться, они демонстрировали характеристики, сходные с человеческими, страдающими синдромом Смита — Лемли — Опица. У них был снижен уровень холестерина, повышен уровень 7- и 8DHC, они отличались замедленным ростом и меньшим весом при рождении, имели черепно-лицевые пороки развития и были менее подвижны. У многих также была волчья пасть и сниженная реакция нейронов на глутамат. Однако в целом у детёнышей было меньше дисморфологических признаков, чем у людей с синдромом Смита — Лемли — Опица; у них не было пороков развития конечностей, почек, надпочечников или центральной нервной системы. Это объясняется тем фактом, что у грызунов материнский холестерин может проникать через плаценту и, по-видимому, действительно необходим для развития плода. У человека очень мало материнского холестерина передаётся плоду. Таким образом, генетическая мышиная модель полезна для объяснения нейропатофизиологии синдрома Смита — Лемли — Опица[6]
Многие открытия в исследованиях синдрома Смита — Лемли — Опица были сделаны с использованием моделей на животных. Они были использованы для изучения различных методов лечения, включая эффективность терапии симвастатином[9]. В других исследованиях изучались поведенческие характеристики, при попытке объяснить лежащий в их основе патогенез[10]. Общим открытием является то, что мышиные модели синдрома Смита — Лемли — Опица демонстрируют аномальное серотонинергическое развитие, которое может быть, по крайней мере, частично ответственно за аутистическое поведение, наблюдаемое при синдроме Смита — Лемли — Опица[11]. Мышиные модели также использовались для разработки методов диагностики; в многочисленных исследованиях изучались биомаркеры, которые являются результатом окисления 7DHC, такие как DHCEO[12]. Вполне вероятно, что по мере совершенствования моделей на животных они приведут к ещё большему количеству открытий в исследованиях синдрома Смита — Лемли — Опица[13].
Классификация
Синдром Смита — Лемли — Опица может проявляться по-разному в разных случаях, в зависимости от тяжести мутации и других факторов. Первоначально пациентов с этим синдромом разделяли на две категории (классическая и тяжёлая) в зависимости от физических и психических характеристик, а также других клинических особенностей. С момента обнаружения специфического биохимического дефекта, ответственного за синдром Смита — Лемли — Опица, пациентам присваивается оценка степени тяжести, основанная на уровнях дефектов головного мозга, глаз, полости рта и гениталий. Затем эта оценка используется для классификации пациентов в соответствии с лёгкой, классической или тяжёлую формой заболевания[14].
Этиология
Синдром Смита — Лемли — Опица является аутосомно-рецессивным заболеванием[2].
Эпидемиология
Синдром Смита — Лемли — Опица чаще всего описывается в европейских популяциях. Также диагностируются люди афро-карибского, японского, восточноазиатского, корейского и арабского происхождения[15][16]. Частота встречаемости оценивается как 1 на 20 000-70 000 новорождённых[17]. Большая распространённость в европейских популяциях, как предполагается, является эффектом основателя[18]. Оценочная распространённость носителей в белой популяции составляет от 1 % до 2 %. Частота пациентов с синдромом Смита — Лемли — Опица ниже из-за перинатальной смертности в тяжёлых случаях и недостаточной диагностики в лёгких случаях[15].
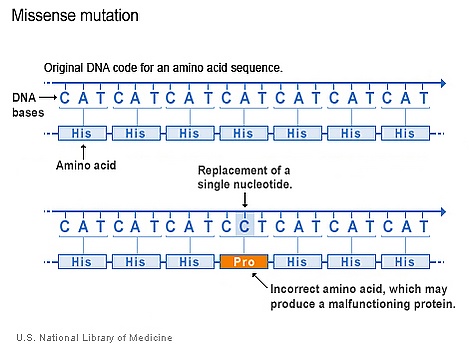
Было идентифицировано более 130 различных типов мутаций. Миссенс-мутации (изменение одного нуклеотида, приводящее к кодированию другой аминокислоты) являются наиболее распространёнными и составляют 87,6 % спектра синдрома Смита — Лемли — Опица . Они обычно снижают функцию фермента, но не могут подавлять его полностью. Многое зависит от природы мутации (то есть от того, какая аминокислота заменена и где). Нулевые мутации встречаются гораздо реже, эти мутации приводят либо к полностью нефункциональному ферменту, либо к отсутствию фермента вообще. Таким образом, миссенс-мутации могут быть более распространены в целом, поскольку они менее смертельны, чем нонсенс-мутации; нонсенс-мутации могут просто привести к самопроизвольному прерыванию беременности[19].
Мутация IVS8-1G>C является наиболее часто регистрируемой мутацией в DHCR7. Эта мутация приводит к нарушению соединения восьмого и девятого экзонов и приводит к вставке 134 нуклеотидов в транскрипт DHCR7. Это нонсенс-мутация, поэтому пациенты, гомозиготные по этому аллелю, сильно страдают. Считается, что эта мутация впервые произошла на Британских островах, и её носительство встречается с частотой 1,09 % среди европейцев. Частота мутаций различна у разных этнических групп, в зависимости от происхождения мутации. Во всех европеоидных популяциях частота носительства этой конкретной мутации составляет, по оценкам, 3 %[2].
Следующая наиболее распространённая мутация — 278C>T, которая приводит к появлению треонина в аминокислотном положении 93. Это миссенс-мутация, которая, как правило, сопровождается менее серьёзными симптомами. Эта мутация наиболее часто встречается у пациентов итальянского, кубинского и средиземноморского происхождения[2].
Третьей наиболее распространённой мутацией является мутация 452G>A. Эта нонсенс-мутация вызывает разрушение белка, так что фермент DHCR7 не образуется. Считается, что он возник на юге Польши и наиболее распространён в Северной Европе[2].
Другие мутации встречаются реже, хотя, по-видимому, они в большей степени воздействуют на определённые белковые домены, чем на другие. Например, мотивы стеролредуктазы являются распространёнными участками мутации. В целом, по оценкам, частота носительства (любой мутации DHCR7, вызывающей синдром Смита — Лемли — Опица) составляет 3-4 % в европеоидных популяциях (среди азиатских и африканских популяций она встречается реже). Это число указывает на гипотетическую частоту рождений в диапазоне от 1/2500 до 1/4500. Однако измеренный показатель заболеваемости составляет от 1/10 000 до 1/60 000 (он различается в зависимости от происхождения). Это намного ниже, чем ожидалось. Это указывает на то, что многие случаи синдрома Смита — Лемли — Опица остаются незамеченными и, вероятно, происходят либо из-за самопроизвольного прерывания беременности, вызванного тяжёлыми мутациями (выкидыш), либо из-за лёгких случаев, которые не диагностируются. У женщин отсутствуют характерные пороки развития половых органов, которые наблюдаются у мужчин, и, следовательно, у них меньше шансов на правильный диагноз[20].
Патогенез
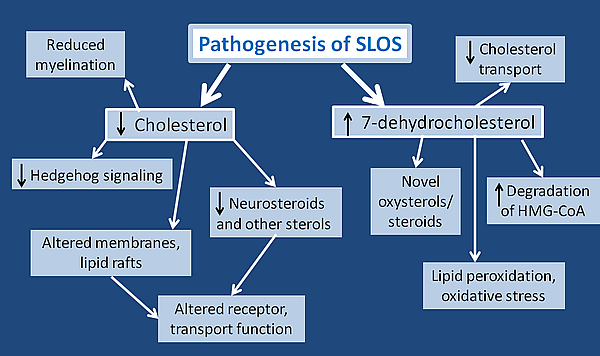
Учитывая, что функции холестерина охватывают очень широкий спектр, маловероятно, что симптомы синдрома Смита — Лемли — Опица обусловлены каким-то одним молекулярным механизмом. Некоторые молекулярные эффекты пока неизвестны, но их можно предположить на основе роли холестерина. В целом, негативные эффекты обусловлены снижением уровня холестерина и повышением уровня предшественников холестерина, в первую очередь 7DHC. Хотя 7DHC структурно схож с холестерином и потенциально может выступать в качестве заменителя, его влияние все ещё изучается[3].
У большинства пациентов с синдромом Смита — Лемли — Опица наблюдается снижение уровня холестерина, особенно в головном мозге. Это также означает, что уровень любых стерольных производных холестерина также будут понижены. Например, при синдроме Смита — Лемли — Опица можно наблюдать снижение уровня нейростероидов. Это липиды, которые принимают участие в передаче сигналов в головном мозге и должны вырабатываться в самом мозге. Они отвечают за взаимодействие с ядерными стероидными рецепторами и связываются с ионными каналами, управляемыми нейромедиаторами. В частности, они модулируют действие ГАМК- и NMDA-рецепторов, что приводит к успокаивающему эффекту, улучшению памяти и многому другому. Таким образом, учитывая, что некоторые характеристики синдрома Смита — Лемли — Опица противоположны этим эффектам (гиперактивность, тревожность), снижение уровня нейростероидов может повлиять как на неврологическое развитие, так и на поведение[21].
Кроме того, как было указано выше, холестерин является важным аспектом передачи сигналов Hedgehog. При более низком уровне холестерина белки hedgehog не подвергались бы необходимой ковалентной модификации и последующей активации. Это может привести к нарушению эмбрионального развития и может способствовать наблюдаемым физическим врождённым дефектам у детей с синдромом Смита — Лемли — Опица. Один из специфических сигнальных белков, sonic hedgehog (SHH), играет важную роль в формировании структур центральной нервной системы, черт лица и конечностей[3]. Другие белки сигнального каскада hedgehog могут быть вовлечены в развитие половых путей и скелета[14].
Изменённый уровень стеролов при синдроме Смита — Лемли — Опица особенно важен для клеточных мембран, которые состоят в основном из липидов. У пациентов с синдромом Смита — Лемли — Опица клеточные мембраны могут иметь аномальные свойства или состав, а сниженный уровень холестерина значительно влияет на стабильность липидных рафтов и белков. Несмотря на их структурное сходство, 7DHC не способен заменить холестерин в липидных рафтах[22]. Кроме того, недостаток холестерина способствует повышению текучести клеточной мембраны и может вызвать аномальное выделение гранул. Все эти изменения в мембране, вероятно, способствуют изменениям в транспортных функциях, которые наблюдаются при синдроме Смита — Лемли — Опица. Они могут вызывать нарушения дегрануляции тучных клеток, опосредованной рецепторами IgE, и выработки цитокинов. Это влияет на NMDA-рецепторы, а также на связывающую способность серотонинового рецептора гиппокампа. Взаимодействие между клетками, которое очень важно для развития, может быть нарушено[23]. Было показано, что экзоцитоз в синаптических везикулах снижен, вероятно, из-за нарушения слияния везикул с клеточной мембраной или плохой утилизации везикул[24]. Наконец, холестерин широко распространён в миелине, поэтому у пациентов с синдромом Смита — Лемли — Опица наблюдается снижение миелинизации полушарий головного мозга, периферических и черепно-мозговых нервов[21].
В дополнение к снижению уровня холестерина, многие симптомы, проявляющиеся при синдроме Смита — Лемли — Опица, обусловлены токсическим действием 7DHC. Известно, что 7DHC нарушает внутриклеточный транспорт холестерина. Он также усиливает расщепление ГМГ-КоА-редуктазы (фермента, который катализирует ограничивающую скорость стадию синтеза холестерина). 7DHC приводит к появлению новых производных оксистерола и стероидов, и многие из их функций или эффектов пока неизвестны. Очень важным открытием в отношении 7DHC является то, что он является наиболее активным липидом для перекисного окисления липидов и приводит к системному окислительному стрессу. Известно, что перекисное окисление липидов разрушает мембраны как клеток, так и мембраносвязанных органелл. Производным 7DHC, которое используется для обозначения окислительного стресса, является 3β,5α-дигидрокси-холест-7-ен-6-он (DHCEO); это соединение образуется из первичного продукта перекисного окисления 7DHC, 7-DHC-5α,6α-эпоксида. DHCEO токсичен для кортикальных нейрональных и глиальных клеток и ускоряет их дифференцировку и разрастание[25]. Считается, что 7DHC, вызывающий окислительный стресс, ответственен за повышенную светочувствительность, проявляющуюся у пациентов с синдромом Смита — Лемли — Опица. Обычное воздействие UVA может привести к окислительному стрессу в клетках кожи. Учитывая, что 7DHC легче окисляется, он усиливает действие UVA, что приводит к усилению окисления липидов мембран и увеличению выработки активных форм кислорода (АФК)[22].
Как правило, более высокие уровни 7DHC и холестерина приводят к более серьёзным симптомам синдрома Смита — Лемли — Опица. Уровни этих метаболитов также соответствуют тяжести мутации (нонсенс или миссенс-мутация); при некоторых мутациях DHCR7 все ещё может наблюдаться остаточный синтез холестерина, а при других — нет. Однако даже у людей с одинаковыми мутациями или генотипом симптомы могут быть разными. Это может быть связано с материнскими факторами, такими как передача холестерина плоду во время беременности, а также с количеством холестерина, присутствующего в головном мозге до того, как внутриутробно сформируется гематоэнцефалический барьер. Скорость накопления и выведения токсичных метаболитов может варьироваться у разных людей. Материнский аполипопротеин Е также участвует в индивидуальной изменчивости проявлений синдрома Смита — Лемли — Опица, хотя точная природа этой взаимосвязи неизвестна. Вероятно, существует ещё больше факторов, способствующих широкому спектру эффектов синдрома Смита — Лемли — Опица, которые ещё не были обнаружены[19].
Учитывая, что синдром Смита — Лемли — Опица вызывается мутацией в гене, кодирующем фермент, который участвует в синтезе холестерина, результирующие биохимические характеристики могут быть предсказуемыми. У большинства пациентов наблюдается снижение уровня холестерина в плазме крови (гипохолестеринемия)[14]. Однако примерно у 10 % может наблюдаться нормальный уровень холестерина, и снижение концентрации холестерина свидетельствует не только о синдроме Смита — Лемли — Опица. Повышенный уровень предшественников холестерина также характерен для синдрома Смита — Лемли — Опица. В частности, повышенный уровень 7-дегидрохолестерина довольно специфичен для этого заболевания[3].
Диагностика
Синдром Смита — Лемли — Опица может проявляться широким спектром клинических признаков и отличается большой фенотипической изменчивостью[26][27]. Это состояние может привести к внутриутробной смерти, аномалиям плода, выявляемым при сканировании, дисморфическим признакам при рождении или нейроинвалидности на более поздних этапах жизни[15]. Признаки наблюдаются в дородовой период в виде повышенной прозрачности воротникового пространства[28].
Постнатальные признаки могут включать следующее:
Черепно-лицевые признаки[29]
- Микроцефалия
- Микрогнатия
- Билатеральный птоз
- Битемпальное сужение
- Волчья пасть
- Короткий вздёрнутый нос
Центральная нервная система[30]
- Гипотония
- Гипопластическое или отсутствующее мозолистое тело
- Гипопластические лобные доли
- Увеличенные желудочки
- Липомы гипофиза
- Глобальная задержка развития
- Нарушение обучаемости
- Голопрозэнцефалия
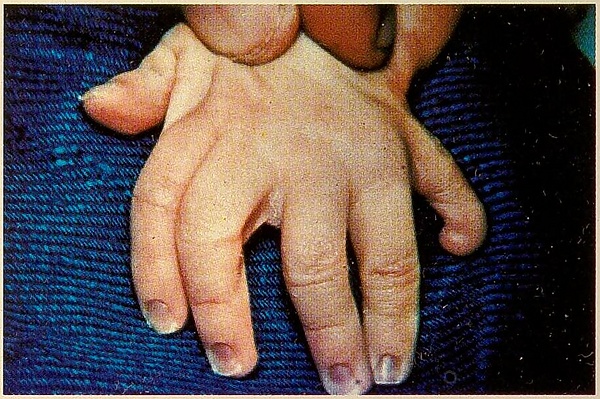
Рост и скелет[31]
- Задержка роста
- Аномальные отпечатки пальцев
- Постаксиальная полидактилия
- Синдактилия
Гениталии[32]
- Двойственные гениталии
- Гипоспадия
- Реверсия пола
Сердечно-сосудистые[33]
- Ostium primum
- Дефекты межпредсердной перегородки
- Дефекты межжелудочковой перегородки
- Открытый артериальный проток
- Атриовентрикулярный канал
Почки и надпочечники[34]
- Гипо/гиперплазия надпочечников
- Эктопия почек
- Аплазия/гипоплазия почек
- Кисты коркового вещества почек
- Удвоение мочеточника
- Недоразвитые наружные половые органы и гипоспадия (у мужчин)
Дыхательная система[35]
- Аномалии хрящей трахеи и гортани
- Лёгочная гипоплазия
- Аномальная лёгочная дольчатость
Гастроэнтерология[36]
- Гастроэзофагеальная рефлюксная болезнь (ГЭРБ)
- Пилоростеноз
- Болезнь Гиршпрунга
- Нарушение моторики кишечника
- Холестатическое заболевание печени
У пациентов с синдромом Смита — Лемли — Опица обычно наблюдаются определённые особенности поведения. У них может быть низкий нормальный интеллект, и они могут негативно или с повышенной чувствительностью реагировать на различные сенсорные раздражители. Это особенно верно в отношении определённых слуховых и зрительных стимулов. Многие пациенты проявляют агрессивность и причиняют себе вред, а нарушения сна представляют собой обычное явление[14]. Часто наблюдается специфическое поведение, напоминающее поведение людей с аутизмом, а также гиперактивность. Аутистическое поведение, наиболее характерное для пациентов с синдромом Смита — Лемли — Опица, — это опистокинез (движение верхней части тела), потягивание верхней части тела и взмахи руками[37]. Аутизм обычно диагностируется отдельно от синдрома Смита — Лемли — Опица с помощью DSM-5, и примерно 50-75 % пациентов с синдромом Смита — Лемли — Опица соответствуют критериям аутизма[38].
Другие формы поведения, ассоциированные с синдромом Смита — Лемли — Опица, могут быть напрямую связаны с физическими отклонениями. Например, у младенцев часто возникают проблемы с кормлением или пищевая непереносимость, и пациентам может потребоваться повышенное потребление калорий из-за ускоренного метаболизма. Также часто встречаются рецидивирующие инфекции, включая ушные инфекции и пневмонию[14].
Наиболее характерным биохимическим показателем синдрома Смита — Лемли — Опица является повышенный уровень 7DHC(снижение уровня холестерина также характерно, но проявляется и при других заболеваниях). Таким образом, внутриутробно синдром Смита — Лемли — Опица диагностируется при обнаружении повышенного соотношения 7DHC:общий стерол в тканях плода или повышенного уровня 7DHC в околоплодных водах. Соотношение 7DHC:общий уровень стеролов можно измерить на 11-12 неделе беременности с помощью пробы ворсинок хориона, а повышенный уровень 7DHC в околоплодных водах можно определить к 13 неделям. Кроме того, если известны родительские мутации, может быть проведено ДНК-тестирование образцов околоплодных вод или ворсинок хориона[14].
Амниоцентез (процесс взятия проб околоплодных вод) и забор ворсинок хориона не могут быть выполнены ранее, чем примерно на 3 месяце беременности. Учитывая, что синдром Смита — Лемли — Опица является очень тяжёлым синдромом, родители могут захотеть прервать беременность, если это повлияет на их плод. Амниоцентез и забор ворсин хориона оставляют очень мало времени для принятия такого решения (аборты становятся все более трудными по мере развития беременности), а также могут представлять серьёзный риск для матери и ребёнка. Таким образом, существует очень большая потребность в неинвазивных диагностических тестах в середине беременности[39]. Исследование концентрации стеринов в моче матери является одним из потенциальных способов пренатального выявления синдрома Смита — Лемли — Опица. Во время беременности плод самостоятельно синтезирует холестерин, необходимый для выработки эстриола. Плод с синдромом Смита — Лемли — Опица не может вырабатывать холестерин и вместо него может использовать 7DHC или 8DHC в качестве предшественников эстриола. В результате образуются 7- или 8-дегидростероиды (такие как 7-дегидроэстриол), которые могут обнаруживаться в моче матери. Это новые метаболиты из-за наличия в норме редуцированной двойной связи в углероде 7 (вызванной неактивностью DHCR7), и их можно использовать в качестве индикаторов синдрома Смита — Лемли — Опица[40]. Другие производные холестерина, которые обладают двойной связью в 7-м или 8-м положении и присутствуют в моче матери, также могут быть использованы в качестве индикаторов синдрома Смита — Лемли — Опица. быть индикаторами синдрома Смита — Лемли — Опица. Было показано, что 7- и 8-дегидропрегнантриолы присутствуют в моче матерей с поражённым плодом, но не у здоровых плодов, и, таким образом, используются при диагностике. Эти прегнадиены возникают у плода и проходят через плаценту, прежде чем попасть к матери. Их выделение указывает на то, что ни плацента, ни материнские органы не обладают необходимыми ферментами, необходимыми для уменьшения двойной связи этих новых метаболитов[39].
Если синдром Смита — Лемли — Опица остаётся незамеченным до рождения, диагноз может быть основан на характерных физических особенностях, а также на выявлении повышенного уровня 7DHC в плазме крови[41]
Существует множество различных способов определения уровня 7DHC в плазме крови, одним из которых является использование реактива Либермана-Бурхарда. Это простой колориметрический анализ, разработанный с целью использования для крупномасштабного скрининга. При обработке реактивом Либермана-Бурхарда образцы, полученные от пациентов с синдромом Смита — Лемли — Опица сразу же становятся розовыми и постепенно синеют; обычные образцы крови изначально бесцветны и приобретают слабый голубой оттенок. Хотя этот метод имеет ограничения и не используется для постановки окончательного диагноза, он привлекателен тем, что является гораздо более быстрым методом, чем использование клеточных культур[41].
Другим способом определения 7DHC является газовая хроматография — метод, используемый для разделения и анализа соединений. Газовая хроматография/масс-спектрометрия для мониторинга отдельных ионов является очень чувствительной версией газовой хроматографии и позволяет обнаруживать даже незначительные случаи синдрома Смита — Лемли — Опица[42]. Другие методы включают времяпролётную масс-спектрометрию, жидкостной хроматографии/масс-спектрометрии с пучком частиц, тандемную масс-спектрометрию с электрораспылением, и поглощение ультрафиолета — все это может быть использовано для анализа образцов крови, околоплодных вод или ворсинок хориона. Измерение уровня жёлчных кислот в моче пациентов или изучение активности DCHR7 в культуре тканей также являются распространёнными методами послеродовой диагностики[41].
Дифференциальная диагностика
Дифференциальная диагностика синдрома Смита — Лемли — Опица широка и включает несколько синдромов с мультисистемным воздействием. Эти состояния имеют перекрывающиеся дисморфические черты, что затрудняет клиническую диагностику[43]. Они включают, но не ограничиваются[44][45]:
- Синдром Гарднера-Силенго-Вахтеля (генито-палато-кардиальный синдром)[46]
- Синдром Янга Маддерса (псевдотрисомия 13/голопрозэнцефалия-полидактилия)[47]
- Синдром Патау (трисомия 13)[48]
- Синдром Нунан[49]
- Опиц G (синдром BBB)[50]
- Синдром Эдвардса (трисомия 18)[51]
- Синдром Цельвегера[52]
- Последовательность Пьера Робина[53]
Лечение
Работа с пациентами с диагнозом Смита — Лемли — Опица, сложна и часто требует привлечения команды специалистов. Некоторые врождённые пороки развития (волчья пасть) можно исправить хирургическим путём. Другие методы лечения ещё не доказали свою эффективность в рандомизированных исследованиях, однако, как ни странно, они приводят к улучшению состояния[54].
Наиболее распространённой формой лечения синдрома Смита — Лемли — Опица является приём пищевых добавок, содержащих холестерин[17]. Отдельные сообщения указывают на то, что это имеет некоторые преимущества; это может привести к ускорению роста, снижению раздражительности, улучшению коммуникабельности, уменьшению случаев нанесения себе увечий, уменьшению тактильной защищённости, уменьшению числа инфекций, повышению мышечного тонуса, светочувствительности и снижению проявлений аутичного поведения[9]. Приём добавок холестерина начинается с дозы 40-50мг/кг/сут, по мере необходимости дозировку увеличивают. Его вводят либо при употреблении продуктов с высоким содержанием холестерина (яйца, сливки, печень), либо в виде очищенного пищевого холестерина. Детям младшего возраста и младенцам грудного возраста может потребоваться кормление через зонд. Однако пищевой холестерин не снижает уровень 7DHC, не может проникать через гематоэнцефалический барьер и, по-видимому, не улучшает результаты развития. Одно эмпирическое исследование показало, что добавки с холестерином не оказывают влияния задержку развития, независимо от возраста, в котором она началась. Вероятно, это связано с тем, что большинство задержек в развитии связаны с пороками развития головного мозга, которые диетический холестерин не может устранить из-за его неспособности преодолевать гематоэнцефалический барьер[55]
Ингибиторы ГМГ-КоА-редуктазы были изучены в качестве средства лечения синдрома Смита — Лемли — Опица. Учитывая, что этот фермент катализирует стадию, ограничивающую скорость синтеза холестерина, его ингибирование уменьшило бы накопление токсичных метаболитов, таких как 7DHC[17]. Симвастатин является известным ингибитором ГМГ-КоА-редуктазы и, что наиболее важно, способен проникать через гематоэнцефалический барьер. Сообщалось, что он снижает уровень 7DHC, а также повышает уровень холестерина. Повышенный уровень холестерина обусловлен влиянием симвастатина на экспрессию различных генов. Симвастатин увеличивает экспрессию DHCR7, что, вероятно, приводит к повышению активности DHCR7. Было также показано, что он увеличивает экспрессию других генов, участвующих в синтезе и усвоении холестерина. Однако эти преимущества зависят от количества остаточного синтеза холестерина. Поскольку некоторые люди обладают менее выраженными мутациями и демонстрируют некоторую активность DCHR7, терапия симвастатином приносит наибольшую пользу этим людям, поскольку у них все ещё частично функционирует фермент. Для индивидуумов, у которых не наблюдается остаточной активности DCHR7, таких как гомозиготы по нулевым аллелям или мутациям, терапия симвастатином на самом деле может быть токсичной Это подчёркивает важность определения конкретного генотипа пациента с синдромом Смита — Лемли — Опица перед назначением лечения. До сих пор неизвестно, может ли симвастатин положительно влиять на поведенческие нарушения у детей с синдромом Смита — Лемли — Опица[56].
Антиоксиданты — это вещества, которые ингибируют окисление молекул или уменьшают количество метаболитов, которые ранее были окислены. Учитывая, что некоторые симптомы синдрома Смита — Лемли — Опица, как полагают, являются результатом перекисного окисления 7DHC и его производных, ингибирование этого перекисного окисления, вероятно, будет иметь положительный эффект. Было показано, что антиоксиданты повышают уровень липидных транскриптов в клетках, эти транскрипты играют важную роль в биосинтезе липидов (холестерина) и, как известно, их уровень понижен при синдроме Смита — Лемли — Опица. Кроме того, известно, что витамин Е, в частности, снижает уровень DHCEO, который является показателем окислительного стресса при синдроме Смита — Лемли — Опица, а также оказывает благотворное влияние на экспрессию генов. Витамин Е, по-видимому, является самым мощным антиоксидантом для лечения синдрома Смита — Лемли — Опица, и в экспериментах на мышах он снижал уровень оксистеролов в головном мозге. Однако антиоксиданты были изучены только на животных моделях синдрома Смита — Лемли — Опица или изолированных клетках. Таким образом, их клиническое значение и негативные побочные эффекты до сих пор неизвестны, а их применение на людях ещё предстоит изучить[57].
При лечении синдрома Смита — Лемли — Опица зачастую стоит вопрос, связаны ли интеллектуальные и поведенческие нарушения с конкретными проблемами развития (то есть с конкретными пороками развития мозга) или с сохраняющимися аномальными уровнями стеролов, которые нарушают нормальную функцию мозга и других тканей. Если верно последнее, то методы лечения, которые изменяют уровень и соотношение стеролов, особенно в головном мозге, скорее всего, улучшат результаты развития пациента. Однако, если верно первое, то лечение, скорее всего, поможет только при симптомах, а не при конкретных нарушениях развития[58].