Синдром Аарскога — Скотта
Синдро́м Аарско́га — Ско́тта (САС, фациогенитальная или фациодигитогенитальная дисплазия) — наследственное заболевание, связанное с X-хромосомой, для которого характерны аномалии строения лица, скелета и половых органов, а также возможны задержки в умственном и физическом развитии[2].
Общие сведения
История
САС впервые описал Аарског в 1970 году, а затем Скотт детализировал его наблюдения, изучив две разные семьи с несколькими поражёнными мужчинами. В последующие годы другие исследователи сообщали о похожих случаях, отмечая у больных различные сочетания симптомов: клинодактилию, брахидактилию, удлинённый желобок верхней губы, вдовий пик, камптодактилию, перепонки между пальцами, а также паховые или пупочные грыжи. Эти наблюдения помогли выделить синдром как отдельное заболевание[3].
Этиология
Развитие САС связано с мутацией в гене FGD1. Этот ген локализован на коротком плече X-хромосомы (Xq11.22) и кодирует фактор обмена гуаниновых нуклеотидов, непосредственно участвуя в организации цитоскелета, регуляции роста и нормального эмбрионального развития у всех млекопитающих[3].
В гене FGD1 при САС было выявлено 52 различных мутации. Синдром демонстрирует клиническую и генетическую гетерогенность — помимо FGD1, в его патогенезе могут участвовать и другие, пока не идентифицированные, гены[3].
Патогенез
Ген FGD1 кодирует одноимённый белок FGD, функционирующий как активатор ГТФазы Cdc42. Этот фермент, относящийся к гидролазам, катализирует гидролиз гуанозинтрифосфата и играет ключевую роль в передаче внеклеточных сигналов. Cdc42 регулирует формирование и динамику цитоскелета, контролируя деление клеток, апоптоз и экспрессию генов. При мутациях в FGD1 нарушается нормальный цикл обмена гуаниндифосфата на гуанинтрифосфат, что приводит к сбоям в передаче внутриклеточных сигналов, особенно критичных во время эмбриогенеза[2].
Эпидемиология
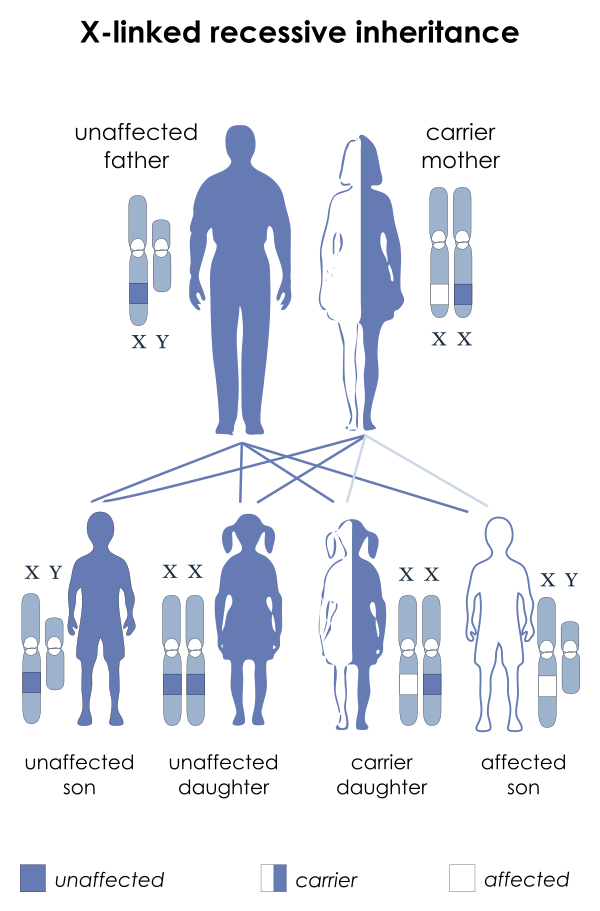
САС представляет собой наследственную патологию с Х-сцепленным рецессивным типом наследования. Заболевание преимущественно проявляется у мужчин, рождённых от матерей — носительниц дефектного гена. У женщин, являющихся носителями мутации, могут отмечаться слабовыраженные симптомы заболевания[2].
САС относится к редким генетическим патологиям с распространенностью 1 случай на 25 000—100 000 новорождённых. В мировой литературе зафиксировано около 250 случаев данного заболевания. Синдром равномерно распределён среди различных этнических и расовых групп, не демонстрируя повышенной частоты встречаемости в каких-либо конкретных популяциях[2].
Диагностика
К основным диагностическим признакам относятся: низкорослость, характерные лицевые аномалии (короткий нос с направленными вперёд ноздрями, гипоплазия верхней челюсти, поперечная складка на нижней губе), лёгкая синдактилия, широкие и короткие ладони, укороченные и искривлённые мизинцы, а также деформация мошонки. Вторичные симптомы включают утолщённые ушные раковины с выраженным наклоном назад, V-образную линию роста волос на лбу, птоз, антимонголоидный разрез глаз, гиперподвижность суставов, широкие стопы, паховые грыжи, гипоспадию и аномалии пупка[4].
Клиническая картина может включать умеренные нарушения интеллектуального развития или признаки гиперактивности с дефицитом внимания[2]
Офтальмологические проявления встречаются редко и чаще всего представлены астигматизмом, страбизмом и близорукостью[3].
Также у пациентов с САС описаны множественные системные нарушения: анатомические аномалии сердечно-сосудистой системы (аортальный стеноз, гипертрофия правого желудочка), нейропсихиатрические проявления (биполярное расстройство, расстройства аутистического спектра, эпилепсия, синдром Аспергера, умственная отсталость), а также патологии опорно-двигательного аппарата (симметричная дистальная артропатия, миопатия, вывих бёдра, гиперрефлексия пальцев и коленных суставов, плоскостопие)[4].
Диагноз САС подтверждается при выявлении мутации в гене FDG1 методом секвенирования[2].
Пренатальная диагностика при повышенном риске заболевания технически возможна, если известна патогенная мутация в конкретной семье (большинство мутаций являются семейно-специфичными). Однако пренатальное тестирование редко бывает востребованным, поскольку клинические проявления часто бывают слабовыраженными, а значительная клиническая гетерогенность затрудняет прогнозирование фенотипа даже внутри одной семьи[5].
Дифференциальная диагностика
Дифференциальная диагностика САС проводится со следующими заболеваниями[4]:
- синдром Робена;
- синдром Опитца;
- синдром Блума;
- синдром Нунан;
- псевдогипопаратиреоз;
- синдром Коффина — Лоури;
- синдром Вильямса;
- синдром Рубинштейна — Тейби;
- синдром Корнелии де Ланге.
Лечение
САС не имеет специфического лечения, так как патологические изменения формируются на этапе внутриутробного развития, однако комплексный симптоматический подход и паллиативные методы позволяют существенно повысить качество жизни пациентов[2].
Хирургическая коррекция показана при выраженных скелетных аномалиях, угрозе компрессии спинного мозга, а также при паховых грыжах и крипторхизме. Раннее начало реабилитационных мероприятий — физиотерапии, лечебной физкультуры — значительно улучшает прогноз и помогает предотвратить развитие вторичных осложнений[2].
Диспансерное наблюдение
Обязательными являются стоматологическое наблюдение с ортодонтической коррекцией аномалий прикуса, вызванных гипоплазией верхней челюсти, и профилактика кариозных поражений. Особое внимание уделяется ортопедическому контролю за формированием скелета, в частности шейного отдела позвоночника и плюсневых костей стопы[2].
Детям с диагнозом САС требуется регулярный мониторинг развития с разработкой индивидуальных коррекционных программ при выявлении когнитивных нарушений, включая специальные образовательные методики при трудностях обучения и медикаментозно-поведенческую терапию при СДВГ[2].
Прогноз
У большинства пациентов прогноз благоприятный. Как правило, с возрастом наблюдается положительная динамика в психоневрологическом статусе, и во взрослом возрасте состояние обычно стабилизируется[5].
Примечания
Литература
- Егоров М. В., Полищук Р. С. Ультраструктурная характеристика аппарата Гольджи при синдроме Аарскога - Скотта // Вестник Ивановской медицинской академии. — 2011. — № 4.