Синдром Файнгольда
Синдром Фа́йнгольда (СФ) представляет собой редкое генетически обусловленное заболевание, проявляющееся комплексом аномалий развития, включающим микроцефалию, множественные деформации пальцев и когнитивные нарушения. Патология манифестирует в пренатальном периоде и требует преимущественно паллиативного и симптоматического лечения. Исход заболевания определяется степенью выраженности врождённых пороков, тяжестью клинических проявлений, наличием осложнений, а также своевременностью диагностических и терапевтических мероприятий. Этиологически выделяют два типа синдрома: 1-й тип, ассоциированный с мутациями гена MYCN, и 2-й тип, связанный с мутациями гена MIR17HG[1].
Общие сведения
История
В 1975 году американский врач Мюррей Файнгольд впервые описал это заболевание, наблюдая семью, где у трёх поколений (бабушки, отца и сына) выявлялись характерные признаки: микроцефалия, аномалии развития конечностей и атрезия двенадцатиперстной кишки. Генетическая основа синдрома была установлена позднее: ген MYCN, ответственный за 1-й тип заболевания, идентифицировали в 1987 году, а ген MIR17HG, ассоциированный со 2-м типом, обнаружили в 2004 году[1][2].
Классификация
Этиология
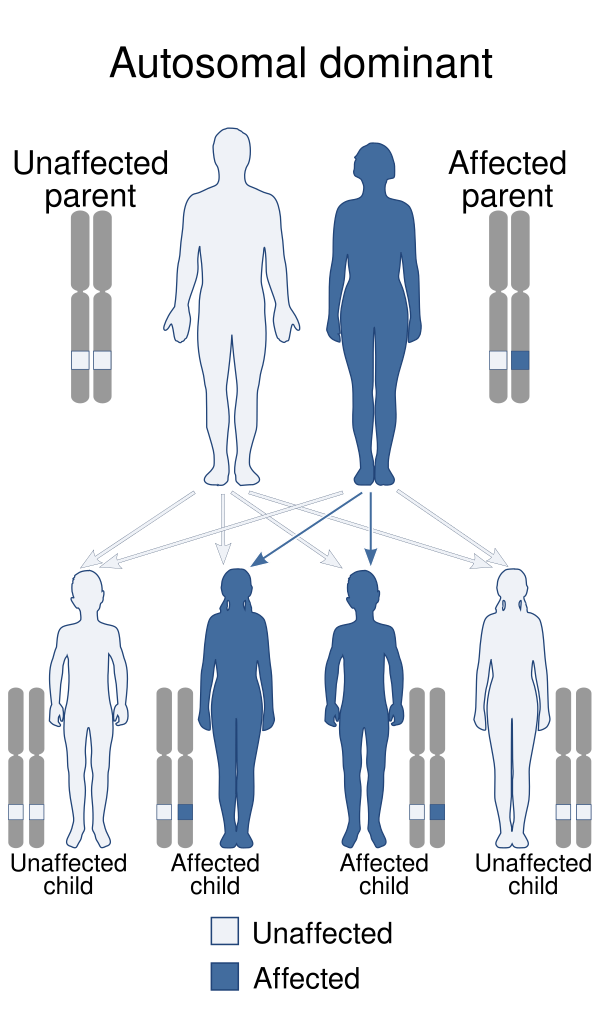
СФ связан с мутациями в генах MYCN и MIR17HG и наследуется по аутосомно-доминантному типу наследования[1].
Патогенез
Ген MYCN кодирует транскрипционный фактор из семейства MYC, критически важный для эмбрионального развития, особенно формирования головного мозга. Ген MIR17HG выступает хозяином для кластера MIR17-92 и продуцирует полицистронную РНК, которая затем процессируется в шесть функциональных микроРНК (MIR17, MIR18, MIR19A, MIR19B, MIR20 и MIR92), регулирующих ключевые клеточные процессы: пролиферацию, дифференцировку, ангиогенез и апоптоз. Мутации в этих генах нарушают нормальное развитие организма, что клинически проявляется характерными для СФ аномалиями — микроцефалией и дефектами формирования конечностей[1].
Эпидемиология
СФ относится к категории крайне редких генетических заболеваний, при этом точные данные о его распространённости в популяции отсутствуют. Наиболее часто встречающейся формой патологии является СФ 1-го типа. В мировой литературе на сегодняшний день зафиксировано лишь около 120 клинических случаев данного заболевания[1].
Диагностика
Клиническая картина
Основными диагностическими признаками являются аномалии пальцев и умеренно выраженная микроцефалия. У большинства пациентов наблюдаются укороченные средние фаланги второго и пятого пальцев. Часто встречаются гипопластичные большие пальцы, их сгибательные контрактуры, ограничение подвижности или гиперэкстензия. Возможны камптодактилия одного или нескольких пальцев, вальгусная деформация локтевого сустава и ограничение разгибания в локте. Характерна синдактилия пальцев стоп, особенно четвёртого и пятого[2].
Микроцефалия обычно врождённая, может прогрессировать после неонатального периода. У части пациентов отмечаются лёгкие когнитивные нарушения или трудности обучения. Разрез глазных щелей часто укорочен, хотя у некоторых больных глаза выглядят нормально[2].
При СФ отмечаются желудочно-кишечные аномалии, включая атрезию пищевода (иногда с трахеопищеводным свищом), атрезию двенадцатиперстной кишки или стеноз (в некоторых случаях вызванные кольцевидной поджелудочной железой), а также единичные случаи множественных атрезий тощей кишки и атрезии ануса[2].
Со стороны сердечно-сосудистой системы встречаются преимущественно аномалии: открытый артериальный проток, атрезия трёхстворчатого клапана, дефект межжелудочковой перегородки, перерыв дуги аорты и открытое овальное окно[2].
Почечные аномалии наблюдаются редко и включают лёгкое расширение почечной лоханки, уменьшенные размеры почек, экстраренальную лоханку, гидронефроз и кистозную дисплазию[2].
Со стороны опорно-двигательного аппарата описаны отсутствие пятого крестцового позвонка, сращение шейных позвонков C5-C7 и наличие 11 пар рёбер[2].
Другие аномалии включают глухоту (одностороннюю полную, двустороннюю потерю слуха на низких частотах или полную двустороннюю глухоту вследствие отсутствия слухового нерва), а также аномалии селезёнки (наличие дополнительных селезёнок или асплению)[2].
Инструментальная диагностика
Рентгенография позволяет выявить характерные изменения скелета[1].
Ультразвуковое исследование органов брюшной полости, сердца и почек также позволяет выявить врождённые пороки развития[1].
Лабораторная диагностика
Проводится путём определения мутаций в генах MYCN и MIR17HG метод секвенирования[1].
Пренатальная диагностика
Пренатальная диагностика проводится методом биопсии ворсин хориона или амниоцентеза с последующим молекулярно-генетическим анализом материала[1].
Дифференциальная диагностика
Дифференциальная диагностика СФ проводится со следующими состояниями[3]:
- VACTERL-ассоциация;
- синдром CHARGE;
- брахидактилия;
- анемия Фанкони.
Лечение
Лечение СФ носит исключительно симптоматический и поддерживающий характер, направленный на коррекцию имеющихся аномалий. Основной подход включает раннее хирургическое вмешательство для устранения врождённых пороков (желудочно-кишечных атрезий, трахеопищеводных свищей, врождённых пороков сердца) с последующей длительной медикаментозной терапией осложнений. При нарушениях слуха показано использование современных цифровых слуховых аппаратов или кохлеарных имплантатов. Обязательными компонентами терапии являются разработка индивидуальных образовательных программ с учётом когнитивных возможностей пациента и создание специальных условий обучения, адаптированных под конкретные потребности больного[1].
Прогноз
Прогноз при СФ зависит от тяжести врождённых пороков развития, особенно сердечных и почечных аномалий. При возможности оптимальной хирургической коррекции прогноз может быть относительно благоприятным, однако у многих пациентов проявления врождённых пороков сохраняются на протяжении всей жизни[3].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Marcelis C.L.M., de Brouwer A.P.M. Feingold Syndrome 1 (англ.) // GeneReviews®. — Seattle (WA): University of Washington, 2009.
- Cognet M., Nougayrede A., Malan V. et al. Dissection of the MYCN locus in Feingold syndrome and isolated oesophageal atresia (англ.) // European Journal of Human Genetics : статья. — 2011. — Vol. 19. — P. 602—606. — doi:10.1038/ejhg.2010.225.