MODY-диабет
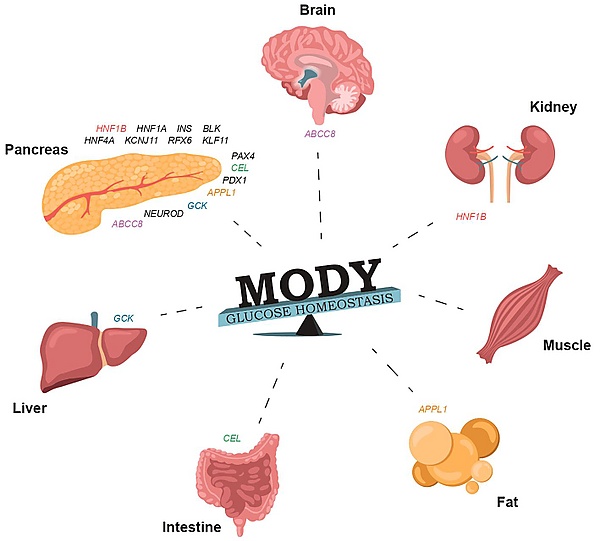
MODY-диабе́т (англ. maturity-onset diabetes of the young, диабе́т зре́лого во́зраста у молоды́х) — наследственная форма моногенного диабета, развивающаяся из-за нарушений углеводного обмена и секреции инсулина. Заболевание дебютирует в молодом возрасте, обычно до 25 лет, и является наиболее распространённой формой наследственного диабета. Различают несколько генетических подтипов MODY-диабета, каждый из которых связан с мутациями в определённых генах: HNF4A, GCK, HNF1A, PDX1, HNF1B, NEUROD1, KLF11, CEL, PAX4, INS, BLK, KCNJ11 и APPL1. Клинические проявления варьируют в зависимости от конкретного генетического подтипа. Лечение включает диету с ограничением легкоусвояемых углеводов, регулярные физические нагрузки, а в некоторых случаях — препараты сульфонилмочевины или инсулинотерапию. Прогноз в большинстве случаев благоприятный и зависит от конкретной формы заболевания. Характерными особенностями MODY-диабета являются аутосомно-доминантный тип наследования и относительно мягкое течение по сравнению с классическими формами сахарного диабета[1].
Общие сведения
История
Заболевание впервые было описано Робертом Таттерсалом в 1974 году. Он исследовал семью, в которой мать 48 лет страдала сахарным диабетом с 12-летнего возраста, а у её двух дочерей болезнь проявилась в 5 и 7 лет. При этом ни мать, ни дочери не нуждались в инсулинотерапии. Кроме того, примерно у половины членов этой семьи наблюдался сахарный диабет 2-го типа. В 1975 году Таттерсал совместно с Стефанией Фаянс предложили для этой формы диабета термин «сахарный диабет взрослого типа у молодых» (англ. maturity onset diabetes of the young, MODY). Длительные наблюдения за пациентами в течение более 20 лет показали, что заболевание имеет стабильное течение и обычно не требует инсулинотерапии — достаточно диеты и приёма пероральных препаратов, таких как сульфонилмочевина[1].
В период с 1981 по 2000 год были идентифицированы гены, ассоциированные с развитием MODY-диабета: HNF4A, GCK, HNF1A, PDX1, HNF1B, NEUROD1, KLF11, CEL, PAX4, INS, BLK, KCNJ11 и APPL1. Эти открытия позволили глубже понять генетическую природу заболевания и его молекулярные механизмы[1].
Классификация
MODY-диабет классифицируют в зависимости от конкретной мутации[2]:
| Подтип MODY | Ответственный ген | Функция гена |
|---|---|---|
| подтип 1 (HNF4A-MODY) | HNF4A (hepatocyte nuclear factor 4 alpha) | Регуляция метаболизма глюкозы и липидов |
| подтип 2 (GCK-MODY) | GCK (глюкокиназа) | Фосфорилирование глюкозы |
| подтип 3 (HNF1A-MODY) | HNF1A (hepatocyte nuclear factor 1 alpha) | Регуляция экспрессии инсулина и транспортёров глюкозы |
| подтип 4 (PDX1-MODY) | PDX1 (панкреатический дуоденальный гомеобокс 1) | Контроль развития поджелудочной железы |
| подтип 5 (HNF1B-MODY) | HNF1B (hepatocyte nuclear factor 1 beta) | Регуляция органогенеза |
| подтип 6 (NEUROD1-MODY) | NEUROD1 (нейрогенный дифференцировочный фактор 1) | Дифференцировка β-клеток |
| подтип 7 (KLF11-MODY) | KLF11 (Krüppel-like factor 11) | Антиоксидантная защита β-клеток |
| подтип 8 (CEL-MODY) | CEL (карбоксил-эстераза липаза) | Липидный обмен |
| подтип 9 (PAX4-MODY) | PAX4 (paired box 4) | Дифференцировка β-клеток |
| подтип 10 (INS-MODY) | INS (инсулин) | Синтез проинсулина |
| подтип 11 (BLK-MODY) | BLK (B-лимфоцитарная киназа) | Регуляция секреции инсулина |
| подтип 12 (ABCC8-MODY) | ABCC8 (SUR1, субъединица KАТФ-канала) | Регуляция секреции инсулина |
| подтип 13 (KCNJ11-MODY) | KCNJ11 (Kir6.2, субъединица KАТФ-канала) | Регуляция секреции инсулина |
| подтип 14 (APPL1-MODY) | APPL1 (адапторный белок инсулинового сигналинга) | Передача инсулинового сигнала |
Генетическая ориентированная классификация предполагает, что MODY-диабет представляет собой единое заболевание, несмотря на очевидные различия в клинических проявлениях, генетике и патофизиологии между 14 известными подтипами. В связи с этим MODY-диабет разделён на пять категорий в соответствии с их молекулярными механизмами развития[2]:
- нарушения транскрипционных факторов (типы 1, 3—7, 9) — мутации в генах, регулирующих работу β-клеток;
- ферментопатии (подтип 2) — дефект глюкокиназы, ключевого фермента метаболизма глюкозы;
- нарушения фолдинга белков (типы 8, 10) — неправильное сворачивание белков приводит к гибели β-клеток;
- нарушения функции ионных каналов (типы 12—13) — нарушение работы каналов, регулирующих секрецию инсулина;
- нарушения сигнальных путей (подтип 14) — дефект передачи инсулинового сигнала.
Этиология
MODY-диабет представляет собой редкую форму сахарного диабета с аутосомно-доминантным типом наследования. Это заболевание развивается вследствие мутаций в различных генах, влияющих на работу поджелудочной железы и выработку инсулина. Выделяют 14 молекулярно-генетических подтипов MODY-диабета, каждый из которых связан с мутацией в конкретном гене и имеет свои клинические особенности[2][3].
Патогенез
Патогенез конкретного типа MODY-диабета связан с мутацией в определённом гене[2]:
- 1-й подтип — связан с мутацией в гене HNF4A, кодирующем ядерный фактор гепатоцитов 4-альфа, который экспрессируется в печени, клетках островков поджелудочной железы и почках. Белок HNF4A относится к суперсемейству стероидных гормональных рецепторов и регулирует экспрессию гена HNF1A, печёночный глюконеогенез и биосинтез липопротеинов. Гетерозиготные мутации в этом гене приводят к дисфункции β-клеток поджелудочной железы, нарушению глюкозозависимой секреции инсулина, повышению уровня липопротеинов низкой плотности и снижению липопротеинов высокой плотности и триглицеридов;
- 2-й подтип — связано с мутацией в гене GCK, кодирующем глюкокиназу, которая экспрессируется в печени и β-клетках поджелудочной железы, где катализирует ключевую реакцию метаболизма глюкозы — АТФ-зависимое фосфорилирование глюкозы с образованием глюкозо-6-фосфата. Гетерозиготные мутации в этом гене приводят либо к снижению ферментативной активности глюкокиназы, либо к нарушению правильного сворачивания белка, что вызывает его агрегацию и деградацию. Эти молекулярные дефекты проявляются в виде нарушения «глюкозного сенсора» в β-клетках, повышения порога глюкозостимулированной секреции инсулина и нарушения постпрандиального накопления гликогена в печени;
- 3-й подтип — связан с мутацией в гене HNF1A, кодирующем ядерный фактор гепатоцитов 1-альфа, который экспрессируется в печени, поджелудочной железе, почках и кишечнике. Кодируемый этим геном белок относится к суперсемейству гомеодомен-содержащих ядерных транскрипционных факторов и регулирует экспрессию генов, кодирующих инсулин, транспортёры глюкозы (GLUT1 и GLUT2), а также натрий-глюкозный котранспортер 2-го типа (SGLT2). Гетерозиготные мутации в гене HNF1A приводят к прогрессирующей дисфункции бета-клеток, снижению глюкозостимулированной секреции инсулина и понижению почечного порога для глюкозы;
- 4-й подтип — связан с мутацией в гене PDX1. Белок PDX1 (панкреатический/дуоденальный гомеобокс 1), также известный как IPF1 (фактор промотора инсулина 1), представляет собой ядерный транскрипционный фактор, играющий ключевую роль в развитии поджелудочной железы и функционировании β-клеток. Он активирует экспрессию генов, кодирующих глюкагон, инсулин, транспортёр глюкозы GLUT2 и фермент глюкокиназу. Гетерозиготные мутации в гене PDX1 приводят к нарушению функции β-клеток и секреции инсулина;
- 5-й подтип — связан с мутацией в гене HNF1B, кодирующем фактор гепатоцитов 1-бета, также известный как TCF2 (транскрипционный фактор 2), относится к семейству ядерных транскрипционных факторов, содержащих гомеодомен, и играет ключевую роль в формировании поджелудочной железы, печени, мочеполовой системы, почек, кишечника и лёгких, в связи с чем для этого типа характерны аномалии развития. Гетерозиготные мутации в гене HNF1B приводят к комплексу патологических изменений, включающих дисфункцию β-клеток поджелудочной железы, развитие инсулинорезистентности и формирование характерного синдрома почечных кист в сочетании с диабетом (RCAD-синдром);
- 6-й подтип — вызван мутациями в гене NEUROD1, который экспрессируется в клетках поджелудочной железы и нейронах, кодируя белок, который относится к классу основных спираль-петля-спираль транскрипционных факторов. Этот белок регулирует экспрессию гена инсулина, а также участвует в морфогенезе островков поджелудочной железы и развитии нервной системы. Гетерозиготные мутации в гене NEUROD1 приводят к нарушению функции β-клеток поджелудочной железы;
- 7-й подтип — вызывается мутациями в гене KLF11 (Krüppel-подобный фактор 11), который экспрессируется в панкреатических островках, где регулирует активность антиоксидантных ферментов (каталаза 1 и супероксиддисмутаза 2). Белок KLF11 представляет собой цинк-содержащий ядерный транскрипционный фактор, который контролирует функцию β-клеток, выступая в качестве глюкозозависимого регулятора экспрессии генов инсулина и PDX1. Гетерозиготные мутации в гене KLF11 приводят к нарушению работы β-клеток и снижению секреции инсулина;
- 8-й подтип — связан с мутациями в гене CEL, который экспрессируется в ацинарных клетках экзокринной части поджелудочной железы, где кодирует важный пищеварительный фермент, зависимый от жёлчных солей. Этот фермент является компонентом панкреатического сока и играет ключевую роль в процессе переваривания жиров, осуществляя гидролиз эфиров холестерина и жирорастворимых витаминов в тонком кишечнике. Гетерозиготные мутации в гене CEL приводят к серьёзным структурным нарушениям молекулы фермента — неправильному сворачиванию (мисфолдингу), образованию агрегатов и развитию цитотоксического эффекта. Эти патологические изменения вызывают комплекс тяжёлых последствий: раннюю атрофию поджелудочной железы, развитие экзокринной недостаточности, липоматоз поджелудочной железы и эндокринную дисфункцию;
- 9-й подтип — ассоциирован с мутации в гене PAX4. Белок PAX4, кодируемый этим геном, представляет собой ядерный транскрипционный фактор, играющий ключевую роль в дифференцировке β-клеток поджелудочной железы. Он регулирует их развитие и функционирование, подавляя активность промоторов генов инсулина и глюкагона. Гетерозиготные мутации в гене PAX4 приводят к нарушениям нормального развития β-клеток, что проявляется их дисфункцией и снижением глюкозозависимой секреции инсулина. Клинически это выражается развитием сахарного диабета, характеризующегося склонностью к кетоацидозу;
- 10-й подтип — развивается вследствие гетерозиготных мутаций в гене INS, который кодирует молекулу препроинсулина — биологически неактивного предшественника инсулина. Эти генетические дефекты вызывают серьёзные нарушения пространственной структуры проинсулина, приводя к трём ключевым патологическим процессам: во-первых, происходит аномальное накопление неправильно свёрнутого проинсулина внутри клеток; во-вторых, нарушается нормальное функционирование сигнального пути NF-kappa B; в-третьих, возникает сбой в процессе биосинтеза инсулина. Все это провоцирует апоптоз инсулин-продуцирующих β-клеток поджелудочной железы;
- 11-й подтип — вызван мутациями в гене BLK, кодирующем B-лимфоцитарную тирозинкиназу, который относится к семейству протоонкогенов SRC, проявляет специфическую экспрессию преимущественно в B-лимфоцитах и β-клетках поджелудочной железы. Кодируемый этим геном белок выполняет критически важную функцию в процессах биосинтеза и секреции инсулина, осуществляя регуляцию через усиление активности ключевых транскрипционных факторов PDX1 и NKX6.1, которые, в свою очередь, контролируют процессы развития и функциональной активности β-клеток. Гетерозиготные мутации в гене BLK приводят к значительному снижению его экспрессии или нарушению функциональной активности, что вызывает каскад патологических изменений: во-первых, развивается дефицит транскрипционных факторов PDX1 и NKX6.1; во-вторых, происходит нарушение глюкозозависимой секреции инсулина; и в-третьих, наблюдается прогрессирующее уменьшение количества β-клеток поджелудочной железы;
- 12-й подтип — ассоциирован с мутацией в гене ABCC8, который активно экспрессируется в клетках поджелудочной железы, отвечает за кодирование важного белка — SUR1 субъединицы АТФ-зависимых калиевых каналов. Эти специализированные каналы расположены на поверхности β-клеток поджелудочной железы и выполняют критически важную функцию в процессе регуляции секреции инсулина. Их работа представляет собой сложный механизм, который напрямую связывает концентрацию глюкозы в крови и уровень внутриклеточного АТФ с изменениями электрической активности мембраны β-клеток. Когда возникают гетерозиготные мутации в гене ABCC8, это приводит к серьёзным нарушениям в работе калиевых каналов. Эти нарушения приводят к развитию сахарного диабета;
- 13-й подтип — вызван мутациями в гене KCNJ11, активно экспрессирующемся в поджелудочной железе, кодирует субъединицу Kir6.2 АТФ-чувствительного калиевого канала. Гетерозиготные мутации в этом гене нарушают нормальную работу калиевого канала, что приводит к дефектам глюкозозависимой секреции инсулина;
- 14-й подтип — ассоциирован с мутациями в гене APPL1, активно экспрессируется в скелетных мышцах, поджелудочной железе, печени и жировой ткани. Белок APPL1 играет ключевую роль в передаче инсулинового сигнала внутри клетки, взаимодействуя с основными компонентами инсулинового каскада (серин-треониновую киназа 2, субстраты инсулинового рецептора IRS-1 и IRS-2, а также непосредственно сам инсулиновый рецептор). Помимо этого, APPL1 регулирует инсулин-стимулированный захват глюкозы в скелетных мышцах и жировой ткани. Гетерозиготные мутации с потерей функции в этом гене приводят к двум основным нарушениям: дефектной глюкозозависимой секреции инсулина и снижению выживаемости β-клеток поджелудочной железы.
Эпидемиология
Общая распространённость MODY-диабета, согласно данным преимущественно европейских исследований, оценивается в 1—5 случаев на 10 000 человек, что составляет 1—5 % от всех случаев сахарного диабета. Имеющиеся данные указывают на вариабельность распространённости MODY-диабета в зависимости от страны. По возрастным группам распространённость MODY-диабет оценивается как 1 случай на 10 000 среди взрослого населения и 1 на 23 000 среди детей. Среди всех типов MODY-диабета особое место занимает 3-й тип, который является одним из наиболее распространённых вариантов — по данным различных исследований, его доля среди всех форм MODY-диабета составляет от 31 до 62 %. В российской популяции детей с MODY-диабетом этот подтип занимает второе место по частоте встречаемости после 2-го типа[2][3].
Диагностика
Каждая форма MODY-диабета имеет свои клинические особенности в зависимости от генетической природы[1]:
- 1-й тип: заболевание может дебютировать уже в 7—9 лет, протекает как классический сахарный диабет и часто сопровождается микроангиопатическими осложнениями, связанными с поражением мелких сосудов;
- 2-й подтип отличается бессимптомным течением с умеренно повышенной концентрацией глюкозы натощак. Эта форма может проявляться уже на первом году жизни;
- 3-й подтип имеет более позднее начало, но отличается быстрым прогрессированием и выраженной гипергликемией. Для этой формы характерно тяжёлое течение с частым развитием диабетических осложнений, особенно ретинопатии;
- 4-й подтип проявляется в более позднем возрасте (17—60 лет и старше) и сопровождается развитием микро- и макрососудистых осложнений. Особенностями этой формы являются агенезия поджелудочной железы и выраженный синдром мальабсорбции;
- 5-й подтип — одна из наиболее тяжёлых форм, сочетающаяся с поликистозом почек. Дополнительные проявления включают аномалии развития половых органов, подагру, гиперурикемию и нарушения развития желудочно-кишечного тракта. Возможен диабетический кетоацидоз. Обычно проявляется после 10 лет;
- 6-й подтип ассоциирован с повышенным риском колоректального рака и полипоза различных отделов желудочно-кишечного тракта, протекает как тяжёлая форма диабета;
- 8-й подтип характеризуется прогрессирующей дисфункцией поджелудочной железы и образованием кист в её ткани;
- Типы 7, 9, 10, 11, 12, 13, 14 имеют раннее начало, но не обладают специфическими клиническими особенностями.
Биохимический анализ крови: характерно повышение концентрации глюкозы крови[4].
Биохимический анализ мочи: характерна глюкозурия[3].
Молекулярно-генетический анализ: характерно выявление мутаций в одном из генов (HNF4A, GCK, HNF1A, PDX1, HNF1B, NEUROD1, KLF11, CEL, PAX4, INS, BLK, ABCC8, KCNJ11, APPL1) методом секвенирования[1].
Характерно повышение концентрации гиликированного гемоглобина крови, выявляемое методом жидкостной хроматографии[5].
Учитывая высокую стоимость и длительность проведения генетического анализа, разработаны показания для генетического тестирования, которые включают[5]:
- Наличие отягощённого семейного анамнеза по диабету, манифестировавшему в возрасте от 20 до 50 лет.
- Нормальная или низкая масса тела.
- Отсутствие аутоантител.
- Наличие клинические признаков, нехарактерных для сахарного диабета 1-го и 2-го типа:
- низкий почечный порог для глюкозы;
- выраженное повышение концентрации глюкозы при проведении глюкозотолерантного теста;
- низкая концентрация С-реактивного белка.
- Пониженная концентрация липропротеинов высокой плотности.
- Высокая чувствительность к терапии инсулином.
- Наличие диагноза сахарного диабета 1-го типа, но:
- при отсутствии аутоантител в крови;
- с охраняющейся повышенной концентрацией С-пептида.
Дифференциальная диагностика
Дифференциальная диагностика диабета MODY-диабета проводится со следующими состояниями[5]:
Осложнения
Вероятность развития и тяжесть осложнения при диабете MODY связаны с конкретным типом диабета[5]:
- подтип 1: у пациентов могут развиваться сосудистые осложнения. Поскольку HNF4A экспрессируется в печени, возможна гиперлипидемия и развитие метаболического синдрома;
- подтип 3: связан с высоким риском сердечно-сосудистых осложнений;
- подтип 4: этот редкий подптип ассоциирован с агенезией поджелудочной железы, неонатальным диабетом и экзокринной недостаточностью;
- подтип 5: помимо диабета, у пациентов наблюдаются врождённые аномалии мочеполовой системы (двурогая матка, синдром Рокитанского, агенезия семявыносящего протока и гипоспадия). Также возможны гипомагниемия (из-за почечных потерь), гиперурикемическая нефропатия с подагрой и первичный гиперпаратиреоз. Другие осложнения включают атрофию поджелудочной железы, умственную отсталость и аутизм;
- подтип 6: гетерозиготные мутации вызывают диабет у детей, неврологические нарушения и задержку развития.
Лечение
Большинству пациентов с MODY-диабетом рекомендуется соблюдение диеты с ограничением простых углеводов в сочетании с регулярной физической активностью. Если эти меры не обеспечивают достаточного контроля уровня глюкозы (при показателях гликированного гемоглобина выше 7 %), рассматривается возможность медикаментозной терапии — назначения препаратов сульфонилмочевины или перехода на инсулинотерапию. Выбор конкретного метода лечения зависит от типа MODY-диабета, степени компенсации углеводного обмена и индивидуальных особенностей пациента[1].
Перспективным направлением является генная терапия с использованием аденоассоциированных вирусных векторов. Эти векторы безопасны, обладают низкой иммуногенностью и обеспечивают длительную экспрессию терапевтических генов[6].
Прогноз
Прогноз течения MODY-диабета в значительной степени определяется конкретным генетическим подтипом заболевания, однако в большинстве случаев характеризуется благоприятным течением при условии своевременной диагностики и адекватного контроля гликемии. Следует отметить, что различные формы MODY-диабета демонстрируют существенные различия в скорости прогрессирования, риске развития осложнений и ответе на терапию, что обусловлено особенностями лежащих в их основе молекулярно-генетических механизмов. Наиболее благоприятный прогноз характерен для 2-го типа MODY-диабета[1].
Диспансерное наблюдение
Пациенты с MODY-диабетом нуждаются в наблюдении эндокринолога, диабетолога, врача-генетика, диетолога, офтальмолога, нефролога, а в отдельных случаях — гинеколога (при 5-м типе, учитывая аномалии развития мочеполовых путей) и кардиолога[5].
Профилактика
Не разработана.
Примечания
Литература
- Зубкова Н. А., Арбатская Н. Ю., Петряйкина Е. Е., Малиевский О. А., Тюльпаков А. Н. Сахарный диабет типа MODY3: клиническая и молекулярно-генетическая характеристика 9 случаев заболевания. — 2014. — Т. 60, № 1. — С. 51—56. — doi:10.14341/probl201460151-56.
- Ellard S., Bellanné-Chantelot C., Hattersley A.T. Best practice guidelines for the molecular genetic diagnosis of maturity-onset diabetes of the young. — 2008. — Т. 51, № 4. — С. 546—553. — doi:10.1007/s00125-008-0942-y. — PMID 18297260.