Факторы транскрипции
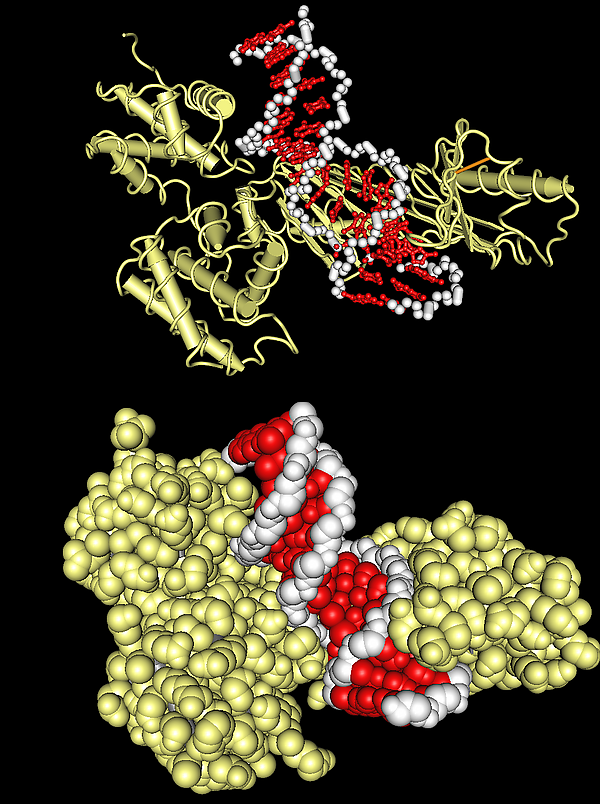
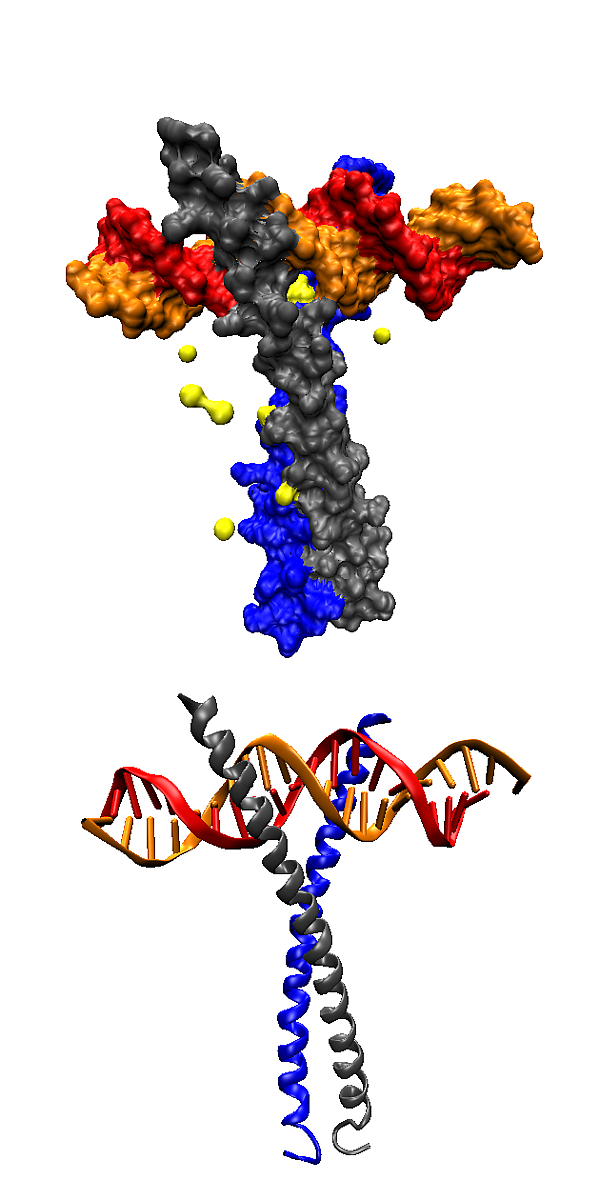
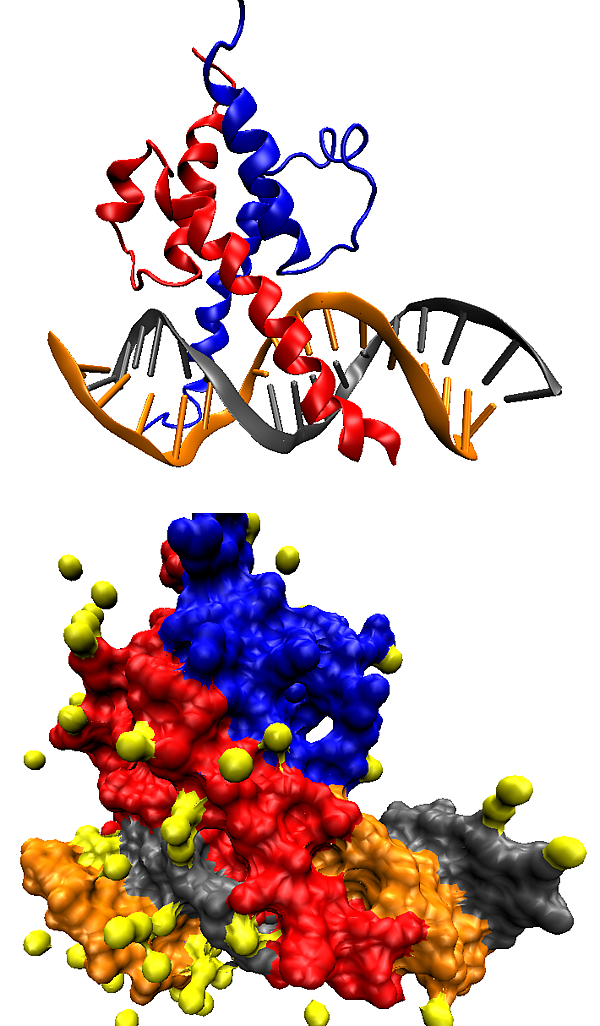
Факторы транскрипции (транскрипционные факторы) — белки́, контролирующие процесс синтеза мРНК, а также других видов РНК [1] на матрице ДНК (транскрипцию) путём связывания со специфичными участками ДНК[2][3]. Транскрипционные факторы выполняют свою функцию либо самостоятельно, либо в комплексе с другими белками. Они обеспечивают снижение (репрессоры) или повышение (активаторы) константы связывания РНК-полимеразы с регуляторными последовательностями регулируемого гена[4][5][6].
Определяющая черта факторов транскрипции — наличие в их составе одного или более ДНК-связывающих доменов, которые взаимодействуют с характерными участками ДНК, расположенными в регуляторных областях генов. Другие белки, играющие ключевую роль в регуляции экспрессии генов, такие как коактиваторы, гистонацетилазы, киназы, метилазы, не имеют ДНК-связывающих доменов, и, следовательно, не могут быть причислены к транскрипционным факторам[7][8][9].
Консервативность у различных организмов
Факторы транскрипции необходимы для регуляции экспрессии генов и обнаружены у всех живых организмов. Их количество, как абсолютное, так и удельное, возрастает с ростом размера генома[10].
В геноме человека обнаружено более 2600 белков, имеющих ДНК-связывающий домен, и большинство из них предположительно являются факторами транскрипции[11]. Следовательно, около 10 % всех генов в геноме кодируют транскрипционные факторы. Таким образом, они являются самым большим семейством белков человека[12]. Более того, активность многих генов регулируется корпоративным взаимодействием большого числа различных факторов транскрипции, что позволяет обеспечить каждому из генов уникальный способ регуляции в процессе развития организма[9].
Функции
Факторы транскрипции — одна из групп белков, обеспечивающих прочтение и интерпретацию генетической информации. Они связывают ДНК и способствуют инициации программы повышения или понижения транскрипции гена. Таким образом, они жизненно необходимы для нормального функционирования организма на всех уровнях. Ниже перечислены важнейшие из процессов, в которые вовлечены факторы транскрипции.
Фоновая транскрипционная активность обеспечивается набором ТФ, общим для всех генов. Важный класс эукариотических факторов транскрипции — GTFs (general transcription factors)[13][14]. Многие из его представителей не связывают ДНК непосредственно, а входят в состав комплекса инициации транскрипции (преинициирующего комплекса), который напрямую взаимодействует с РНК-полимеразой. Наиболее распространенными GTF являются TFIIA, TFIIB, TFIID (связываются с т. н. ТАТА-боксом (элементом промотора)), TFIIE, TFIIF, и TFIIH[15].
Помимо ТФ, необходимых для экспрессии всех генов, существуют также специфичные факторы транскрипции, обеспечивающие включение/выключение определённых генов в нужный момент.
Многие ТФ многоклеточных организмов вовлечены в обеспечение их развития[16]. Действуя в соответствии с генетической программой и/или в ответ на внешние воздействия, они инициируют или подавляют транскрипцию определённых генов, что влечет за собой изменения в клеточной морфологии, клеточную дифференциацию, морфогенез, органогенез и т. д. Например, семейство гомеобоксных ТФ критично для формирования правильной морфологии тела у организмов от дрозофилы до человека[17][18]. Мутации генов этих белков (гомеозисные мутации) у дрозофил приводят к серьёзным нарушениям в дифференцировке сегментов тела данных насекомых (например, развитие ног вместо усиков).
Другой пример данной группы ТФ — продукт гена полопределяющего региона Y (SRY, Sex-determining Region Y), который играет важную роль в детерминации пола человека.[19]
Согласованная регуляция взаимодействия клеток многоклеточного организма осуществляется путём высвобождения специальных молекул (гормонов, цитокинов и т. п.), которые вызывают сигнальный каскад в клетках-мишенях. В случае, если сигнал вызывает изменение уровня экспрессии определённых генов, конечным звеном каскада часто оказываются ТФ[20]. Эстрогеновый сигнальный путь — пример короткого каскада, включающего транскрипционный фактор рецептора эстрогена: эстроген секретируется тканями плаценты и яичника, преодолевает плазматическую мембрану реципиентных клеток, и связывается со своим рецептором в цитоплазме. Рецептор эстрогена проникает в ядро и связывает специфичный участок ДНК, изменяя регуляции транскрипции соответствующего гена[21].
ТФ — не единственные конечные звенья сигнальных каскадов, возникающих в ответ на различные внешние стимулы, но они тоже могут быть эффекторами в сигнальных каскадах, индуцируемых воздействием окружающей среды. Например, фактор теплового шока (HSF) активирует гены белков теплового шока, которые обеспечивают выживание при повышении температуры (например, шапероны)[22], фактор, индуцируемый гипоксией (HIF) — при снижении концентрации кислорода[23]; белок SREBP (sterol regulatory element binding protein) помогает поддерживать необходимое содержание липидов в клетках[24].
Многие ТФ, особенно онкогены и онкосупрессоры, участвуют в регуляции клеточного цикла. Они определяют переход от одной фазы клеточного цикла к другой, частоту делений и интенсивность роста. Один из наиболее известных подобных ТФ — онкоген Myc, играющий важную роль в росте клеток и направлении их в апоптоз.
Регуляция
Все общебиологические процессы имеют многоуровневую регуляцию и контроль. Это верно и для ТФ — ТФ не только обеспечивают регуляцию уровня накопления белков и РНК в клетке, но и регулируют активность собственных генов (часто с помощью других ТФ). Ниже кратко описаны основные способы регуляции активности ТФ.
Уровень накопления ТФ в клетке регулируется по той же схеме, что и у других белков за счет контроля транскрипции, деградации мРНК, трансляции, постпроцессинга белка, его внутриклеточной локализации и деградации. Возможна саморегуляция по принципу отрицательной обратной связи — ТФ репрессирует активность кодирующего его гена.
У эукариотических организмов процессы транскрипции и трансляции пространственно разделены — они происходят в ядре и цитоплазме соответственно. После синтеза ТФ должны проникнуть в ядро, преодолев двойную мембрану. Многие белки, функционирующие в ядре, имеют сигнал ядерной локализации — специфичный участок полипептидной цепи, адресующий белок в ядро. Для многих ТФ транслокация является ключевым фактором в регуляции их активности[25]. Важные классы ТФ, такие как некоторые ядерные рецепторы, должны сперва связать эндогенный лиганд-агонист в цитоплазме и только потом транспортироваться в ядро[25].
ТФ могут быть активированы/деактивированны путём воздействия на их сигнал-чувствительный домен различным образом:
- связывание лиганда — необходимой для функционирования субстанции, не входящий в состав полипептида (например, ионов Zn2+)
- фосфорилирование[26][27] — многие ТФ должны быть фосфорилированы для получения возможности связывать ДНК.
- взаимодействие с другими ТФ и/или корегуляторными белками.
У эукариот гены, не транскрибируемые постоянно, часто находятся в гетерохроматине (участках ДНК, плотно упакованных за счет связывания гистонов и организованных в компактные хроматиновые фибриллы). ДНК в составе гетерохроматина недоступна для многих факторов транскрипции. Для того, чтобы ТФ могли связаться с ДНК, гетерохроматин должен быть трансформирован в эухроматин, обычно путём модификаций гистонов. Также для связывания ТФ с ДНК важную роль играет свобода хроматина от нуклеосом. Хроматин свободный от нуклеосом называется открытым хроматином и значительно чаще связывает факторы транскрипции, чем связанный с нуклеосомами хроматин. Перераспределение нуклеосом осуществляют факторы ремоделирования хроматина. Сайт связывания ТФ на ДНК может быть недоступным и в случае, если он связан другим фактором транскрипции. Пары факторов транскрипции могут играть антагонистическую роль (активатор — репрессор) при регуляции активности одного гена.
Большинство ТФ не работают в одиночку. Часто для активации транскрипции гена с его регуляторными элементами должно связаться большое количество ТФ. Связывании ТФ вызывает привлечение промежуточных белков, таких как кофакторы, что приводит к сборке преинициационного комплекса и посадке на промотор РНК-полимеразы.
Структура
ТФ являются модульными по структуре и содержат следующие домены[2]:
- ДНК-связывающий домен (DBD) — взаимодействует со специфичными последовательностями ДНК, характерными для промоторов и энхансеров. Специфичность распознавания определённых последовательностей определяет набор генов, подверженных регуляции данным ТФ;
- трансактивирующий домен (TAD) — содержит участки связывания других белков, например, транскрипционных корегуляторов[28];
- сигналраспознающий домен (SSD) (например, лиганд-связывающий домен), который чувствителен к внешнем сигналам и отвечающим за передачу сигнала к другим компонентам транскрипционного комплекса, что вызывает повышение или понижение уровня экспрессии.
Структурно-функциональная единица (домен) факторов транскрипции, связывающая ДНК, называется ДНК-связывающим доменом. Ниже приведен список важнейших семейств ДНК-связывающих доменов/ТФ:
| Семейство | NCBI conserved domains | База данных структурной классификации белков (SCOP) | База данных InterPro |
|---|---|---|---|
| Спираль-петля-спираль (helix-loop-helix)[29] | cl00228 | 47460 | IPR001092 |
| Лейциновая молния[30] | cl02576 | 57959 | IPR004827 |
| C-концевые эффекторные домены составных регуляторов ответа | 46894 | IPR001789 | |
| GCC box | cl00033 | 54175 | |
| Спираль-поворот-спираль (helix-turn-helix)[31] | cl02600 | ||
| Гомеодоменные белки — связывают гомеобокс (особый участок ДНК). Играют критическую роль в индивидуальном развитии организмов (онтогенезе).[32] | cd00086 | 46689 | IPR009057 |
| Подобные репрессору фага лямбда | 47413 | IPR010982 | |
| srf-подобные | cl00109 | 55455 | IPR002100 |
| Парный бокс[33] | cl09102 | ||
| winged helix | 46785 | IPR011991 | |
| Цинковые пальцы[34] | |||
| * многодоменные цинковые пальцы типа Cys2His2[35] | pfam00096 | 57667 | IPR007087 |
| * Zn2/Cys6 | 57701 | ||
| * цинковые пальцы типа Zn2/Cys8 ядерных рецепторов гормонов | pfam00105 | 57716 | IPR001628 |
Участки ДНК, которые взаимодействуют с факторами транскрипции, называются сайтами связывания ТФ. Взаимодействие осуществляется за счет электростатических сил, водородных связей и сил Ван-дер-Ваальса. За счет корпоративного, стерически детерминированного действия данных сил, которое определяется пространственной структурой белковой молекулы, ТФ связываться только с определёнными участками ДНК. Не все нуклеотидные основания в ДНК, входящие в сайт связывания ТФ, имеют одинаковую значимость при взаимодействии с белком. Вследствие этого, ТФ обычно связывают не участок со строго определённой первичной структурой, а группу структур с близким сходством, каждую — с разной степенью сродства. Например, хотя консенсусной последовательностью сайта связывания ТАТА-связывающих белков является ТАТАААА, они могут взаимодействовать также с ТАТАТАТ и ТАТАТАА.
Вследствие того, что ТФ взаимодействуют с короткими участками ДНК гетерогенной структуры, потенциальные сайты связывания ТФ могут возникать случайно в достаточно протяженной молекуле ДНК. Маловероятно, однако, что ТФ взаимодействуют со всеми подходящими элементами в геноме.
Различные ограничения, такие как доступность сайтов и наличие кофакторов, могут способствовать направлению ТФ в нужные участки ДНК. Таким образом, затруднительно на основании последовательности генома достоверно предсказать реальное место посадки ТФ на ДНК in vivo. Дополнительная специфичность ТФ может опосредоваться наличием нескольких ДНК связывающих доменов в составе одного белка, которые взаимодействуют с двумя или более смежными последовательностями одновременно.
Клинические аспекты
В связи с ключевой ролью ТФ в процессе реализации наследственной информации, некоторые заболевания человека могут быть вызваны мутациями в генах ТФ. Ниже приведены некоторые наиболее изученные нарушения подобного рода:
- Синдром Ретта. Мутации в гене ТФ MECP2 ассоциированы с синдромом Ретта, нарушением в развитии нервной системы[36].
- Диабеты. Редкая форма диабета, называемая MODY (Maturity onset diabetes of the young) может быть обусловлена мутациями в генах некоторых ТФ[37].
- Developmental verbal dyspraxia. (нарушение речевых функций). Мутации в гене ТФ FOXP2 ассоциированы с развитием данного заболевания, при котором человек не может производить координированных движений, необходимых для речевой функции[38][39].
- Аутоиммунные заболевания. Мутации в гене ТФ FOXP3 связаны с аутоиммунным заболеванием IPEX (immune dysregulation polyendocrinopathy enteropathy X-linked syndrome)[39].
- Рак. Многие факторы транскрипции являются онкогенами или онкосупрессорами, и их мутации или неправильная регуляция могут приводить к развитию рака. Например, синдром Li-Fraumeni обусловлен мутациями в гене онкосупрессора p53[40].
Классификация
ТФ могут классифицироваться по (1) механизму действия, (2) регуляторной функции, (3) структуре ДНК-связывающего домена, а также на натуральные и (5)искусственные.
По данному признаку выделяют три класса ТФ:
- Главные факторы транскрипции (GTFs), вовлеченные в образование инициационного комплекса. Наиболее важные из них — TFIIA, TFIIB, TFIID, TFIIE, TFIIF, и TFIIH. Они присутствуют во всех клетках и взаимодействуют с кором промотора генов, транскрибируемых РНК-полимеразой второго класса.
- ТФ, взаимодействующие с upstream-участками ДНК, (областями, расположенными до промотора, лежащими относительно него с другой стороны от кодирующей области гена).
- Индуцируемые ТФ сходны с предыдущим классом, но требуют активации либо ингибирования.
- Конститутивные — присутствуют всегда во всех клетках — главные факторы транскрипции, Sp1, NF1, CCAAT.
- Активируемые (активны в определённых условиях)
- Участвующие в развитии организма (клетко-специфичные) — экспрессия строго контролируется, но, начав экспрессироваться, не требуют дополнительной активации — GATA, HNF, PIT-1, MyoD, Myf5, Hox, Winged Helix.
- Сигнал-зависимые — требуют внешнего сигнала для активации
Факторы транскрипции классифицируют на основании сходства первичной структуры (что предполагает и сходство третичной структуры) ДНК-связывающих доменов[41][42][43].
- 1 Надкласс: Basic Domains (Basic-helix-loop-helix)
- 1.1 Класс: Лейциновая молния (bZIP)
- 1.2 Класс: Спираль-петля-спираль (bHLH)
- 1.2.1 Семейство: Ubiquitous (Класс A) factors
- 1.2.2 Семейство: Myogenic transcription factors (MyoD)
- 1.2.3 Семейство: Achaete-Scute
- 1.2.4 Семейство: Tal/Twist/Atonal/Hen
- 1.3 Класс: Спираль-петля-спираль / лейциновая молния factors (bHLH-ZIP)
- 1.4 Класс: NF-1
- 1.4.1 Семейство: NF-1 (NFIC)
- 1.5 Класс: RF-X
- 1.6 Класс: bHSH
- 2 Надкласс: Zinc-coordinating DNA-binding domains
- 2.1 Класс: Cys4 zinc finger of nuclear receptor type
- 2.1.1 Семейство: Steroid hormone receptors
- 2.1.2 Семейство: Thyroid hormone receptor-like factors
- 2.2 Класс: diverse Cys4 zinc fingers
- 2.2.1 Семейство: GATA-Factors
- 2.3 Класс: Cys2His2 zinc finger domain
- 2.4 Класс: Cys6 cysteine-zinc cluster
- 2.5 Класс: Zinc fingers of alternating composition
- 2.1 Класс: Cys4 zinc finger of nuclear receptor type
- 3 Надкласс: Спираль-поворот-спираль
- 3.1 Класс: Гомеодомен
- 3.1.1 Семейство: Homeo domain only; includes Ubx
- 3.1.2 Семейство: POU domain factors; includes Oct
- 3.1.3 Семейство: Homeo domain with LIM region
- 3.1.4 Семейство: homeo domain plus zinc finger motifs
- 3.2 Класс: Paired box
- 3.2.1 Семейство: Paired plus homeo domain
- 3.2.2 Семейство: Paired domain only
- 3.3 Класс: Fork head / winged helix
- 3.3.1 Семейство: Developmental regulators; includes forkhead
- 3.3.2 Семейство: Tissue-specific regulators
- 3.3.3 Семейство: Cell-cycle controlling factors
- 3.3.0 Семейство: Other regulators
- 3.4 Класс: Heat Shock Factors
- 3.4.1 Семейство: HSF
- 3.5 Класс: Tryptophan clusters
- 3.5.1 Семейство: Myb
- 3.5.2 Семейство: Ets-type
- 3.5.3 Семейство: Interferon regulatory factors
- 3.6 Класс: TEA (transcriptional enhancer factor) domain
- 3.1 Класс: Гомеодомен
- 4 Надкласс: beta-Scaffold Factors with Minor Groove Contacts
- 4.1 Класс: RHR (Rel homology region)
- 4.2 Класс: STAT
- 4.2.1 Семейство: STAT
- 4.3 Класс: p53
- 4.3.1 Семейство: p53
- 4.4 Класс: MADS box
- 4.4.1 Семейство: Regulators of differentiation; includes (Mef2)
- 4.4.2 Семейство: Responders to external signals, SRF (serum response factor) (SRF)
- 4.4.1 Семейство: Regulators of differentiation; includes (Mef2)
- 4.5 Класс: beta-Barrel alpha-helix transcription factors
- 4.6 Класс: TATA binding proteins
- 4.8 Класс: Heteromeric CCAAT factors
- 4.8.1 Семейство: Heteromeric CCAAT factors
- 4.9 Класс: Grainyhead
- 4.9.1 Семейство: Grainyhead
- 4.10 Класс: Cold-shock domain factors
- 4.10.1 Семейство: csd
- 4.11 Класс: Runt
- 4.11.1 Семейство: Runt
- 0 Надкласс: Другие факторы транскрипции
- 0.1 Класс: Copper fist proteins
- 0.2 Класс: HMGI(Y) (HMGA1)
- 0.2.1 Семейство: HMGI(Y)
- 0.3 Класс: Pocket domain
- 0.4 Класс: E1A-like factors
- 0.5 Класс: AP2/EREBP-related factors
Систему CRISPR можно адаптировать так, чтобы она действовала как транскрипционный фактор (crisprTF). Для этого CRISPR-ассоциированный белок, известный как Cas9, изменяют так, чтобы он после связывания с ДНК больше не мог её расщепить. Затем к нему добавляют сегмент, который активирует или подавляет экспрессию генов путём модуляции транскрипционного механизма клетки[44][45][46][47]. В отличие от транскрипционных факторов на базе цинковых пальцев и TAL-эффектора, для узнавания ДНК системе CRISPR-Cas требуется только создание соответствующей последовательности РНК-«гида», а не создание новых белковых доменов фермента, что делает его гораздо более доступным благодаря дешевизне и простоте (вплоть до того что разработан набор правил — «грамматика» — описывающих, как спроектировать синтетический транскрипционный фактор (STFS) и программа для его автоматизированного проектирования[48]).