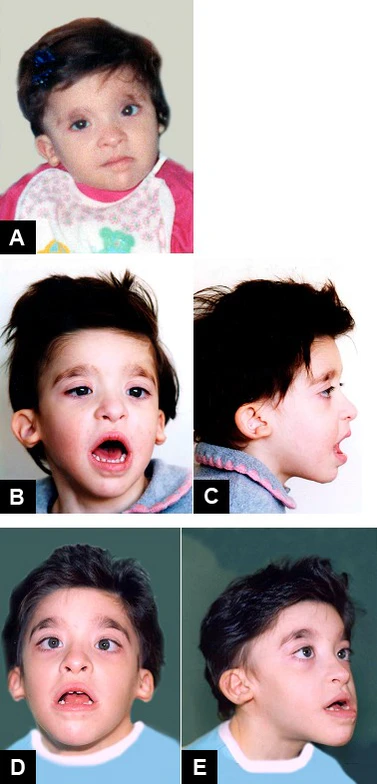
Синдром Мовата–Вильсон
Синдром Мовата-Вильсон — это генетическое заболевание, характеризующееся множественными врождёнными пороками развития. Заболевание также сопровождается специфическими чертами внешности, интеллектуальной недостаточностью и эпилептическими приступами. Синдром развивается в результате мутаций или делеций гена ZEB2[2].
Что важно знать
История
Заболевание было впервые описано в 1998 году детским неврологом Дэвидом Р. Моватом и клиническим генетиком Мередит Дж. Вильсон. В 2001 году две независимые группы исследователей установили причину синдрома Мовата-Вильсона (СМВ), обнаружив мутации или делеции гена ZEB2. Это открытие было сделано на основе изучения двух случаев спонтанных транслокаций, а также выявления мутаций у нескольких пациентов с данным заболеванием[2][3].
Этиология
Большинство мутаций в гене ZEB2 относятся к типу сдвига рамки считывания, что приводит к образованию преждевременного стоп-кодона. На втором месте по частоте находятся нонсенс-мутации. В некоторых случаях наблюдается полная делеция гена[4][5].
Мутации в гене ZEB2 приводят к образованию нефункционального или недостаточного количества белка ZEB2, что вызывает развитие СМВ. Изменённый белок не способен выполнять свои нормальные регуляторные функции в сложных процессах эмбрионального развития, что оказывает каскадное влияние на экспрессию других генов, участвующих в формировании нервной системы, лица и внутренних органов. Белок ZEB2 играет ключевую роль в функционировании клеток, участвуя в важных сигнальных путях, особенно в сигнальном пути трансформирующего фактора роста бета. Благодаря этому взаимодействию он регулирует клеточные ответы и процессы развития. Кроме того, ZEB2 может играть важную роль в восстановлении гистондеацетилазы[4].
Эпидемиология
Распространённость СМВ в настоящее время неизвестна, однако предполагается, что заболевание часто остаётся недиагностированным, особенно у пациентов без болезни Гиршпрунга. С момента первого описания синдрома Моватом и коллегами в 1998 году было зарегистрировано около 171 пациента с мутациями, делециями или цитогенетическими аномалиями гена ZEB2, преимущественно из Северной Европы, Австралии, Италии и США. Синдром выявлен у представителей различных этнических групп, при этом клинические проявления заболевания схожи во всех популяциях. СМВ встречается как у мужчин, так и у женщин[3][6].
Клиническая картина
Рост и масса тела
При рождении рост и масса тела обычно находятся в пределах нормы. Микроцефалия чаще приобретённая, но может выявляться уже при рождении. Низкорослость становится заметна с возрастом: средний рост у взрослых составляет 165 см у мужчин и 150 см у женщин. Телосложение часто худощавое[2].
Глаза
Примерно у половины больных наблюдается косоглазие, реже встречаются астигматизм и миопия. У детей младшего возраста может отмечаться нистагм, который с возрастом проходит. Также возможны микрофтальм, птоз, катаракта и аплазия сетчатки[2].
Уши
У трети больных отмечаются рецидивирующие отиты, приводящие к тугоухости[2].
Зубы
Наблюдаются нарушение роста зубов, широкие межзубные промежутки, гипертрофия дёсен и бруксизм[2].
Сердечно-сосудистая система
Врождённые пороки сердца встречаются у 60 % больных. Наиболее распространены стеноз лёгочной артерии, коарктация аорты, аномалии клапанов и тетрада Фалло. Стеноз лёгочной артерии может сочетаться со стенозом трахеи[2].
Желудочно-кишечный тракт
При поражении желудочно-кишечного тракта чаще всего встречаются болезнь Гиршпрунга, пилоростеноз и дисфагия[2].
Мочевыделительная система
Аномалии почек встречаются у 25 % больных: пузырно-мочеточниковый рефлюкс, гидронефроз, реже — удвоение почки, тазовая почка и поликистоз почек[2].
Половая система
У мужчина часто наблюдается гипоспадия и крипторхизм[2].
Костно-мышечная система
Характерными признаками являются длинные пальцы, задержка ядер окостенения у детей, синдактилия. С возрастом развиваются деформации межфаланговых суставов, плоскостопие, сколиоз, камптодактилия, вальгусная деформация[2].
Неврологические нарушения
Мышечная гипотония особенно характерна для детей до 1 года, после чего постепенно нарастают спастические изменения, формируются контрактуры и остеопороз. Эпилепсия встречается почти у 80 % больных[2].
Когнитивные функции и поведение
Характерна умственная отсталость. Речевое развитие нарушено, обычно речь ограничивается отдельными словами или простыми фразами. Психомоторное развитие задержано, многие пациенты начинают ходить только к 2-4 годам. Самообслуживание развито слабо, часто отмечается недержание мочи и кала[2].
Сон
Нарушения сна наблюдаются у 50 % пациентов, включая частые или ранние пробуждения[2].
Редкие случаи
Описаны единичные случаи осложнений анестезии из-за узких дыхательных путей, холестаз, медуллобластома, глиобластома и рабдомиосаркома[2].
Диагностика
Электроэнцефалография: основной ритм замедлен, отмечаются нерегулярные диффузные асимметричные разряды пик-медленная волна с бифронтальным акцентом. Во время медленного сна изменения наиболее выражены. Электрический эпилептический статус сна коррелирует с нарушениями поведения и когнитивным дефицитом[2].
Магнитно-резонансная томография головного мозга: изменения выявляются в половине случаев, чаще — аномалии мозолистого тела (гипоплазия, агенезия). Также наблюдаются расширение желудочков, аномалии гиппокампа, кортикальные мальформации, лейкопатия и аномалии задней черепной ямки[2].
Для исключения крупных делеций или транслокаций проводится цитогенетический анализ. Метод флeоресцентной гибридизации in situ позволяет выявить субмикроскопические делеции. Секвенирование полной кодирующей последовательности гена ZEB2 идентифицирует мутации[3].
Цитогенетическая анализ: использование полимеразной цепной реакции в реальном времени позволяет обнаружить другие перестройки, которые не выявляются традиционными методами[3].
Дифференциальная диагностика
Дифференциальную диагностику СМВ проводят со следующими состояниями:
2. Синдром Рубинштейна — Тайби
4. Синдром Гольдберга-Шпринцена
Лечение
Лечение СМВ должно быть индивидуальным и направленным на специфические особенности клинической картины каждого пациента, с привлечением команды специалистов, включая неврологов, кардиологов и хирургов. Для коррекции сопутствующих состояний (болезнь Гиршпрунга, пороки сердца и эпилептические приступы) применяются хирургические вмешательства, антиэпилептические препараты и реабилитационные методы (физиотерапия, эрготерапия, логопедическая терапия). Пациентам с иммунодефицитом рекомендуется специфическая вакцинация и, в некоторых случаях, профилактический приём антибиотиков[6].
Прогноз
Летальность при СМВ зависит от тяжести врождённых аномалий. Пациенты могут доживать до раннего взрослого возраста, но обычно нуждаются в помощи в повседневной жизни[7].
Примечания
Литература
- Livia Garavelli, Paola Cerruti Mainardi. Mowat-Wilson syndrome (англ.) // Orphanet Journal of Rare Diseases. — 2007-10-24. — Vol. 2, iss. 1. — ISSN 1750-1172. — doi:10.1186/1750-1172-2-42.
- Yalda Zhoulideh, Jamil Joolideh. Mowat-Wilson syndrome: unraveling the complexities of diagnosis, treatment, and symptom management (англ.) // Egyptian Journal of Medical Human Genetics. — 2024-03-27. — Vol. 25, iss. 1. — ISSN 2090-2441. — doi:10.1186/s43042-024-00517-2.