Болезнь Кеннеди
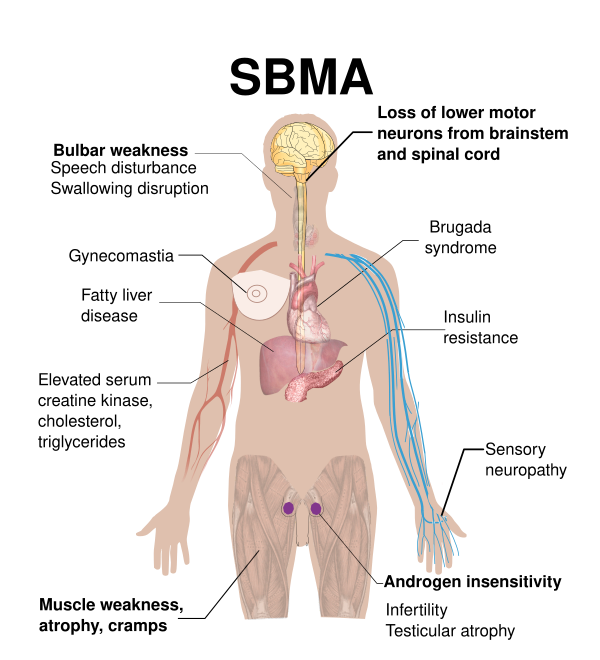
Боле́знь Ке́ннеди (бульбоспина́льная мы́шечная атрофи́я Ке́ннеди) — редкое наследственное заболевание, при котором постепенно разрушаются мотонейроны. Оно проявляется слабостью и атрофией мышц, особенно в верхних и нижних конечностях, а также бульбарными нарушениями. Характерным признаком являются частые фасцикуляции. Кроме неврологических симптомов, у пациентов часто наблюдают гинекомастию, уменьшение размеров яичек, бесплодие, снижение чувствительности к мужским гормонам и развитие сахарного диабета. Болезнь прогрессирует медленно, но неуклонно[1].
Общие сведения
История
Болезнь Кеннеди (БК) получила своё название в честь исследователя У. Р. Кеннеди и его коллег, которые впервые описали это заболевание, наблюдая за 11 пациентами из двух семей. Учёные отметили, что болезнь наследуется по рецессивному типу. Позже, в 1982 году, другая группа исследователей классифицировала это заболевание как X-сцепленную бульбоспинальную невропатию, указав на её ключевые особенности: помимо поражения двигательных нейронов, у пациентов также наблюдалась сенсорная невропатия. В 1991 году была установлена генетическая причина болезни — экспансия CAG-повторов в первом экзоне гена андрогенового рецептора (АР). Это открытие позволило точнее диагностировать заболевание и изучить его механизмы развития[1].
Этиология
БК входит в группу полиглутаминовых заболеваний, поскольку в поражённых мотонейронах обнаруживаются внутриядерные включения, содержащие белки с избыточным количеством полиглутаминовых повторов. Это заболевание вызвано мутацией в гене АР, который расположен на X-хромосоме (локус Xp11.2-12). Патологический механизм связан с увеличением числа CAG-повторов в первом экзоне этого гена. В норме их количество колеблется от 10 до 36, тогда как у пациентов с БК оно возрастает до 38—72. Интересно, что в медицинской литературе описаны редкие случаи гомозиготного носительства CAG-экспансии у женщин. Однако, в отличие от мужчин, у них заболевание проявляется в очень лёгкой форме — эпизодическими судорогами, тремором рук и нечастыми фасцикуляциями[2].
Патогенез
Точный механизм, с помощью которого экспансия CAG-повторов приводит к нейродегенерации, остаётся не до конца изученным. Общим патоморфологическим признаком всех полиглутаминовых болезней является образование внутриядерных включений, состоящих из неправильно свёрнутых белков с расширенными полиглутаминовыми участками, в поражённых нейронах. При БК накоплены данные, свидетельствующие о том, что токсичность мутантного белка обусловлена андроген-зависимым приобретением патологической функции рецептора (андроген-зависимая нейродегенерация). У здоровых людей связывание андрогенов с рецептором приводит к его транспорту в ядро и регуляции андроген-чувствительных элементов генома. В случае БК это взаимодействие вызывает агрегацию мутантного рецептора, формирование внутриядерных включений (в тканях, где он экспрессируется) и нарушение его нормальной функции. Токсичность мутантного АР опосредована дисрегуляцией транскрипции, а также другими, пока недостаточно изученными механизмами. Однако важную роль играет и утрата нормальной функции рецептора, что объясняет возникновение гинекомастии и снижения фертильности. У больных наблюдается дегенерация мотонейронов передних рогов спинного мозга. Помимо нейрогенной мышечной атрофии, в мышцах также отмечаются признаки первичного миопатического процесса. Мутантный АР выявляется в виде включений при иммуногистохимическом исследовании. Точный механизм вовлечения мотонейронов и мышц в патогенез БК до конца не ясен. Исследования на мышиных моделях частично подтверждают гипотезу о том, что дегенерация скелетных мышц может быть первичным звеном, приводящим впоследствии к дисфункции и гибели мотонейронов[3].
Эпидемиология
БК относится к крайне редким заболеваниям в большинстве популяций, поэтому исследования её распространённости немногочисленны. Исследование в Великобритании выявило лишь 61 пациента за 9 лет, несмотря на создание национального регистра заболевания. Истинная распространённость болезни может быть недооценена из-за низкой осведомлённости врачей. Часто цитируемый показатель 1—2 случая на 100 000 населения, вероятно, отражает недостаточную диагностику. По некоторым оценкам, распространённость достигает 1 случая на 40 000, тогда как в итальянском регионе Реджо-Эмилия этот показатель составил 1,6 на 100 000. Отмечаются эффекты основателя, особенно в генетически изолированных популяциях — например, в регионе Вааса (Западная Финляндия) частота достигает 13 случаев на 85 000 мужского населения. Подобный эффект наблюдается и в японской популяции, что объясняет более высокую распространённость БК среди японцев по сравнению с другими этническими группами. БК проявляется преимущественно у мужчин после 40 лет, при этом средний возраст дебюта составляет 45—55 лет. В более редких случаях заболевание может развиться до 40 или после 70 лет[3][4].
Клиническая картина
Основными клиническими проявлениями БК являются мышечная слабость и атрофия конечностей, бульбарные нарушения, тремор, судороги, фасцикуляции, сенсорная невропатия, гинекомастия и сексуальная дисфункция. Описана внутрисемейная вариабельность клинических симптомов[3][4].
Поскольку БК является болезнью нижних мотонейронов, основным двигательным симптомом выступает мышечная слабость. Наиболее частой жалобой, с которой пациенты обращаются за медицинской помощью, является слабость в нижних конечностях (90 % случаев). Однако другие симптомы, такие как судороги или тремор, могут предшествовать появлению слабости. На ранних стадиях заболевания слабость в нижних конечностях обычно носит проксимальный характер, что может служить важным дифференциально-диагностическим признаком в сравнении с дистальными наследственными моторными невропатиями. Тремор чаще всего представляет собой высокочастотный постуральный тремор рук, хотя у некоторых пациентов также отмечается постуральный тремор ног. При осмотре выявляются мышечная атрофия, фасцикуляции, снижение или отсутствие сухожильных рефлексов. Бульбарные нарушения редко бывают первым симптомом и обычно развиваются после появления слабости в ногах. Они проявляются фасцикуляциями языка с образованием срединной борозды вследствие атрофии его мышц, периоральными фасцикуляциями-миокимией, дизартрией и дисфагией. Последняя встречается почти у 80 % пациентов, особенно на поздних стадиях болезни. У части больных наблюдаются ларингоспазмы. Дыхательная недостаточность встречается редко, даже на поздних стадиях заболевания. Однако при появлении любых признаков дыхательных нарушений необходимо провести соответствующее обследование[3].
Более чем у половины пациентов с БК наблюдаются сенсорные симптомы (онемение, покалывание), преимущественно в дистальных отделах конечностей, обычно на поздних стадиях заболевания. Хотя вегетативная нервная система формально не считается мишенью при БК, существуют данные о её субклиническом вовлечении[3].
У мужчин с БК часто отмечаются признаки андрогенной резистентности: гинекомастия, снижение фертильности и атрофия яичек, иногда проявляющиеся уже в подростковом возрасте. Характерны олигоспермия и эректильная дисфункция. У многих пациентов выявляются метаболические расстройства. В отдельных исследованиях описана неалкогольная жировая болезнь печени[3].
Наиболее распространённым расстройством сна является обструктивное апноэ (22 % пациентов также имеют синдром периодических движений конечностей во сне).
Более 40 % пациентов имеют симптомы дизурии без признаков гиперплазии простаты. Предполагается роль андрогенного дефицита в развитии этих нарушений[3].
Диагностика
Лабораторная диагностика включает[3][4]:
- биохимический анализ крови: наблюдается повышение активности креатинкиназа, аспартатаминотрансферазы, аланинаминотрансферазы, дислипидемия, гипергликемия и гиперхолестеринемия;
- иммунохимический анализ: определяется снижение концентрации тестостерона;
- молекулярно-генетический анализ на наличие мутации в гене AR.
Инструментальная диагностика[3]:
- электромиография: характерно снижение амплитуд сенсорных потенциалов при сохранной скорости проведения по моторным нервам. Часто обнаруживают сочетание нейрогенных изменений (денервация) с миопатическими паттернами (укороченные потенциалы);
- электрокардиграфия: выявляются изменения по типу синдрома Бругада (подъём сегмента ST в правых грудных отведениях);
- компьютерная томография и магнитно-резонансная томография демонстрируют уменьшение объёма серого вещества (особенно в лобных долях) и атрофию белого вещества. Позитронно-эмиссионная томография выявляет снижение метаболизма глюкозы в лобных областях.
Дифференциальная диагностика
Дифференциальную диагностику БК проводят со следующими состояниями[2][3]:
- боковой амиотрофический склероз;
- болезнь Кугельберга — Веландера (III тип);
- спинальная мышечная атрофия типа IV;
- дистальные наследственные моторные невропатии;
- метаболические миопатии;
- миастения;
- полимиозит;
- прогрессирующая мышечная атрофия;
- структурные поражения спинного мозга;
- паранеопластические синдромы;
- хроническое отравление свинцом;
- синдром Клайнфелтера.
Осложнения
К возможным осложнениями БК относятся[3]:
- ограничение подвижности;
- дыхательная недостаточность;
- дисфагия;
- аспирационная пневмония;
- контрактуры суставов;
- дислипидемия;
- нарушения мочеиспускания;
- остеопороз;
- деформации позвоночника;
- нарушения сна;
- обструктивное апноэ сна;
- депрессия;
- когнитивные нарушения.
Лечение
На 2025 год эффективного лечения БК не существует. Основу ведения больных составляет симптоматическое лечение, включающее в себя ноотропные препараты и витамины группы В, умеренные физические нагрузки и предупреждение соматических осложнений[4].
К методам лечения, находящимся на стадии изучения, относятся[3]:
- подавление андрогенов: лейпролид представляет собой аналог гормонов, который снижает уровень тестостерона. В ходе исследований было выявлено, что он способен замедлять прогрессирование болезни, однако значительного улучшения функциональных показателей не наблюдается. Дутастерид является ингибитором 5α-редуктазы, блокируя образование дигидротестостерона. Однако в рамках двухлетнего клинического исследования его эффективность не была подтверждена;
- анаболические агенты: кленбутерол, относящийся к β2-агонистам, в ходе пилотного исследования продемонстрировал улучшение результатов 6-минутного теста ходьбы и показателей жизненной ёмкости лёгких у пациентов;
- генная терапия: РНК-интерференция направлена на подавление экспрессии мутантного гена АР. Данный подход успешно прошёл испытания на доклинических моделях, демонстрируя перспективность для дальнейшего изучения.
Диспансерное наблюдение
Ежегодное диспансерное наблюдение включает в себя[5]:
- оценку мышечной силы, подвижности и способности к повседневной деятельности;
- контроль речевых и глотательных функций;
- исследование функции лёгких (при прогрессирующей стадии);
- обследование сердечно-сосудистой системы.
Профилактика
Не разработана.