Синдром Гиллеспи
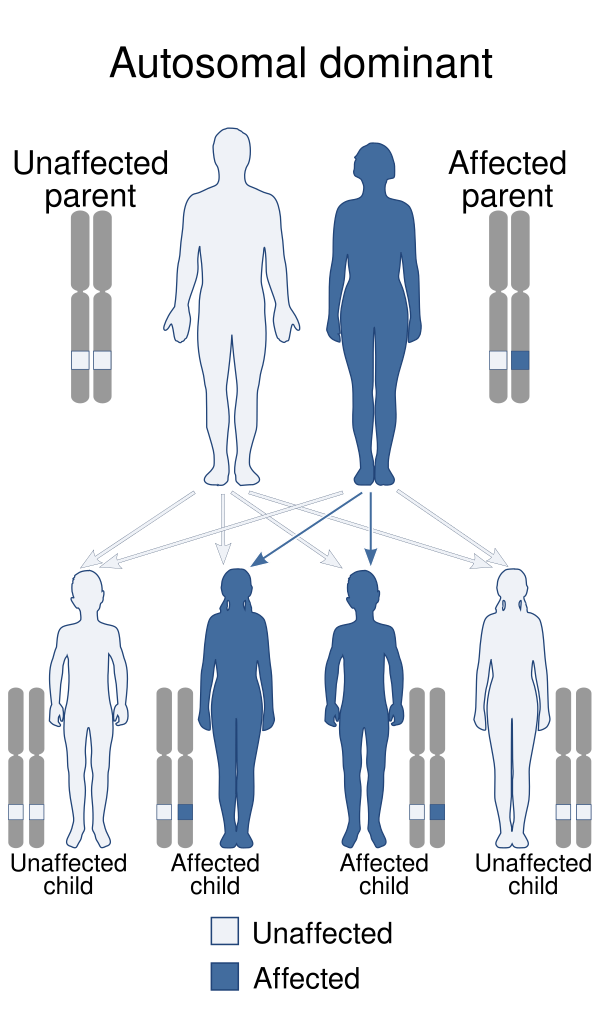
Синдро́м Гилле́спи (СГ) — редкое моногенное заболевание, характеризующееся врождённой мышечной гипотонией, задержкой психомоторного и речевого развития, атаксией и гипоплазией радужной оболочки глаз. СГ может наследоваться как по аутосомно-рецессивному, так и по аутосомно-доминантному типу. Патология развивается вследствие различных мутаций в гене ITPR1, расположенном на коротком плече 3-й хромосомы (3p26). Этот ген кодирует белок — инозитол-1,4,5-трифосфатный рецептор, который функционирует как кальциевый канал в мембранах эндоплазматического ретикулума и аппарата Гольджи. Данный белок играет ключевую роль в системе внутриклеточной кальциевой сигнализации, что объясняет многообразие клинических проявлений синдрома[2].
Что важно знать
История
В качестве самостоятельного заболевания СГ был выделен в 1965 году Ф. Д. Гиллеспи, который описал клинический случай брата и сестры 19 и 22 лет с характерной триадой симптомов: аниридией, нарушением координации движений и умственной отсталостью. Исследователь высказал предположение об аутосомно-рецессивном механизме наследования этой патологии[2].
В 2016 году исследовательская группа под руководством Гербера установила, что причиной развития СГ являются либо доминантно-негативные патогенные варианты, либо рецессивные мутации гена ITPR1[3].
Этиология
Развитие СГ связано с различными типами мутаций в гене ITPR1, включая гомозиготные, компаунд-гетерозиготные и гетерозиготные варианты. Этот ген расположен на хромосоме 3p26 и состоит из 62 экзонов. Он кодирует инозитол-1,4,5-трифосфатный рецептор — белок, функционирующий как кальциевый канал в мембранах эндоплазматического ретикулума и аппарата Гольджи, который играет ключевую роль в регуляции внутриклеточного кальциевого обмена. В гене ITPR1 идентифицировано более 50 различных мутаций. Однако только 10 из них были обнаружены у пациентов с клинически подтверждённым диагнозом СГ, что свидетельствует о неполной пенетрантности и вариабельной экспрессивности генетических изменений[2].
Патогенез
Ген ITPR1 кодирует белок инозитол-1,4,5-трифосфатный рецептор 1-го типа, который регулирует высвобождение кальция из эндоплазматического ретикулума. Этот белок особенно активно экспрессируется в клетках Пуркинье мозжечка, играя ключевую роль в обеспечении двигательной координации[4].
Мутации в гене ITPR1 приводят к нарушению функции кальциевых каналов и сбоям в регуляции высвобождения кальция. Эти патологические изменения вызывают дегенеративные процессы в центральной нервной системе, что клинически проявляется характерными симптомами[4].
Эпидемиология
СГ представляет собой исключительно редкое заболевание. С момента его первого описания в 1965 году в мировой литературе было зарегистрировано менее 100 случаев, причём только у 37 пациентов диагноз подтверждён молекулярно-генетическими методами (в 29 случаях выявлены доминантные варианты мутации, в 8 — рецессивная форма заболевания)[3].
Диагностика
Клиническая картина СГ включает характерные офтальмологические и неврологические проявления. С рождения отмечается двусторонняя частичная аниридия, проявляющаяся фиксированно расширенными зрачками с фестончатыми краями гипоплазированной радужной оболочки. Пациенты испытывают светобоязнь, жалуются на нечёткость зрения, у них наблюдается нистагм. В редких случаях выявляются дополнительные глазные аномалии: гипоплазия фовеолы, мозаичная гипоплазия радужки и зрительного нерва, гипопигментация сетчатки, пигментные изменения жёлтого пятна, приводящие к снижению остроты зрения[5].
Неврологическая симптоматика представлена непрогрессирующей мозжечковой атаксией, которая сочетается с задержкой моторного развития и мышечной гипотонией, заметными уже на первом году жизни. Характерны нарушения походки и равновесия, дискоординация движений, интенционный тремор и скандированная речь. Умственная отсталость варьирует от лёгкой до умеренной степени выраженности[5].
У части пациентов отмечаются незначительные дизморфические черты лица: высокий лоб, гипертелоризм, эпикантус, уплощённая переносица с вывернутыми вперёд ноздрями, тонкая верхняя губа, низко расположенные ушные раковины. Поражение других органов нехарактерно, хотя в отдельных случаях описаны врождённые пороки сердца и скелетные аномалии[5].
При компьютерной и магнитно-резонансной томографии у пациентов с СГ выявляются характерные изменения мозжечка в виде его гипоплазии или атрофии, наиболее выраженные в области червя. В некоторых случаях могут также обнаруживаться сопутствующие изменения белого вещества головного мозга и другие аномалии мозжечковых структур[6].
При офтальмоскопии: край зрачка радужной оболочки имеет характерный фестончатый или «зубчатый» вид, при этом отдельные тяжи радужки равномерно распространяются на переднюю поверхность хрусталика[5].
Молекулярно-генетический анализ: характерно выявление мутации гене ITPR1 методом секвенирования[5].
Дифференциальная диагностика
Дифференциальная диагностика СГ проводится со следующими состояниями[5][7]:
- синдром Маринеску — Шёгрена;
- спиноцеребеллярная атаксия 29-го типа;
- спиноцеребеллярная атаксия 15-го типа.
Лечение
Лечение СГ направлено на коррекцию конкретных симптомов у каждого пациента и требует скоординированной работы мультидисциплинарной команды специалистов. Пациентам с выраженными неврологическими проявлениями могут быть показаны: физиотерапия, специальная коррекционная программа обучения, логопедическая помощь[8].
Прогноз
Данные о естественном течении СГ в литературе отсутствуют, однако имеющиеся наблюдения позволяют предположить, что заболевание не сокращает продолжительность жизни пациентов. Прогноз в значительной степени зависит от качества медицинского сопровождения, включающего своевременную коррекцию офтальмологических нарушений и адекватную терапию неврологических и когнитивных расстройств[8].
Примечания
Литература
- Васильева Т. А., Воскресенская А. А., Хлебникова О. В., Поздеева Н. А., Марахонов А. В., Зинченко Р. А. Дифференциальная диагностика наследственных форм врождённой аниридии с позиций современной генетики // Вестник Российской академии медицинских наук. — 2017. — № 4.
- Васильева Т. А., Поздеева Н. А., Воскресенская А. А., Хлебникова О. В., Зинченко З. А., Гинтер Е. К. Генетические аспекты врождённой аниридии // Практическая медицина. — 2015. — № 2—1 (87).