Синдром Аксенфельда — Ригера
Синдро́м Аксенфе́льда — Ри́гера (САГ) — редкое генетическое заболевание, проявляющееся врождёнными аномалиями развития глаз, зубов, деформацией ушных раковин и наличием пупочной грыжи. Симптомы заболевания проявляются либо внутриутробно, либо вскоре после рождения[1].
История
В 1920—1930-х годах немецкий офтальмолог Теодор Аксенфельд описал аномалию развития глаз, включавшую задний эмбриотоксон и корэктопию. Примерно в тот же период австрийский исследователь Густав Ригер выделил схожий синдром, для которого были характерны недоразвитие радужки (гипоплазия), ложное множественное зрачковое отверстие (псевдополикория), задний эмбриотоксон, а также системные нарушения других органов. Поскольку оба состояния имели сходные клинические проявления и могли встречаться у членов одной семьи, в 1983 году их объединили под общим названием — синдром Аксенфельда — Ригера[2].
Классификация
САГ классифицируется по мутации в гене, лежащем в основе заболевания:
- тип 1 вызывается мутациями в гене PITX2 (4q25);
- тип 3 связан с мутациями FOXC1 (6p25);
- тип 2 менее изучен, потенциально может быть ассоциирован с FOXO1A (13q14)[3].
Этиология
САГ 1-го типа — аутосомно-доминантное заболевание, вызванное гетерозиготной мутацией в гене PITX2, расположенном на хромосоме 4q25. Ген PITX2 является гомеобоксным транскрипционным фактором, играющим ключевую роль в развитии зубов и радужки.
САГ 2-го типа — аутосомно-доминантное заболевание, связанное с хромосомой 13q14. Фенотип или локус мутации известны, но молекулярная основа пока не установлена.
САГ 3 — аутосомно-доминантное заболевание, ассоциированное с хромосомой 6p25.3, в частности с геном FOXC1. Гетерозиготные мутации в гене FOXC1 приводят к развитию САГ 3-го типа.
Примерно 25—30 % случаев с офтальмологическими проявлениями САГ коррелируют с мутациями в генах FOXC1 и PITX2 на хромосомах 6p25 и 4q25 соответственно. Гены FOXC1 (Forkhead-Box C1) и PITX2 (Pituitary Homeobox 2) являются наиболее изученными транскрипционными факторами. Мутации FOXC1 включают фреймшифт-, нонсенс-, миссенс-мутации, делеции и дупликации. Мутации PITX2 включают сайты сплайсинга, делеции и хромосомные транслокации у пациентов с САГ[3].
Белки, кодируемые этими генами, представляют собой полифункциональные транскрипционные факторы. Белки PITX2 и FOXC1, а также транскрипционный фактора роста бета-2 являются участниками одного сигнального каскада. Нарушение работы любого из этих регуляторных факторов приводит к серьёзным, часто фенотипически сходным аномалиям развития глаза[1].
Патогенез
САГ возникает вследствие нарушения миграции клеток нервного гребня на ранних этапах эмбриогенеза. Ключевые структуры глаза (цилиарное тело, роговица и строма радужки) зависят от правильной миграции клеток нервного гребня. Эти процессы строго регулируются транскрипционными факторами различных генов.
На поздних сроках гестации эндотелий, покрывающий роговицу, в норме подвергается резорбции. Нарушение этого процесса может привести к формированию заднего эмбриотоксона и аномальному прикреплению радужки, что вызывает изменения зрачка. Аномалии развития передней камеры глаза могут влиять на формирование шлеммова канала, нарушая отток водянистой влаги и повышая риск развития глаукомы.
Патологическая миграция клеток нервного гребня при САГ часто затрагивает и внеглазные ткани, включая вестибуло-акустический ганглий, что у некоторых пациентов может проявляться нарушением слуха[3].
Гистологическая картина при САГ демонстрирует признаки аномального разделения переднего сегмента глаза, включая выраженную линию Швальбе, гипоплазию шлеммова канала, недоразвитие радужки, гипоклеточность трабекулярной сети и иридокорнеальные сращения. Характерно, что данные изменения преимущественно локализуются со стороны смещения зрачка или эктропиона увеальной ткани, а также в противоположном квадранте от атрофированного участка радужки[3].
Эпидемиология
Диагностика
САГ характеризуется сочетанием глазных, зубных, лицевых и абдоминальных аномалий. В большинстве случаев диагноз устанавливается в младенческом или детском возрасте, хотя глаукома может развиться в позднем детском возрасте или даже у взрослых. В редких случаях возможна врождённая или ранняя глаукома (диагностируемая в первые 3 года жизни).
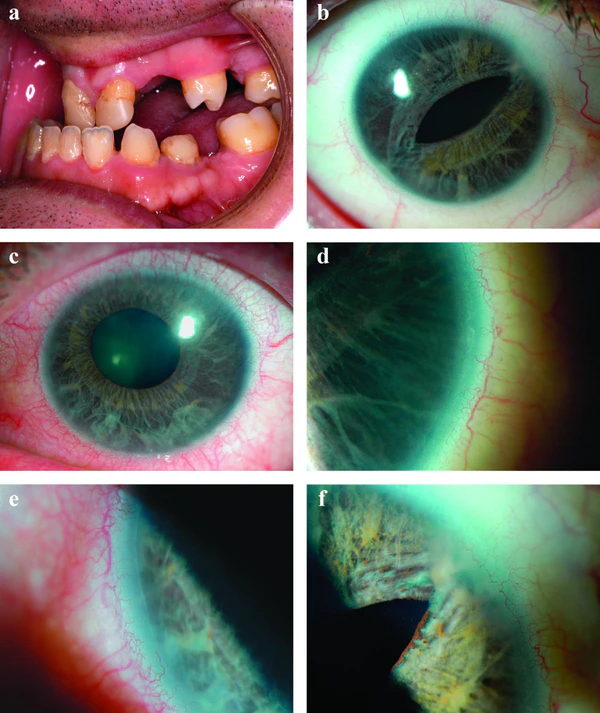
Клинические проявления врождённой глаукомы включают увеличенную голубоватую роговицу (буфтальм), слезотечение и светобоязнь. Типичные жалобы включают необычный внешний вид глаз, косоглазие или снижение зрения. Светобоязнь обусловлена аномалиями радужки и зрачка. Аномалии радужки при АГС включают сквозные дефекты («дыры») радужки, создающие эффект множественных зрачков (псевдополикория), смещение зрачка (корэктопия) и эктропион увеальной ткани. В некоторых случаях радужка может выглядеть нормальной. Другие глазные проявления включают передние периферические синехии, помутнение роговицы, мегалокорнеа, микрокорнеа и глаукому[3][4].
Типичные стоматологические аномалии включают гиподонтию (отсутствие 1—5 зубов), олигодонтию (отсутствие 6 и более зубов) и микродонтию (уменьшенные размеры зубов). Характерные лицевые особенности: лёгкая краниофациальная дисморфия, телекантус, гипертелоризм, гипоплазия верхней челюсти и широкая уплощённая переносица. К другим системным проявлениям относятся гипоспадия, избыток кожи вокруг пупка, пупочная грыжа, гидроцефалия, тугоухость, стриктура заднего прохода, почечные аномалии, пороки сердечных клапанов, арахноидальные кисты, аномалии гипофиза («пустое турецкое седло»), эндокринные нарушения (низкорослость, задержка роста) и врождённый вывих бедра[3][4].
Гониоскопия играет ключевую роль в диагностике САГ, позволяя детально оценить состояние иридокорнеального угла. При проведении исследования типично выявляют[3]:
- выраженную линию Швальбе;
- тяжи радужки, прикреплённые к линии Швальбе;
- переднее прикрепление радужки.
Молекулярно-генетический анализ: выявление мутаций в генах PITX2 и FOXC1 [3].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими состояниями[3][5]:
- иридогониодисгенез;
- аномалия Петерса;
- первичная врождённая глаукома;
- иридокорнеальный эндотелиальный синдром;
- иридошизис;
- аниридия;
- изолированный задний эмбриотоксон;
- окулодентодигитальная дисплазия;
- врождённый увеальный эктропион;
- эктопия хрусталика и зрачка.
Осложнения
Лечение
При выявлении глаукомной оптической нейропатии в первую очередь рекомендуется медикаментозная терапия, и только при её неэффективности рассматривается вопрос о хирургическом вмешательстве. Наиболее эффективными препаратами считаются средства, уменьшающие продукцию водянистой влаги (β-блокаторы, α-агонисты и ингибиторы карбоангидразы), тогда как лекарства, влияющие на её отток, демонстрируют меньшую результативность[3].
В случаях врождённой глаукомы предпочтение отдаётся хирургическим методам коррекции. Дополнительно пациентам с выраженной светобоязнью, вызванной корэктопией и поликорией, могут быть рекомендованы специальные контактные линзы, маскирующие дефекты радужной оболочки[3].
Ряд клинических исследований изучал эффективность дренажных устройств при лечении глаукомы, ассоциированной с САГ. Результаты демонстрируют, что имплантация клапанных дренажных систем обеспечивает контроль внутриглазного давления примерно в 70 % случаев. Альтернативным методом хирургического лечения является транссклеральная циклофотокоагуляция, однако максимальная эффективность этого подхода достигается при его комбинировании с установкой дренирующих устройств[2].
Прогноз
Прогноз при САГ вариабелен и зависит от индивидуальных особенностей течения заболевания. У пациентов наблюдается широкий спектр клинических проявлений — от изолированных аномалий передней камеры глаза до сочетанных патологий, включая пороки сердца различной степени тяжести, которые могут существенно ухудшать общий прогноз. Офтальмологический прогноз благоприятен при отсутствии глаукомы, так как это состояние часто оказывается резистентным к медикаментозной терапии. Поздняя диагностика и несвоевременно начатое лечение глаукомы могут привести к необратимой слепоте и развитию фтизиса глазного яблока[3].
Примечания
Литература
- Маркитантова Ю. В., Фирсова Н. В., Смирнова Ю. А., Панова И. Г., Сухих Г. Т., Зиновьева Р. Д. Регуляторные факторы в контроле формирования сетчатки и ретинального пигментного эпителия в эмбриогенезе человека // Практическая медицина. — 2013. — № 1—3 (70).
- Seifi, M.; Walter, M. A. Axenfeld-Rieger syndrome (англ.) // Clinical Genetics : статья. — 2018. — Июнь (vol. 93, no. 6). — P. 1123–1130. — doi:10.1111/cge.13148.